题目内容
11.有一包固体,可能由硝酸铜、硫酸钠、氯化钠、碳酸氢钠、氢氧化钠中的一种或几种组成,为了探究该固体的组成,某化学小组设计并开展以下实验:
已知,步骤I中固体全部消失,溶液呈蓝色,无气泡产生.步骤II、III中均可观察到有白色沉淀生成.请回答下列问题:
(1)白色固体B的化学式为:AgCl;
(2)步骤II中产生白色沉淀的化学方程式是Ba(NO3)2+Na2SO4═BaSO4↓+2NaNO3;
(3)原固体中一定含有的物质是Cu(NO3)2、Na2SO4(写化学式,下同);
(4)原固体中一定不含有的物质是NaHCO3;
(5)原固体中可能含有的物质是NaCl、NaOH.
分析 根据固体加过量稀盐酸,固体完全溶解且溶液呈蓝色,说明固体中一定有硝酸铜;又因为无气泡产生,所以固体中一定不含有碳酸氢钠;步骤Ⅱ加入过量硝酸钡产生白色沉淀,说明固体中一定含有硫酸钠;步骤Ⅲ中加入硝酸银溶液,出现白色沉淀,则该白色沉淀为氯化银,由于一开始加入过量稀盐酸,所以溶液中一定有氯离子,所以会生成氯化银沉淀,但不能确定一定含有氯化钠.
解答 解:(1)通过推导可知,B是AgCl;
(2)步骤II中产生白色沉淀的反应是硝酸钡和硫酸钠反应生成硝酸钠和硫酸钡沉淀,化学方程式是Na2SO4+Ba(NO3)2=2NaNO3+BaSO4↓;
(3)固体加过量稀盐酸,固体完全溶解且溶液呈蓝色,说明固体中一定有硝酸铜;步骤Ⅱ加入过量硝酸钡产生白色沉淀,说明固体中一定含有硫酸钠;
(4)固体加过量稀盐酸无气泡产生,所以固体中一定不含有碳酸氢钠;
(5)原固体中可能含有的物质是NaCl、NaOH.
故答案为:(1)AgCl;
(2)Ba(NO3)2+Na2SO4═BaSO4↓+2NaNO3;
(3)Cu(NO3)2、Na2SO4;
(4)NaHCO3;
(5)NaCl、NaOH.
点评 本题主要考查盐的性质,要求学生熟练的掌握盐的水溶性,及两种盐之间的反应,并且知道无色的硝酸铜粉末溶于水后得到的溶液呈蓝色.

练习册系列答案
相关题目
1.水是生命之源,下列有关水的说法错误的是( )
| A. | 蒸馏水属于软水 | |
| B. | 电解水时产生氧气与氢气的体积比约为1:2 | |
| C. | 吸附能除去天然水中所有的杂质 | |
| D. | 水体污染主要来于工业污染、农业污染、生活污染 |
2.我国已研究出C1O2的新制法,其反应的微观过程如图所示,下列说法正确的是( )

| A. | ClO2中氯元素的化合价为+5价 | |
| B. | 该反应中的各微粒是不运动的 | |
| C. | 该反应符合质量守恒定律 | |
| D. | 该反应的化学方程式为:2Cl+NaClO2=2ClO2+2NaCl |
19.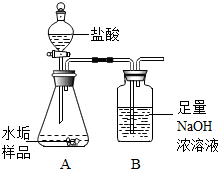 长期使用的水壶底部都结有一层水垢,其主要成分是碳酸钙和氢氧化镁.为较准确测定水垢中氢氧化镁的含量,实验小组分别取三份同样的水垢样品各7.00g,利用右图所示装置连续进行三次实验,并将每次实验中装置B的质量变化记录于下表:
长期使用的水壶底部都结有一层水垢,其主要成分是碳酸钙和氢氧化镁.为较准确测定水垢中氢氧化镁的含量,实验小组分别取三份同样的水垢样品各7.00g,利用右图所示装置连续进行三次实验,并将每次实验中装置B的质量变化记录于下表:
分析上面实验与数据后,回答:
(1)第一次实验测得数据较低的原因是第一次实验生成的二氧化碳没有全部进入B装置中区去;
(2)平均每份水垢样品中碳酸钙的质量为多少克?(列出计算过程)
(3)水垢样品中氢氧化镁的平均质量分数为28.6%.(计算结果精确到0.1)
 长期使用的水壶底部都结有一层水垢,其主要成分是碳酸钙和氢氧化镁.为较准确测定水垢中氢氧化镁的含量,实验小组分别取三份同样的水垢样品各7.00g,利用右图所示装置连续进行三次实验,并将每次实验中装置B的质量变化记录于下表:
长期使用的水壶底部都结有一层水垢,其主要成分是碳酸钙和氢氧化镁.为较准确测定水垢中氢氧化镁的含量,实验小组分别取三份同样的水垢样品各7.00g,利用右图所示装置连续进行三次实验,并将每次实验中装置B的质量变化记录于下表:| 第一次 | 第二次 | 第三次 | 平均值 | |
| B装置增加的质量(g) | 2.17 | 2.22 | 2.21 | 2.20 |
(1)第一次实验测得数据较低的原因是第一次实验生成的二氧化碳没有全部进入B装置中区去;
(2)平均每份水垢样品中碳酸钙的质量为多少克?(列出计算过程)
(3)水垢样品中氢氧化镁的平均质量分数为28.6%.(计算结果精确到0.1)
6.下列过程不属于物理变化过程的是( )
| A. | 晾干衣物 | B. | 冶炼金属 | C. | 蒸发结晶 | D. | 钢丝球刷碗 |
3.“低碳生活”倡导我们在生活中所耗用的能量、材料要尽量减少,从而减少二氧化碳排放量.下列做法不符合“低碳生活”理念的是( )
| A. | 教科书循环使用 | B. | 购物时用布袋代替塑料袋 | ||
| C. | 大量使用私家汽车出行,节约时间 | D. | 随手关灯,节约用电 |
1.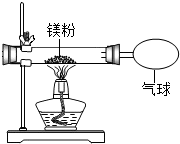 某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.
某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.
(1)请写出镁条与氧气反应的化学方程式2Mg+O2 $\frac{\underline{\;点燃\;}}{\;}$2MgO.
(2)小明发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵守质量守恒定律.我不同意(“同意”或“不同意”)小明的观点,因为所有的化学反应都遵循质量守恒定律.
(3)小红按如图装置改进实验,验证了质量守恒定律,却发现产物中还有少量黄色固体.
[提出问题]黄色固体是什么呢?
[查阅资料]
①氧化镁为白色固体
②镁能与氮气反应生成黄色的氮化镁(Mg3N2)固体;
③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝.
[做出猜想]黄色固体为Mg3N2
[反思与交流]空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成的氧化镁却远多于氮化镁,为什么?请给出合理的解释氧气的化学性质比氮气更活泼,镁条更容易与氧气发生反应.
(4)该兴趣小组又做了镁条与盐溶液反应的实验,发现均能产生H2,实验现象如下:
上表中,用水进行实验的目的是对比.
根据上表中的实验现象,请写出三条结论,并分析可能的原因(不分析原因,不得分):
①盐可以做镁与水反应的催化剂,因为盐能加快产生气体的速率;
②温度改变反应速率,因为升高温度可以加快产生气体的速率;
③升高温度能使反应更复杂,因为升高温度使镁与水反应的生成物在与盐反应生成氨气(NH3).
 某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.
某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.(1)请写出镁条与氧气反应的化学方程式2Mg+O2 $\frac{\underline{\;点燃\;}}{\;}$2MgO.
(2)小明发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵守质量守恒定律.我不同意(“同意”或“不同意”)小明的观点,因为所有的化学反应都遵循质量守恒定律.
(3)小红按如图装置改进实验,验证了质量守恒定律,却发现产物中还有少量黄色固体.
[提出问题]黄色固体是什么呢?
[查阅资料]
①氧化镁为白色固体
②镁能与氮气反应生成黄色的氮化镁(Mg3N2)固体;
③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝.
[做出猜想]黄色固体为Mg3N2
| 实验操作 | 实验现象及结论 |
| 将镁条燃烧的产物放在一只试管中,加入少量的蒸馏水,然后将一湿润的红色石蕊试纸放在试管口,观察现象; | 看到红色的石蕊试纸变成蓝色,说明黄色固体为氮化镁 |
(4)该兴趣小组又做了镁条与盐溶液反应的实验,发现均能产生H2,实验现象如下:
| 实验序号 | 实验1 | 实验2 | 实验3 | / |
| 镁条反应的溶液 | NH4Cl | NaCl | Na2S04 | H20 |
| 实验现象 | 有大量气泡产生 | 有较多气泡产生 | 有少量气泡产生 | 气泡极少 |
| 加热后实验现象 | 气泡明显增多.可闻到氨味 | 气泡增多 | 气泡增多 | 气泡增多 |
根据上表中的实验现象,请写出三条结论,并分析可能的原因(不分析原因,不得分):
①盐可以做镁与水反应的催化剂,因为盐能加快产生气体的速率;
②温度改变反应速率,因为升高温度可以加快产生气体的速率;
③升高温度能使反应更复杂,因为升高温度使镁与水反应的生成物在与盐反应生成氨气(NH3).
 如图是“×××”补钙剂商品标签图.我能根据标签信息完成下列问题:
如图是“×××”补钙剂商品标签图.我能根据标签信息完成下列问题: