题目内容
9. 广西具有丰富的石灰石资源.化学兴趣小组欲测定某石灰石样品中CaCO3的质量分数,取石灰石样品15g,加入适量稀盐酸(杂质不溶于水,也不与盐酸反应),消耗稀盐酸的质量与放出二氧化碳的质量关系如图所示,请你计算:
广西具有丰富的石灰石资源.化学兴趣小组欲测定某石灰石样品中CaCO3的质量分数,取石灰石样品15g,加入适量稀盐酸(杂质不溶于水,也不与盐酸反应),消耗稀盐酸的质量与放出二氧化碳的质量关系如图所示,请你计算:(1)CaCO3的相对分子质量100
(2)该石灰石样品中CaCO3的质量分数.
分析 根据化学方程式计算的步骤有:一设、二写、三找、四列、五答、六查.在本题中,由图象可知:产生的二氧化碳的质量是4.4g,根据二氧化碳的质量可以求出碳酸钙的质量和生成的氯化钙的质量,然后再求CaCO3的质量分数.
解答 解:(1)CaCO3的相对分子质量:40+12+16×3=100,故答案为:100;
(2)由图象可知:产生的二氧化碳的质量是4.4g,设碳酸钙的质量为x,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 4.4g
$\frac{100}{44}=\frac{x}{4.4g}$
x=10g
石灰石样品中CaCO3的质量分数为:$\frac{10g}{15g}$×100%=66.7%
答:石灰石样品中CaCO3的质量分数66.7%
点评 本考点考查了根据化学方程式的计算和质量守恒定律,属于溶质的质量分数和化学方程式的综合应用.图象型计算题是中考计算题中经常出现的题型.做题时要注意:化学方程式要写正确,始终不要忘记质量守恒定律.本考点主要出现在计算题中.

练习册系列答案
 全程金卷系列答案
全程金卷系列答案 快乐5加2金卷系列答案
快乐5加2金卷系列答案
相关题目
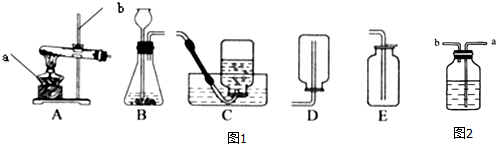
16.下列有关实验现象描述不正确的是( )
| A. |  细铁丝在空气中剧烈燃烧 | B. |  蜡烛逐渐熄灭 | ||
| C. |  铜片有有划痕 | D. |  冷却后粗铜丝b端会上升 |
17.燃烧、爆炸、缓慢氧化的共同之处是( )
| A. | 它们都发生了剧烈的化学反应 | |
| B. | 它们都发生了氧化反应 | |
| C. | 它们都达到了着火点,才能发生反应 | |
| D. | 它们都会产生发光、发热的现象 |
4.下列除去杂质(括号内)的方法正确的是( )
| A. | CO(CO2):通过灼热的氧化铜 | B. | CuO(C):加CO | ||
| C. | CO2(HCl):加入CaCO3) | D. | ZnSO4(FeSO4):加入Zn |