题目内容
1.多少克过氧化氢完全分解产生的氧气与24.5克氯酸钾加热完全分解产生的氧气质量相等.分析 根据过氧化氢受热分解生成水和氧气,氯酸钾分解生成氯化钾和氧气,氯酸钾中的氧元素完全转化成氧气,根据氯酸钾的质量可以计算需要的过氧化氢的质量.
解答 解:设过氧化氢完全分解产生的氧气与24.5克氯酸钾加热完全分解产生的氧气质量相等的质量为x
2KClO3$\frac{\underline{\;MnO_2\;}}{\;}$2KCl+3O2↑,2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,2个氯酸钾会生成3个氧气,2个过氧化氢会生成1个氧气,所以
2KClO3--3O2---6H2O2,
245 204
24.5g x
$\frac{245}{24.5g}$=$\frac{204}{x}$
x=20.4g
故答案为:20.4g.
点评 解答本题的关键是分析出过氧化氢、氯酸钾分解时氧元素的转化关系,这是解答的关键,要注意理解.

练习册系列答案
相关题目
11.鉴别CO和H2的最好方法是( )
| A. | 闻气体的气味 | B. | 点燃观察火焰的颜色 | ||
| C. | 点燃后检验其生成物 | D. | 溶解于水 |
12.下列叙述中正确的是( )
| A. | 二氧化碳分子是由一个碳原子和一个氧分子构成的 | |
| B. | 分子一定比原子大 | |
| C. | 不同元素的原子的核电荷数一定不同 | |
| D. | 核外电子排布相同的粒子一定属于同一种元素 |
16.加热24.5克氯酸钾和含少量二氧化锰的混合物,当质量减少了9.6克时,停止加热、则反应剩余物中含有的是( )
| A. | KClO3、KCl | B. | KCl、KClO3、MnO2 | C. | KCl | D. | KCl、MnO2 |
13.自来水是我国目前主要的生活饮用水,下表是我国颁布的生活饮用水水质标准的部分内容:
(1)感官指标表现的是自来水的物理(填“物理”或“化学”)性质.
(2)自来水中的游离氯有少量可转变为氯离子,氯离子的符号是Cl-.
(3)实验室用自来水制取蒸馏水的方法是D(填序号).
A.吸附 B.沉淀 C.过滤 D.蒸馏.
| 项目 | 标准 |
| 感官指标 | 无异味、异臭等 |
| 化学指标 | pH 6.5-8.5,铜<1.0mg•L-1,铁<0.3mg•L-1, 氟化物<1.0mg•L-1,游离氯≥0.3mg•L-1等 |
(2)自来水中的游离氯有少量可转变为氯离子,氯离子的符号是Cl-.
(3)实验室用自来水制取蒸馏水的方法是D(填序号).
A.吸附 B.沉淀 C.过滤 D.蒸馏.
3.在浓硫酸的催化作用下,固体草酸(H2C2O4)受热分解生成碳的氧化物和水,某化学课外兴趣小组对生成物中碳的氧化物种类进行了如图实验探究:
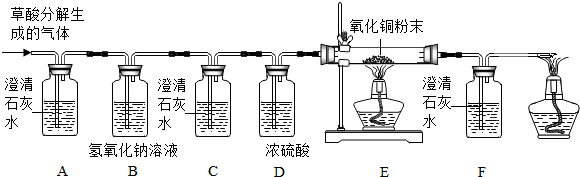
【提出问题】生成物中有哪种碳的氧化物?
【猜测】
【设计实验】基于猜想3,依据CO和CO2的性质,兴趣小组同学设计了如下实验:
【实验探究】
(1)观察到A装置(填序号)中的澄清石灰水变浑浊,证明草酸分解有CO2气体生成.
(2)有两种实验现象都能分别证明草酸分解的气体中含有CO:
①C装置中澄清石灰水不变浑浊,F装置中澄清石灰水变浑浊;
②E装置中出现黑色粉末变红的现象;
【实验结论】通过实验探究证明:猜想3成立.
草酸分解的化学方程式是C2H2O4$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+CO↑+H2O.
【问题讨论】
(1)B装置的作用是除去生成的二氧化碳气体;
(2)装置末端酒精灯的作用是将一氧化碳点燃生成二氧化碳,防止形成空气污染.

【提出问题】生成物中有哪种碳的氧化物?
【猜测】
| 猜想1 | 猜想2 | 猜想3 |
| 只有CO | 只有CO2 | 含有CO和CO2 |
【实验探究】
(1)观察到A装置(填序号)中的澄清石灰水变浑浊,证明草酸分解有CO2气体生成.
(2)有两种实验现象都能分别证明草酸分解的气体中含有CO:
①C装置中澄清石灰水不变浑浊,F装置中澄清石灰水变浑浊;
②E装置中出现黑色粉末变红的现象;
【实验结论】通过实验探究证明:猜想3成立.
草酸分解的化学方程式是C2H2O4$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+CO↑+H2O.
【问题讨论】
(1)B装置的作用是除去生成的二氧化碳气体;
(2)装置末端酒精灯的作用是将一氧化碳点燃生成二氧化碳,防止形成空气污染.

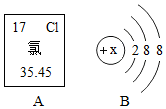 如图中A是氯元素在元素周期表中的相关信息,B是氯离子的结构示意图,分析图中提供的信息,回答问题
如图中A是氯元素在元素周期表中的相关信息,B是氯离子的结构示意图,分析图中提供的信息,回答问题