题目内容
10.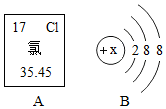 如图中A是氯元素在元素周期表中的相关信息,B是氯离子的结构示意图,分析图中提供的信息,回答问题
如图中A是氯元素在元素周期表中的相关信息,B是氯离子的结构示意图,分析图中提供的信息,回答问题(1)氯元素的相对原子质量为35.45;
(2)图B中X代表的数值为17;
(3)氯离子属于(选填“阴离子”或“阳离子”)阴离子.
分析 根据已有的知识进行分析,离子的质子数=原子序数;根据元素周期表中的一个小格即可得到相对原子质量,据此解答.
解答 解:(1)氯原子的相对原子质量为35.45,故填:35.45;
(2)氯离子的质子数=原子序数;故图B中X代表的数值为17;故填:17;
(2)氯离子的电子数大于质子数,故属于阴离子;故填:阴离子;
点评 本题考查学生根据当核电荷数、质子数与核外电子数的关系辨别微粒种类方法的掌握与应用的能力.

练习册系列答案
相关题目
20.关于CO 的叙述不正确的是( )
| A. | CO 有可燃性和还原性 | |
| B. | CO 可用排水集气法收集 | |
| C. | CO 有毒,能跟血红蛋白结合,使人体缺氧 | |
| D. | CO 可用向上排空气法收集 |
5.对比分析CO和CO2得出下列结论,错误的是( )
| A. | 都属于氧化物 | B. | 组成元素种类相同 | ||
| C. | 化学性质不同 | D. | 构成分子的原子种类不同 |
11.某化学兴趣小组的同学在探究酸碱的化学性质时,做了如下实验.请你一起与小组同学完成下列探究活动:
【学生实验】取一定质量的澄清石灰水,滴加稀盐酸,无明显现象.请写出反应方程式 ①Ca(OH)2+2HCl=CaCl2+2H2O.
【提出问题】反应后溶液中的溶质成分是什么?
【假设猜想】猜想Ⅰ:溶质为CaCl2; 猜想Ⅱ:CaCl2和HCl;
猜想Ⅲ:②CaCl2和Ca(OH)2; 猜想Ⅳ:CaCl2和Ca(OH)2和HCl;
某同学认为以上猜想有一个是不合理的,是猜想 ③Ⅳ(填序号)并说明原因 ④氢氧化钙和稀盐酸不能共存.
【实验探究】用上述反应后的溶液进行如下实验(填写表格中未完成的项目):
【实验结论】通过以上实验探究,得出猜想⑦Ⅱ成立.
【拓展迁移】小组同学反思了酸碱中和反应如果没有明显现象,通常在反应前的溶液中先滴加酸碱指示剂,借助指示剂颜色的变化来判断反应进行的程度.
下列中和反应需要借助指示剂来判断反应发生的是⑧BD(填字母)
A.氢氧化钡溶液和稀硫酸 B.烧碱溶液和稀硫酸
C.氢氧化铁和稀盐酸 D.氢氧化钾溶液和稀盐酸.
【学生实验】取一定质量的澄清石灰水,滴加稀盐酸,无明显现象.请写出反应方程式 ①Ca(OH)2+2HCl=CaCl2+2H2O.
【提出问题】反应后溶液中的溶质成分是什么?
【假设猜想】猜想Ⅰ:溶质为CaCl2; 猜想Ⅱ:CaCl2和HCl;
猜想Ⅲ:②CaCl2和Ca(OH)2; 猜想Ⅳ:CaCl2和Ca(OH)2和HCl;
某同学认为以上猜想有一个是不合理的,是猜想 ③Ⅳ(填序号)并说明原因 ④氢氧化钙和稀盐酸不能共存.
【实验探究】用上述反应后的溶液进行如下实验(填写表格中未完成的项目):
| 实验方案 | 方案一:加锌粒 | 方案二:滴加酚酞溶液 |
| 实验操作 | 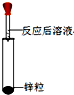 | 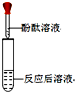 |
| 实验现象 | ⑤产生气泡 | 无明显现象 |
| 实验结论 | 溶液中有HCl | 溶液中无⑥Ca(OH)2 |
【拓展迁移】小组同学反思了酸碱中和反应如果没有明显现象,通常在反应前的溶液中先滴加酸碱指示剂,借助指示剂颜色的变化来判断反应进行的程度.
下列中和反应需要借助指示剂来判断反应发生的是⑧BD(填字母)
A.氢氧化钡溶液和稀硫酸 B.烧碱溶液和稀硫酸
C.氢氧化铁和稀盐酸 D.氢氧化钾溶液和稀盐酸.
12.下列关于水的叙述中错误的是( )
| A. | 冰是由氢元素和氧元素组成的 | |
| B. | 生活中通过煮沸可降低水的硬度 | |
| C. | 净化水的方法通常有吸附、沉淀、过滤 | |
| D. | 生化污水直接排放不会造成水污染 |