题目内容
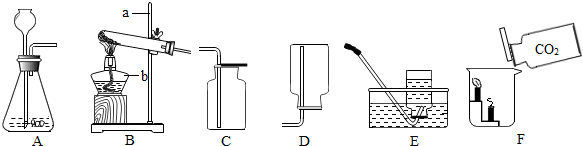
7. 某兴趣小组用如图所示装置制取氧气,试管中固体的质量随时间变化的数据见表.制取结束后,将剩余固体用适量水充分溶解后,过滤,回收二氧化锰固体,并得到氯化钾溶液100g.
某兴趣小组用如图所示装置制取氧气,试管中固体的质量随时间变化的数据见表.制取结束后,将剩余固体用适量水充分溶解后,过滤,回收二氧化锰固体,并得到氯化钾溶液100g.| 加热时间/min | 0 | t1 | t2 | t3 |
| 固体质量/g | 28.0 | 23.2 | 18.4 | 18.4 |
(2)共制得氧气9.6g.
(3)计算所得氯化钾溶液的溶质质量分数.
分析 氯酸钾受热分解生成氯化钾和氧气,反应前后的质量差即为反应生成氧气的质量,根据氧气的质量可以计算氯化钾的质量,进一步可以计算所得氯化钾溶液的溶质质量分数.
解答 解:(1)氧气的相对分子质量=16×2=32;
故填:32;
(2)由表中的数据可知,共制得氧气的质量为:28.0g-18.4g=9.6g;
故填9.6;
(3)设反应生成氯化钾的质量为x
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
149 96
x 9.6g
$\frac{149}{96}=\frac{x}{9.6g}$
x=14.9g
所得氯化钾溶液的溶质质量分数为:$\frac{14.9g}{100g}$×100%=14.9%
答:所得氯化钾溶液的溶质质量分数为14.9%.
点评 本题主要考查学生运用化学方程式进行计算和推断的能力,难度不大,计算时要注意规范性和准确性.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.下列事实的结论或解释错误的是( )
| A. | 酸碱中和反应都能生成水--实质是H +与OH-结合生成H2O | |
| B. | 分离液态空气制氧气--说明分子可以再分 | |
| C. | 气体可压缩储存于钢瓶中--说明分子之间有间隔 | |
| D. | 桂花开放时满园飘香--说明分子在不断运动 |
15.下列关于二氧化碳的说法错误的是( )
| A. | 实验室用大理石与稀硫酸反应制取二氧化碳 | |
| B. | 二氧化碳是引起“温室效应”的主要气体之一 | |
| C. | 大气中的二氧化碳是植物进行光合作用必需的物质 | |
| D. | 将二氧化碳气体通入紫色石蕊试液中,溶液变为红色 |
12.下列各组物质分别加入到足量的水中,能得到无色透明溶液的是( )
| A. | Na2CO3 KCl Ca(OH)2 | B. | FeCl3 Na2SO4 KCl | ||
| C. | CuSO4 H2SO4 KOH | D. | KNO3 NaCl HCl |
19.食品安全日益受到人们关注,下列食品因有毒而不能食用的是( )
| A. | 用含发酵粉(含碳酸氢钠和有机酸等)制作发面食品 | |
| B. | 用水浸过的大米、花生 | |
| C. | 用亚硝酸钠(NaNO2)代替食品烹调食品 | |
| D. | 食盐腌制的咸鸭蛋 |
10.一氧化碳有毒是因为( )
| A. | 它不能供呼吸 | |
| B. | 它具有还原性 | |
| C. | 它具有可燃性 | |
| D. | 它能与血液里的血红蛋白结合,使血红蛋白不能很好地与氧气结合 |