题目内容
8.小娜及学习小组的同学在老师的指导下对黄铜中的铜和锌的含量及性质展开了探究.【查阅资料】
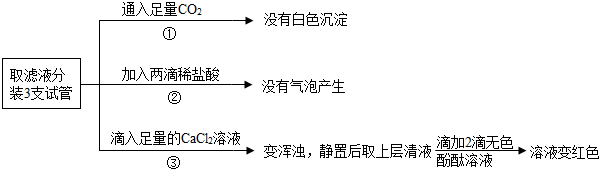
HCl+AgNO3═AgCl↓+HNO3,AgCl 是一种白色沉淀,这个反应在化学上用于检验和鉴别氯离子.
【提出问题】测定黄铜中锌、铜的质量分数.
【实验原理及实验方案设计】(略).
Ⅰ【探究实验】
1、先将黄铜在热碱液中浸泡一段时间,以除去表面的油污,这属于物理变化(填物理变化和化学变化),然后再放在稀盐酸中浸泡片刻以除去表面的氧化物,用蒸馏水清洗干净,干燥,取少量研碎,称取质量为 a g.
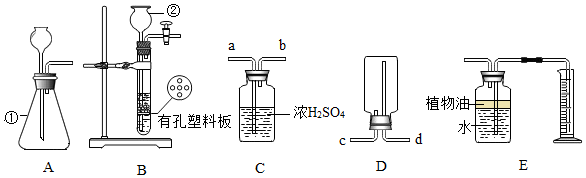
2、将 a g 试样放入小烧杯中,加入足量稀盐酸,搅拌使其充分反应.
3、洗涤、干燥(请将此实验步骤补充完整).
4、计算出黄铜中锌和铜的质量分数.
Ⅱ【反思与评价】在步骤 1 中,若试样用蒸馏水洗涤之后,不干燥,则计算出合金中锌的质量分数将偏大(填“偏大”、“偏小”或“不受影响”)
Ⅲ【拓展探究】
1、重复【探究实验】步骤 1.
2、将 a g 试样放入一定量的硝酸银溶液中,使其充分反应后过滤,得到固体和蓝色滤液,并对滤液的组成进行探究.
(1)锌和硝酸盐溶液反应的化学方程式是Zn+2AgN03=Zn(N03)2+2Ag.
(2)同学们对蓝色滤液中所含的溶质做出多种猜想,其中只有两种猜想可能成立,这两种猜想是:
①溶质为硝酸锌和硝酸铜;②溶质为硝酸锌、硝酸铜和硝酸银.
(3)设计一种实验方案来验证以上猜想取少量滤液于试管中,在滤液中插入一根铜丝,如果铜丝表面无变化,说明了溶液中无硝酸银,则猜想①成立;如果铜丝表面有银白色固体析出,说明了溶液中有硝酸银,则猜想②成立.
分析 【探究实验】①(1)根据金属易于空气中的氧气反应,在金属的表面形成一层氧化膜进行分析;
③根据从溶液中过滤出的物质的表面一般沾有溶液进行分析;
【反思与评价】根据在步骤1中,若试样用蒸馏水洗涤之后,不干燥,则使称量的混合物的质量增加,如果减去铜的质量后,锌的质量增大,最后分析对计算出合金中锌的质量分数的影响.
【拓展探究】②(1)根据锌和硝酸盐溶液反应写出反应的方程式;
(2)根据锌、铜与硝酸银溶液的反应进行分析;
(3)根据稀盐酸(或其他氯化物溶液)与硝酸银的反应分析溶液中的溶质.
解答 解:
HCl+AgNO3═AgCl↓+HNO3,AgCl 是一种白色沉淀,这个反应在化学上用于检验和鉴别氯离子;
【探究实验】
①将黄铜在热碱液中浸泡一段时间,以除去表面的油污,这属于物理变化;由于金属易于空气中的氧气反应,在金属的表面形成一层氧化膜,所以,将黄铜在放在稀盐酸中浸泡片刻,其目的是除去合金表面的氧化膜;
③由于从溶液中过滤出的物质的表面一般沾有溶液,所以,将过滤出的物质需要进行洗涤、干燥;
【反思与评价】
在步骤1中,若试样用蒸馏水洗涤之后,不干燥,称量的a值偏大,求出锌的质量偏大,则计算出合金中锌的质量分数将偏大;
【拓展探究】②(1)锌和硝酸盐溶液反应写出反应的方程式是:Zn+2AgN03=Zn(N03)2+2Ag.
(2)将黄铜放入一定量的硝酸银溶液中,锌先与硝酸银反应,当锌反应完后,铜再与硝酸银反应.当锌的量不足时,溶液中的溶质可能有:硝酸锌和硝酸铜或硝酸锌、硝酸铜和硝酸银;
(3)方案一:取少量滤液于试管中,在滤液中插入一根铜丝,如果铜丝表面无变化,说明了溶液中无硝酸银,则猜想①成立;如果铜丝表面有银白色固体析出,说明了溶液中有硝酸银,则猜想②成立;
方案二:可以根据稀盐酸(或其他氯化物溶液)与硝酸银的反应鉴别溶液中是否含有硝酸银,所以,取少量滤液于试管中,滴加几滴稀盐酸,如果滤液无明显变化,说明了溶液中无硝酸银,则猜想①成立;如果生成白色沉淀,说明了溶液中有硝酸银,则猜想②成立.
故答为:氯离子;
【探究实验】①物理变化;③洗涤、干燥;
【反思与评价】偏大;
【拓展探究】②(1)Zn+2AgN03=Zn(N03)2+2Ag,(2)②硝酸锌、硝酸铜和硝酸银;
(3)取少量滤液于试管中,在滤液中插入一根铜丝,如果铜丝表面无变化,说明了溶液中无硝酸银,则猜想①成立;如果铜丝表面有银白色固体析出,说明了溶液中有硝酸银,则猜想②成立;
点评 在解此类题时,首先要会根据物质质量的多少进行正确的猜想,然后根据各种物质的性质选择有特征的实验选择试剂进行验证.

 期末集结号系列答案
期末集结号系列答案【提出问题】如何利用石灰石与稀盐酸反应来测定生成CO2的质量和体积,并处理数据.
【实验设计】通过下列两个实验分别测定CO2的质量和体积:
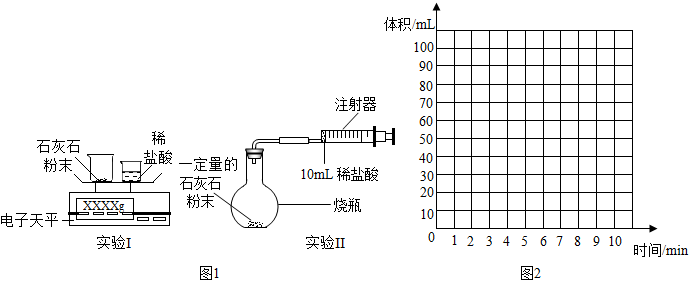
【分析与表达】
(1)上述两个实验中,反应的化学方程式为CaCO3+2HCl═CaCl2+CO2↑+H2O.
(2)实验Ⅰ中,将小烧杯中的所有稀盐酸分几次加入到大烧杯中,并不断搅拌,判断石灰石中CaCO3完全反应的实验现象是最后一次加入稀盐酸,仍没有气泡产生.
(3)实验Ⅱ中,先连接好装置,在检查装置的气密性(请简述方法将注射器往右拉,松开时活塞回到之前的刻度,则气密性良好),然后装好药品,最后将10mL稀盐酸快速推入烧杯中,若稀盐酸是缓慢推入的,则可能造成的后果是烧瓶内气压增大,稀盐酸难以完全推入烧瓶中或仪器连接处脱落.
【记录与处理】
(4)已知实验Ⅰ反应前的总质量【m(大烧杯+石灰石粉末)+m(小烧杯+稀盐酸)】,要计算生成CO2的质量,至少还需要的数据是AC
A.m(小烧杯) B.m(大烧杯) C.m(大烧杯+反应后剩余物)
(5)实验Ⅱ的实验记录如下(表中数据在相同温度、相同压强条件下测定)
| 时间/min | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 注射器读数/ml | 60.0 | 85.0 | 88.0 | 89.0 | 89.5 | 89.8 | 89.9 | 90.0 | 90.0 | 90.0 |
注意:若答对下面题奖励4分,但化学总分不超过60分.
(6)根据你的认识,在图2中坐标图中绘制出0~10min生成CO2体积随时间变化的曲线.
【反思与评价】
(7)经过分析,你认为实验Ⅰ的优点是巧妙利用质量守恒定律测出气体的质量,实验Ⅱ的优点是用十分简单的装置,利用前后气体体积差测得二氧化碳的体积.
| A. | 11.43 | B. | 22.85 | C. | 80.01 | D. | 160.02 |
| A. | 都是带电荷的粒子 | B. | 都是保持物质化学性质的最小粒子 | ||
| C. | 都是化学变化中的最小粒子 | D. | 都是构成物质的基本粒子 |