题目内容
18.同学们已经学过实验室制取气体的一般思路和方法,请利用下列装置回答相关问题.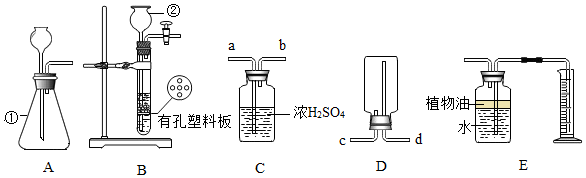
(1)写出有标号仪器的名称:①锥形瓶,②长颈漏斗
(2)实验室制取CO2的化学反应方程式CaCO3+2HCl═CaCl2+H2O+CO2↑,若要控制反应的发生和停止,选用的发生装置是B.
(3)浓H2SO4具有强烈的吸水性,可作为干燥剂除去某些气体中的水份,如用装置C干燥CO2,则CO2应从a(填字母)端口通入.
(4)如用装置D收集CO2,则CO2应从c(填字母)端口通入,如何检验CO2是否收集满?把燃着的木条放在导管d端,若木条熄灭,则已集满
(5)装置E用于通入CO2将水压入量筒中以测量CO2的体积,植物油的作用是防止二氧化碳溶于水.
分析 (1)熟记仪器的名称;
(2)根据实验室制取二氧化碳的原理以及装置的特点来分析;
(3)干燥气体时,导管一般遵循长进短出的原则;
(4)二氧化碳的密度比空气大;
(5)二氧化碳能够溶于水.
解答 解:(1)①是锥形瓶,②是长颈漏斗;故填:锥形瓶;长颈漏斗;
(2)实验室选用石灰石与稀盐酸反应制取二氧化碳的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑,装置B关闭活塞,则气体无法导出,在试管内聚集,压强变大,使液体沿着长颈漏斗上升,与固体分离,反应停止;故填:CaCO3+2HCl═CaCl2+H2O+CO2↑;B;
(3)如用装置C干燥CO2,则CO2应从a端口通入.故填:a.
(4)如用装置D收集CO2,由于二氧化碳的密度比空气大,则CO2应从c端口通入,验满时,把燃着的木条放在导管d端,若木条熄灭,则已集满.故填:c;把燃着的木条放在导管d端,若木条熄灭,则已集满;
(5)装置E用于通入CO2将水压入量筒中以测量CO2的体积,植物油的作用是防止二氧化碳溶于水,从而使实验结果更精确.
故填:防止二氧化碳溶于水.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
9.“见著知微”是化学学科的重要特点之一.它是指通过实验现象的观察、思考和推论.建立起对微小的原子、分子的认识.下列不符合这一特点的是( )
| A. |  蔗糖溶解 | B. |  电解水实验 | ||
| C. |  测定空气里氧气含量 | D. |  A烧杯中溶液变红 |
6.丙氨酸(化学式C3H7O2N)具有预防肾结石、协助葡萄糖的代谢,有助缓和低血糖,改善身体能量的功效.下列关于丙氨酸说法正确的是( )
| A. | 一个丙氨酸分子中共含有13个原子 | |
| B. | 丙氨酸中氢元素的质量分数最大 | |
| C. | 一个丙氨酸分子中含有一个氧分子 | |
| D. | 丙氨酸中C、H、O、N三种原子的质量比为3:7:2:1 |
7.①大米②小麦③玉米④土豆⑤白菜⑥脐橙是常见的食品.这些物质中富含淀粉的是( )
| A. | ①②③④ | B. | ②③④⑤ | C. | ①②④⑥ | D. | ①③⑤⑥ |
8.下列图象分别与选项中的操作相对应,其中不合理的是( )
| A. |  一定量的木炭在空气中完全燃烧 | B. |  在密闭容器中加热氧化汞 | ||
| C. |  加热两份质量相等的氯酸钾 | D. |  电解水产生的氢气和氧气的体积 |