题目内容
3.关于下列四个图象的说法中正确的是( )| A. | 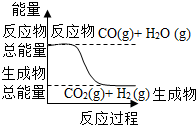 如图表示可逆反应“CO(g)+H2O(g)?CO2(g)+H2(g)”中的△H大于0 | |
| B. | 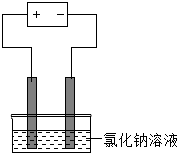 如图是在电解氯化钠稀溶液的电解池中,阴、阳极产生气体体积之比一定为1:1 | |
| C. | 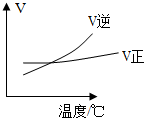 如图可表示可逆反应“A2(g)+3B2(g)?2AB3(g)”的△H小于0 | |
| D. | 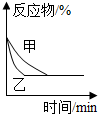 如图可表示压强对可逆反应2A(g)+2B(g)?3C(g)+D(s)的影响,乙的压强大 |
分析 A、根据反应物总能量和生成物总能量的相对大小来判断该反应是吸热还是放热反应;
B、根据氯气在水中的溶解度比氢气大进行分析;
C、根据升高温度,逆反应速率大于正反应速率,平衡向着逆方向进行;
D、根据先到达平衡的反应,压强大,再根据平衡移动原理,判断平衡是否移动进行分析.
解答 解:A、反应物总能量大于生成物总能量,反应放热,△H小于0,故A错误;
B、电解氯化钠溶液,阳极生成氯气,阴极生成氢气,氯气在水中的溶解度比氢气大,所以阴、阳极产生气体体积之比一定大于1:1,故B错误;
C、升高温度,逆反应速率大于正反应速率,平衡向着逆方向进行,说明反应放热,△H小于0,故C正确;
D、乙显到达平衡,所以乙的压强大,甲的压强小,增大压强,平衡向正反应方向移动,而图中的平衡没有移动,乙应该是加入催化剂的原因,故D错误.
故选:C.
点评 本题主要考查了化学反应是吸热还是放热,氯气与氢气溶解度大小的比较,温度和压强对化学反应速率和平衡的影响.

练习册系列答案
相关题目
18.已知CaCO3+H2O+CO2=Ca(HCO3)2,Ca(HCO3)2可溶于水.下列图象不能正确反映其对应变化关系的是
( )
( )
| A. | 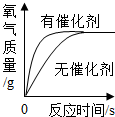 用等质量、等浓度的过氧化氢溶液在有无催化剂条件下制氧气 用等质量、等浓度的过氧化氢溶液在有无催化剂条件下制氧气 | |
| B. | 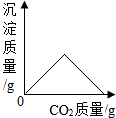 表示澄清石灰水中持续通入CO2 表示澄清石灰水中持续通入CO2 | |
| C. | 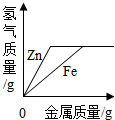 向等质量、等浓度的稀硫酸中分别逐渐加入锌粉和铁粉 向等质量、等浓度的稀硫酸中分别逐渐加入锌粉和铁粉 | |
| D. | 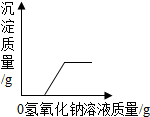 向一定质量的氯化铜和稀盐酸的混合溶液中逐滴加入氢氧化钠溶液 向一定质量的氯化铜和稀盐酸的混合溶液中逐滴加入氢氧化钠溶液 |
8.“84”消毒液的主要成分是次氯酸钠,是烧碱溶液与物质X反应得到的,反应方程式如下:
2NaOH+X═NaClO+NaCl+H2O 则X的化学式是( )
2NaOH+X═NaClO+NaCl+H2O 则X的化学式是( )
| A. | HCl | B. | Cl2 | C. | ClO2 | D. | HClO |
12.下列关于生活和健康常识的说法不正确的是( )
| A. | 用碳酸氢钠焙制糕点 | |
| B. | 饮用牛奶和豆浆可以缓解重金属引起的中毒 | |
| C. | 医疗上用酒精杀菌消毒 | |
| D. | 用甲醛溶液对水产品保鲜 |
 “低碳生活,绿色出行”.下图为潍坊公共自行车.请回答下列问题:
“低碳生活,绿色出行”.下图为潍坊公共自行车.请回答下列问题: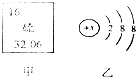 (4分) 图甲是某元素在元素周期表中的部分信息,图乙是该元素的一种粒子结构示意图.
(4分) 图甲是某元素在元素周期表中的部分信息,图乙是该元素的一种粒子结构示意图.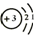 则锂离子的符号为Li+.
则锂离子的符号为Li+.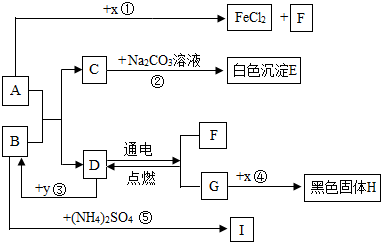
 如图是配制好的盐酸溶液的标签,请根据标签上的文字信息,进行计算:某纯碱样品中含有少量氯化钠.为测定样品中碳酸钠的质量分数,现称取该样品11.0g,放入烧杯中加水完全溶解后滴加上述配制的盐酸溶液至完全反应,最后测得生成气体的质量为4.4g,计算:
如图是配制好的盐酸溶液的标签,请根据标签上的文字信息,进行计算:某纯碱样品中含有少量氯化钠.为测定样品中碳酸钠的质量分数,现称取该样品11.0g,放入烧杯中加水完全溶解后滴加上述配制的盐酸溶液至完全反应,最后测得生成气体的质量为4.4g,计算: