题目内容
13.(1)请用化学用语填空:①氩气的化学式Ar②氯化铁中的阳离子Fe3+③水溶液呈碱性的气体是NH3
④在化学反应N2O+2KNH2=KN3+KOH+X中,“X”的化学式是NH3,N2O中N的化合价为+1.
⑤用来改良酸性土壤的碱是Ca(OH)2.
(2)①锅里的油一旦着火,可立即盖上锅盖,其原理是隔绝氧气.
②治疗胃酸过多症的化学反应方程式Al(OH)3+3HCl=AlCl3+3H2O(写出一个即可).
分析 (1)①根据氩气是单原子分子进行分析;
②根据氯化铁溶液的阳离子是铁离子,然后依据离子的正确书写进行分析;
③根据氨气的水溶液形成氨水,氨水显碱性进行分析;
④根据质量守恒定律和化合价代数和为零进行分析;
⑤根据用来改良酸性土壤的碱是氢氧化钙进行分析;
(2)①根据灭火的原理进行分析;
②根据氢氧化铝和盐酸反应生成氯化铝和水进行分析.
解答 解:(1)①氩气是单原子分子,表示为:Ar;
②氯化铁溶液的阳离子是铁离子,离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略,所以铁离子表示为:Fe3+;
③氨气的水溶液形成氨水,氨水显碱性,所以水溶液呈碱性的气体是NH3;
④化学反应前后原子个数不变,反应物中有4个氮原子,1个氧原子,2个钾原子,4个氢原子,生成物质有2个钾原子,3个氮原子,1个氢原子,1个氧原子,所以X是NH3,设氮元素的化合价为x,所以2x+(-2)=0,x=+1;
⑤用来改良酸性土壤的碱是氢氧化钙,化学式为:Ca(OH)2;
(2)①锅里的油一旦着火,可立即盖上锅盖,其原理是:隔绝氧气;
②氢氧化铝和盐酸反应生成氯化铝和水,化学方程式为:Al(OH)3+3HCl=AlCl3+3H2O.
故答案为:(1)①Ar;
②Fe3+;
③NH3;
④NH3,+1;
⑤Ca(OH)2;
(2)①:隔绝氧气;
②Al(OH)3+3HCl=AlCl3+3H2O.
点评 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础,题目难度较易.

练习册系列答案
相关题目
3.关于下列四个图象的说法中正确的是( )
| A. | 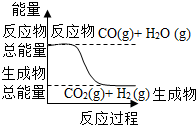 如图表示可逆反应“CO(g)+H2O(g)?CO2(g)+H2(g)”中的△H大于0 | |
| B. | 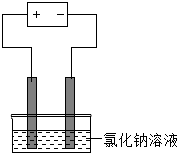 如图是在电解氯化钠稀溶液的电解池中,阴、阳极产生气体体积之比一定为1:1 | |
| C. | 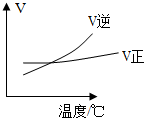 如图可表示可逆反应“A2(g)+3B2(g)?2AB3(g)”的△H小于0 | |
| D. | 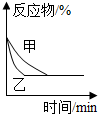 如图可表示压强对可逆反应2A(g)+2B(g)?3C(g)+D(s)的影响,乙的压强大 |
4.下列现象能用物理变化解释的是( )
| A. | 水壶烧水出现水垢 | B. | 冬季室内窗户玻璃出现水雾 | ||
| C. | 牛奶变酸 | D. | 石墨在一定条件下转化为金刚石 |
1.在一个密闭容器内有如下反应,反应前后测得各物质的质量如下表所示,试回答:
①该反应的反应物是M.
②待测值为16.
③反应生成的P和Q的质量比为3:2.
| 物质 | M | N | P | Q |
| 反应前的质量/g | 40 | 4 | 3.6 | 4.8 |
| 反应后的质量/g | 待测 | 13 | 12.6 | 10.8 |
②待测值为16.
③反应生成的P和Q的质量比为3:2.
8.在一定条件下,锌与稀硝酸可发生反应:4Zn+10HNO3=4Zn(NO3)2+□X+N2O↑,其中X为一种常见物质.关于物质X,下列说法正确的是( )
| A. | X的化学式为H2O2 | B. | X前面的计量系数为5 | ||
| C. | X中两种元素的质量比为1:16 | D. | X中元素化合价为零 |
18.王强同学进实验室取45ml稀盐酸,他选择50ml的量筒,读数时,他仰视读数,那么王强量出的实际液体体积是( )
| A. | 等于45ml | B. | 大于45ml | ||
| C. | 小于45ml | D. | 可能大于45ml,也可能小于45ml |
5. 根据如图的溶解度曲线,判断下列说法不正确的( )
根据如图的溶解度曲线,判断下列说法不正确的( )
 根据如图的溶解度曲线,判断下列说法不正确的( )
根据如图的溶解度曲线,判断下列说法不正确的( )| A. | 20℃时,将20克甲、乙两种物质分别加入到50g水中都能得到饱和溶液 | |
| B. | 甲物质中含有少量乙物质可以采用降温结晶方法提纯 | |
| C. | 10℃时,甲、乙两物质的饱和溶液中含溶质的质量相等 | |
| D. | 10℃时,甲、乙两物质的饱和溶液中溶质质量分数相等 |
2.如图是几种粒子的结构示意图,下面几种说法正确的是( )


| A. | 所有结构示意图均是原子结构示意图,且②和③在元素周期表中在同一列 | |
| B. | 只有④具有稳定结构,②和④的化学性质相似 | |
| C. | 其中③④属于同种元素的不同粒子 | |
| D. | ①和④能形成AB3型化合物 |
2.利用下列原理制取氧气,具有反应快、操作简便、能耗少、无污染的是( )
| A. | 氯酸钾$→_{加热}^{二氧化锰}$氯化钾+氧气 | |
| B. | 高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气 | |
| C. | 过氧化氢$\stackrel{二氧化锰}{→}$水+氧气 | |
| D. | 氧化汞$\stackrel{加热}{→}$汞+氧气 |