题目内容
18.浓硫酸与Cu加热时能发生反应:Cu+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O(1)将铜片换成铜粉反应速率将加快,原因是增大了铜与浓硫酸的接触面积.
(2)用Cu制CuSO4有两种方案:
方案一:Cu与浓H2SO4加热 Cu+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O
方案二:将空气通入加有Cu的稀H2SO4中加热 2Cu+O2+2H2SO4(稀)$\frac{\underline{\;\;△\;\;}}{\;}$2CuSO4+2H2O
选择方案二较好,理由是不产生污染物、硫酸利用率高.
(3)有元素化合价升降的反应是氧化还原反应,所含元素化合价降低的反应物是氧化剂,所含元素化合价升高的反应物是还原剂,则下列反应中属于氧化还原反应的是①②,H2SO4作氧化剂的是①②.
①Zn+H2SO4(稀)=═ZnSO4+H2↑
②Zn+2H2SO4(浓)═ZnSO4+SO2↑+2H2O
③2Cu+O2+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$2CuSO4+2H2O
④FeO+H2SO4=FeSO4+H2O.
分析 (1)根据将铜片换成铜粉,增大了铜与浓硫酸的接触面积进行解答;
(2)根据方案一中会生成二氧化硫,二氧化硫会污染空气进行解答;
(3)根据有元素化合价升降的反应是氧化还原反应,所含元素化合价降低的反应物是氧化剂进行解答.
解答 解:(1)将铜片换成铜粉,增大了铜与浓硫酸的接触面积,所以将铜片换成铜粉反应速率将加快;故填:增大了铜与浓硫酸的接触面积;
(2)当制取相同质量的硫酸铜时,方案一消耗掉的硫酸比方案二多一倍;方案一制取过程中产生了污染大气的有毒气体SO2,而方案二不产生污染物.
故填:二;不产生污染物、硫酸利用率高;
(3)①Zn+H2SO4(稀)═ZnSO4+H2↑中锌的化合价由0价变为+2价,而氢元素的化合价由+1价变为0价,所以属于氧化还原反应,其中硫酸是氧化剂;
②Zn+2H2SO4(浓)═ZnSO4+SO2↑+2H2O锌的化合价由0价变为+2价,而硫元素的化合价由+6价变为+4价,所以属于氧化还原反应,其中硫酸是氧化剂;
③2Cu+O2+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$2CuSO4+2H2O中没有元素化合价升降的反应是氧化还原反应,不属于氧化反应反应;
④FeO+H2SO4=FeSO4+H2O中没有元素化合价升降的反应是氧化还原反应,不属于氧化反应反应.
故答案为:①②;①②.
点评 本题难度不是很大,实验设计的评价要注意从实验本身去分析,要注意从实验方案的科学性、可行性上进行分析解答

练习册系列答案
相关题目
8. 实验室里,用如图所示装置还原氧化铁的过程中,可能生成四氧化三铁、氧化亚铁或铁等固体物质.关于该实验,下列说法错误的是( )
实验室里,用如图所示装置还原氧化铁的过程中,可能生成四氧化三铁、氧化亚铁或铁等固体物质.关于该实验,下列说法错误的是( )
 实验室里,用如图所示装置还原氧化铁的过程中,可能生成四氧化三铁、氧化亚铁或铁等固体物质.关于该实验,下列说法错误的是( )
实验室里,用如图所示装置还原氧化铁的过程中,可能生成四氧化三铁、氧化亚铁或铁等固体物质.关于该实验,下列说法错误的是( )| A. | 实验时,试管中澄清的石灰水变浑浊,证明该反应有二氧化碳生成 | |
| B. | 实验结束时,玻璃管中红棕色的氧化铁粉末变成黑色,该产物不一定是铁 | |
| C. | 反应后,玻璃管中的固体物质的质量比反应前减少了,证明一定有铁生成 | |
| D. | 为了减少空气污染,应增加尾气处理装置 |
9.市场上有一种加酶洗衣粉,衣物的汗渍,血迹及人体排放的蛋白质油渍遇到它,皆能水解而除去,下列衣料①羊毛织品②棉织品③锦纶布料④蚕丝制品,不能用加酶洗衣粉洗涤的是( )
| A. | ①② | B. | ③④ | C. | ②③ | D. | ①④ |
6. 甲、乙、丙三种固体物质的溶解度曲线如图所示.下列说法,正确的是( )
甲、乙、丙三种固体物质的溶解度曲线如图所示.下列说法,正确的是( )
 甲、乙、丙三种固体物质的溶解度曲线如图所示.下列说法,正确的是( )
甲、乙、丙三种固体物质的溶解度曲线如图所示.下列说法,正确的是( )| A. | 25℃时,将20g甲固体加入到50g水中,充分溶解并恢复到原温度可形成70 g溶液 | |
| B. | 35℃时丙的饱和溶液降温到25℃,则其溶液的溶质质量分数不变 | |
| C. | 甲是三种物质中溶解度最大的 | |
| D. | 35℃时,甲物质饱和溶液的溶质质量分数为40% |
13. 如图是物质A、B、C的溶解度曲线,下列相关说法正确的是( )
如图是物质A、B、C的溶解度曲线,下列相关说法正确的是( )
 如图是物质A、B、C的溶解度曲线,下列相关说法正确的是( )
如图是物质A、B、C的溶解度曲线,下列相关说法正确的是( )| A. | 若要将B从溶液中结晶出来常采用的方法是降温结晶 | |
| B. | 将T2℃时A、B、C的饱和溶液冷却到T1℃,所得的三种溶液中A溶液的质量分数最小 | |
| C. | 若要将组成在M点的A溶液转变为N点的溶液,只能采取恒温蒸发溶剂的方法 | |
| D. | 将T2℃时组成相当于在M点的C 与水的混合物降温到T1℃,可得到C的不饱和溶液 |
3. 如图是物质A、B、C的溶解度曲线,下列相关说法正确的是( )
如图是物质A、B、C的溶解度曲线,下列相关说法正确的是( )
 如图是物质A、B、C的溶解度曲线,下列相关说法正确的是( )
如图是物质A、B、C的溶解度曲线,下列相关说法正确的是( )| A. | 若要将A从溶液中结晶出来常采用的方法是蒸发溶剂 | |
| B. | 将T2℃时A、B、C的饱和溶液冷却到T1℃,所得的三种溶液中A溶液的质量分数最小 | |
| C. | 若要将组成在M点的A溶液转变为N点的溶液,只能采取恒温蒸发溶剂的方法 | |
| D. | 将T1℃时A、B、C三种物质的饱和溶液升温到T2℃,此时三物质的溶质质量分数由大到小的顺序是B>A>C |
4.下列说法中不正确的是( )
| A. | 农业上可采用喷灌、滴灌来节水 | B. | 用肥皂水可以区分硬水和软水 | ||
| C. | 家中天然气泄漏赶紧打开排风扇 | D. | 在钢铁表面涂油可以防止生锈 |
 甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答:
甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答:
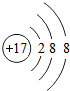 表示的是(填名称)氯离子;
表示的是(填名称)氯离子;