题目内容
7.元素周期律是学习和研究化学的重要工具.如表是元素周期表的部分信息:
认真分析信息,回答:
(1)地壳中含量最多的金属元素的符号是Al;
(2)
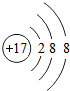 表示的是(填名称)氯离子;
表示的是(填名称)氯离子;(3)由1、8、12号元素组成化合物的化学式Mg(OH)2.
(4)上表中每一周期元素原子序数的变化规律是从左到右依次增大.
分析 (1)根据地壳中各元素含量的排序及元素的分类、元素符号的书写方法进行分析解答即可.
(2)根据微粒结构来分析;
(3)首先确定元素名称,再来书写化学式;
(4)根据元素周期表中每周期的元素的原子序数变化找到规律即可.
解答 解:(1)地壳含量较多的元素(前四种)按含量从高到低的排序为:氧、硅、铝、铁,其中含量最多的金属元素是铝元素,其元素符号为:Al.故答案为:Al.
(2)该微粒核内有17个质子,属于氯元素,核外电子数为18,带一个单位的负电荷,是氯离子,故填:氯离子;
(3)1号元素是氢元素,8号元素是氧元素,12号元素是镁元素,组成的化合物为氢氧化镁,故填:Mg(OH)2;
(4)将每一周期的元素的原子序数对比可知,由左向右原子序数依次增大.故填:从左到右依次增大.
点评 本题难度不大,考查学生灵活运用元素周期表中元素的信息、化学式的书写等进行分析解题的能力.

练习册系列答案
相关题目
2.某实验小组的同学用碳酸钠粉末、粒状大理石、稀盐酸、浓盐酸、稀硫酸这几种药品,探究哪两种药品的反应适合在实验室制取CO2.请你参与下列的探究并回答问题.
【提出问题】上述人酸和碳酸盐的反应是否适合在实验室制取CO2?
【方案设计】大家经过讨论,一致认为浓盐酸不适合用于实验室制取CO2,你认为原因浓盐酸易挥发,使制出的CO2不纯.讨论后大家设计了如下三个实验进行对比分析.如图1

【实验与结论】(1)请你填写实验报告中①、②处的内容.
(2)根据探究结论,实验室制取二氧化碳的反应原理为CaCO3+2HCl═CaCl2+H2O+CO2↑ ( 用化学方程式表示).
【拓展与迁移】
(1)由上述探究可知,在确定实验室制取气体的反应原理时,要考虑诸多因素,例如反应速率要适中,便于收集等.请你再写出一种需要考虑的因素:制出的气体要纯净.
(2)图2是一种灭火器的工作原理示意图,其中用碳酸钠和浓盐酸反应来产生CO2的理由是能够迅速产生大量CO2.
【提出问题】上述人酸和碳酸盐的反应是否适合在实验室制取CO2?
【方案设计】大家经过讨论,一致认为浓盐酸不适合用于实验室制取CO2,你认为原因浓盐酸易挥发,使制出的CO2不纯.讨论后大家设计了如下三个实验进行对比分析.如图1

【实验与结论】(1)请你填写实验报告中①、②处的内容.
| 实验 | 实验现象 | 实验内容 |
| A | 剧烈反应,迅速放出大量气泡 | 反应速率过快,气体不便收集,不宜于实验室制取二氧化碳 |
| B | 产生气泡,速率迅速减慢,反应几乎停止. | 无法持续产生CO2,不能用于实验室制取CO2 |
| C | ①产生大量气泡 | ②反应速率适中,气体便于收集 |
【拓展与迁移】
(1)由上述探究可知,在确定实验室制取气体的反应原理时,要考虑诸多因素,例如反应速率要适中,便于收集等.请你再写出一种需要考虑的因素:制出的气体要纯净.
(2)图2是一种灭火器的工作原理示意图,其中用碳酸钠和浓盐酸反应来产生CO2的理由是能够迅速产生大量CO2.
12. 每年的4月22日是“世界地球日”,旨在唤起人类爱护地球、保护家园的意识,下列做法不符合“低碳生活”理念的是( )
每年的4月22日是“世界地球日”,旨在唤起人类爱护地球、保护家园的意识,下列做法不符合“低碳生活”理念的是( )
 每年的4月22日是“世界地球日”,旨在唤起人类爱护地球、保护家园的意识,下列做法不符合“低碳生活”理念的是( )
每年的4月22日是“世界地球日”,旨在唤起人类爱护地球、保护家园的意识,下列做法不符合“低碳生活”理念的是( )| A. | 节约用电 | B. | 焚烧落叶 | C. | 骑自行车出行 | D. | 使用太阳能路灯 |
16.下列实验设计能实现其对应的实验目的是( )
| A. |  测定空气中O2的含量 | B. |  能证明CO2与NaOH反应 | ||
| C. |  比较铜盐与亚铁盐的催化效果 | D. |  此装置具有“启普发生器”的功能 |
13.“绿色化学”能实现零排放(即反应物中的原子利用率达到100%).CO和H2在一定条件下按照不同的比例可以合成不同的化工原料.根据零排放的要求,以CO和H2合成的下列物质中,符合要求的是( )
| A. | 乙醇(C2H6O) | B. | 丙酸(C3H6O2) | C. | 乙醛(C2H4O) | D. | 甲醇(CH4O) |
 2011年3月我国云南与日本相继发生地震,特别是日本的地震震级达到9级,并且引发了一场核危机,日本福岛的多个核电机组发生爆炸.请根据所学知识回答下列问题.
2011年3月我国云南与日本相继发生地震,特别是日本的地震震级达到9级,并且引发了一场核危机,日本福岛的多个核电机组发生爆炸.请根据所学知识回答下列问题.