题目内容
5.如图是有关物质转化关系的示意图,其中A是含有碳元素的化合物,D是一种含有钠元素的化合物.请回答下列问题: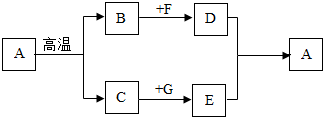
(1)写出下列物质的化学式:
A:CaCO3;D:Na2CO3;G:H2O
(2)写出B转化为D的反应方程式CO2+2NaOH=Na2CO3+H2O,
(3)写出D和E反应的化学方程式Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
分析 本题为框图型物质推断题,完成此题,关键是找准解题突破口,直接得出有关物质的化学式,再推导得出其他物质的化学式,A是含有碳元素的化合物,高温能分解为B和C,则A可能为碳酸钙,分解的B和C可能为氧化钙或二氧化碳,D是一种含有钠元素的化合物,则D可能为碳酸钠,B可能为二氧化碳,F可能为氢氧化钠,C可能为氧化钙,G可能为水,氧化钙与水生成的E为氢氧化钙,代入框图,推断合理.
解答 解:(1)A是含有碳元素的化合物,高温能分解为B和C,则A可能为碳酸钙,分解的B和C可能为氧化钙或二氧化碳,D是一种含有钠元素的化合物,则D可能为碳酸钠,B可能为二氧化碳,F可能为氢氧化钠,C可能为氧化钙,G可能为水,氧化钙与水生成的E为氢氧化钙,所以本题答案为:CaCO3,Na2CO3,H2O;
(2)B是二氧化碳,二氧化碳和氢氧化钠反应产生碳酸钠和水,所以本题答案为:CO2+2NaOH=Na2CO3+H2O;
(3)根据推断,D为碳酸钠,E为氢氧化钙,碳酸钠能与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,所以本题答案为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
点评 本题为框图型物质推断题,完成此类题目,关键是根据框图以及题干提供的信息,找准解题的突破口,直接得出有关物质的化学式,然后顺推或逆推或由两边向中间推,得出其他物质的化学式.

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
15.关于空气的说法正确的是( )
| A. | 空气是由空气分子构成的 | |
| B. | 按质量计算,空气中的氮气约占78%、氧气约占21% | |
| C. | 分离液态空气法制氧气属于分解反应 | |
| D. | 空气是由氮气、氧气等组成的混合物 |
16.推理和归纳是化学学习和研究中常用的思维方法,下列推理正确的是( )
| A. | 碱的溶液能使酚酞溶液变红色,则能使酚酞溶液变红色的一定是碱的溶液 | |
| B. | 单质是由一种元素组成的物质,由一种元素组成的物质一定是单质 | |
| C. | 性质活泼的金属在空气中由容易被腐蚀,铝在空气中不易被腐蚀是因为其性质不活泼 | |
| D. | 酸能跟碱反应生成盐和水,能跟碱反应生成盐和水的物质不一定是酸 |
13.现有生石灰和碳酸钙的固体混合物8.9g,高温煅烧一段时间剩余固体7.8g,向剩余固体中加入溶质质量分数7.3%的稀盐酸至恰好不再冒气泡,共用去稀盐酸100g,若7.8g剩余固体煅烧至完全反应生成二氧化碳的质量为( )
| A. | 2.2g | B. | 4.4g | C. | 3.3g | D. | 6.6g |
20.小明同学进行了如下的实验操作并观察现象,你认为实验结论分析不正确的是( )
| 选项 | 操作 | 现象 | 结论 |
| A | 铁钉浸入硫酸铜溶液中 | 铁钉变红 | 铁比铜活泼 |
| B | 氢气通入灼热的氧化铜粉末中 | 黑色粉末变红 | 氢气具有还原性 |
| C | 向汗液中滴入硝酸银溶液、稀硝酸 | 产生白色沉淀 | 汗液中含有氯离子 |
| D | 纯碱与盐酸混合 | 有气泡产生 | 纯碱与盐酸发生中和反应 |
| A. | A | B. | B | C. | C | D. | D |

 化学反应中,物质所含元素的化合价发生变化的反应为氧化还原反应.其中化合价升高的发生氧化反应,作还原剂,化合价降低的发生还原反应,作氧化剂.
化学反应中,物质所含元素的化合价发生变化的反应为氧化还原反应.其中化合价升高的发生氧化反应,作还原剂,化合价降低的发生还原反应,作氧化剂. (1)如图是常用的电源插头,在标示的部件中,属于有机合成材料的是塑料.
(1)如图是常用的电源插头,在标示的部件中,属于有机合成材料的是塑料.