题目内容
18.生活处处有化学,请用化学知识回答以下生活中的问题:(1)饮用硬度过大的水不利于人体健康,生活中可用肥皂水区分硬水和软水;
(2)清洗餐具上的油污常用到洗涤剂,是因为洗涤剂有乳化功能;
(3)奶制品含有丰富的钙元素(填“单质”或“元素”),人体每天要摄入足够量的钙,老年人缺钙会导致骨质疏松.
(4)生产生活中可以用紫色石蕊溶液来检测土壤的酸碱性.
分析 (1)根据区分硬水和软水的方法进行分析;
(2)根据洗涤剂的乳化作用进行分析;
(3)根据奶制品和人体中钙的存在形式和钙的生理功能及缺乏症进行分析;
(4)根据检测溶液的酸碱性的方法进行分析.
解答 解:(1)硬水和软水的区别在于所含的钙镁离子的多少,生活中常用肥皂水来区分硬水和软水,产生泡沫较多的是软水,产生泡沫较少的是硬水;
(2)清洗餐具上的油污常用到洗涤剂,是因为洗涤剂有乳化功能;
(3)在奶制品中或在人体内,钙是以无机盐的形式存在的,这里的钙是指盐中含有的钙元素;老年人缺钙会患骨质疏松;
(4)紫色石蕊溶液遇酸性溶液变红,遇碱性溶液变蓝,可用于检测溶液的酸碱性.
故答案为:(1)肥皂水;(2)乳化;(3)元素;骨质疏松;(4)紫色石蕊溶液.
点评 化学来源于生产、生活,又服务于生产、生活,因此要充分利用所学的化学知识为生产、生活服务.

练习册系列答案
 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案
相关题目
3.某冶金厂的废液中含有硝酸铜和硝酸银,为回收其中的金属,四十七中学化学兴趣小组的同学们向废液中加入8.4g铁粉,恰好全反应得固体17.2g,则所得固体中铜和银的质量比为( )
| A. | 24:19 | B. | 94:85 | C. | 16:27 | D. | 8:27 |
10.下列各组物质在给定pH的溶液中能大量共存并形成无色溶液的是( )
| A. | pH为12:BaCl2、Na2CO3、NaOH | B. | pH为1:NaOH、KHCO3、Na2SO4 | ||
| C. | pH为2:KNO3、NaCl、H2SO4 | D. | pH为3:FeCl3、CuSO4、KCl |
7.某同学梳理归纳了以下知识点:①用水灭火的原理是降低了可燃物的着火点;②饱和溶液一定是该温度下该种溶质形成的最浓的溶液;③“粗盐中难溶性杂质的去除”的实验中,当蒸发皿中出现较多固体时,停止加热;④用点燃的方法能除去二氧化碳中混有的少量一氧化碳;⑤洗涤剂能去除油污是因为洗涤剂可以溶解油污;⑥日常生活中的不锈钢、铝合金和生铁都属于合金.其中正确的组合( )
| A. | ①⑤⑥ | B. | ②④⑤ | C. | ②③⑥ | D. | ③④⑥ |
8. 2008年“中国水周”活动的宣传主题为“发展水利,改善民生”.
2008年“中国水周”活动的宣传主题为“发展水利,改善民生”.
(1)①水属于(填“属于”或“不属于”)六大类营养素之一.
②保持水的化学性质的最小粒子是水分子.
(2)有一杯主要含有MgCl2和CaCl2的硬水.某兴趣小组设计出软化水的部分实验方案,请你一起来完成.
可供选用的物质有:Ca(OH)2溶液、NaOH溶液、饱和Na2CO3溶液、肥皂水
 2008年“中国水周”活动的宣传主题为“发展水利,改善民生”.
2008年“中国水周”活动的宣传主题为“发展水利,改善民生”.(1)①水属于(填“属于”或“不属于”)六大类营养素之一.
②保持水的化学性质的最小粒子是水分子.
(2)有一杯主要含有MgCl2和CaCl2的硬水.某兴趣小组设计出软化水的部分实验方案,请你一起来完成.
可供选用的物质有:Ca(OH)2溶液、NaOH溶液、饱和Na2CO3溶液、肥皂水
| 实验步骤 | 实验现象 | 结论或化学方程式 |
| ①取少量水样于试管中,滴加氢氧化钙溶液,直到不再产生沉淀 | 有白色沉淀产生 | MgCl2+Ca(OH)2═Mg(OH)2↓+CaCl2 |
| ②继续向上述试管中滴加 饱和Na2CO3溶液直到不再产生沉淀 | 有白色沉淀产生 | Na2CO3+CaCl2═CaCO3↓+2NaCl |
| ③过滤 | 滤液澄清 | --- |
| ④向滤液中滴加适量的肥皂水 | 产生大量泡沫 | 证明硬水已软化 |
 《花千骨》是一部古装仙侠玄幻剧,里面的主角迷倒了无数人.请试着用自己积累的化学知识回答下列问题
《花千骨》是一部古装仙侠玄幻剧,里面的主角迷倒了无数人.请试着用自己积累的化学知识回答下列问题

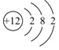 ,镁元素位于周期表中第三周期.;
,镁元素位于周期表中第三周期.;