题目内容
20.小明同学进行了如下的实验操作并观察现象,你认为实验结论分析不正确的是( )| 选项 | 操作 | 现象 | 结论 |
| A | 铁钉浸入硫酸铜溶液中 | 铁钉变红 | 铁比铜活泼 |
| B | 氢气通入灼热的氧化铜粉末中 | 黑色粉末变红 | 氢气具有还原性 |
| C | 向汗液中滴入硝酸银溶液、稀硝酸 | 产生白色沉淀 | 汗液中含有氯离子 |
| D | 纯碱与盐酸混合 | 有气泡产生 | 纯碱与盐酸发生中和反应 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、根据金属的化学性质,进行分析判断.
B、根据氢气具有还原性,进行分析判断.
C、根据氯离子的检验方法,进行分析判断.
D、中和反应是酸与碱作用生成盐和水的反应,反应物是酸和碱,生成物是盐和水.
解答 解:A、铁钉浸入硫酸铜溶液中生成硫酸亚铁溶液和铜,会观察到铁钉表面覆盖一层红色物质,说明铁比铜活泼,故选项说法正确.
B、氢气能与氧化铜反应生成铜和水,氢气通入灼热的氧化铜粉末中,黑色粉末变红,说明氢气具有还原性,故选项说法正确.
C、向汗液中滴入硝酸银溶液、稀硝酸,产生白色沉淀,说明生成了不溶于稀硝酸的氯化银白色沉淀,说明汗液中含有氯离子,故选项说法正确.
D、纯碱与盐酸混合,有气泡产生,是因为碳酸钠与稀盐酸反应生成氯化钠、水和二氧化碳,反应物是盐和酸,不属于中和反应,故选项说法错误.
故选:D.
点评 本题难度不大,掌握盐的化学性质、氢气的化学性质、金属的化学性质、中和反应的特征等是正确解答本题的关键.

练习册系列答案
相关题目
10.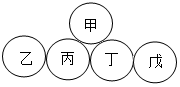 如图所示,图中甲、乙、丙、丁、戊分别是铁、盐酸、氢氧化钙、二氧化碳、碳酸钠中的一种.图中相连的两圆表示相应物质间能发生反应.下列说法错误的是( )
如图所示,图中甲、乙、丙、丁、戊分别是铁、盐酸、氢氧化钙、二氧化碳、碳酸钠中的一种.图中相连的两圆表示相应物质间能发生反应.下列说法错误的是( )
 如图所示,图中甲、乙、丙、丁、戊分别是铁、盐酸、氢氧化钙、二氧化碳、碳酸钠中的一种.图中相连的两圆表示相应物质间能发生反应.下列说法错误的是( )
如图所示,图中甲、乙、丙、丁、戊分别是铁、盐酸、氢氧化钙、二氧化碳、碳酸钠中的一种.图中相连的两圆表示相应物质间能发生反应.下列说法错误的是( )| A. | 甲一定是碳酸钠 | B. | 丙与丁的反应无明显现象 | ||
| C. | 丙可能是盐酸 | D. | 戊与丁的反应可能是复分解反应 |
11.下列是关于溶液的一些图表和图象,请根据图示回答问题:

(1)甲、乙两种固体物质的溶解度曲线如图1所示,分析并回答下列问题.
①图1中,溶解度随温度升高而减小的是乙.
②20℃时,将等质量的甲、乙分别加入盛有等质量水的试管中,充分溶解后如图2所示.据此推断,图1中温度t>(填“>”“<”或“=”)20℃.
(2)某烧杯中盛有一定质量、温度为60℃的甲溶液,将其置于室温环境中,测定不同温度时析出固体甲的质量.测定结果记录如下表.
若不考虑水蒸发对实验的影响,请思考:50℃时,该溶液是否为饱和溶液?无法判断(填“是”“否”或“无法判断”).

(1)甲、乙两种固体物质的溶解度曲线如图1所示,分析并回答下列问题.
①图1中,溶解度随温度升高而减小的是乙.
②20℃时,将等质量的甲、乙分别加入盛有等质量水的试管中,充分溶解后如图2所示.据此推断,图1中温度t>(填“>”“<”或“=”)20℃.
(2)某烧杯中盛有一定质量、温度为60℃的甲溶液,将其置于室温环境中,测定不同温度时析出固体甲的质量.测定结果记录如下表.
| 溶液的温度/℃ | 55 | 50 | 40 | 30 | 20 |
| 析出固体甲的质量/g | 0 | 0 | 2.0 | 4.5 | 8.4 |
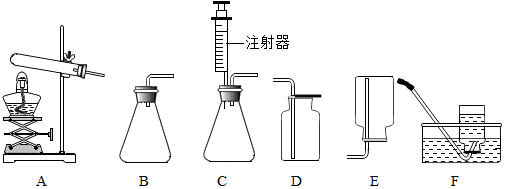
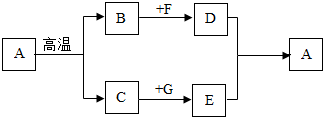
8. 将CO2和O2通入图中装置进行净化,最终得到的气体是( )
将CO2和O2通入图中装置进行净化,最终得到的气体是( )
 将CO2和O2通入图中装置进行净化,最终得到的气体是( )
将CO2和O2通入图中装置进行净化,最终得到的气体是( )| A. | CO2、O2 | B. | CO2 | C. | O2 | D. | O2、H2O |
14.在Cu(NO3)2和AgNO3的混合溶液中加入一定量的Zn,充分反应后过滤,留在滤纸上的固体一定( )
| A. | 有Zn | B. | 有ZnCuAg | C. | 有Cu和Ag | D. | 有Ag |

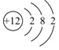 ,镁元素位于周期表中第三周期.;
,镁元素位于周期表中第三周期.;