题目内容
20.在浓硫酸的催化作用下,固体草酸(H2C2O4)受热分解生成碳的氧化物和水.某化学课外兴趣小组对碳的氧化物的成分进行了实验探究.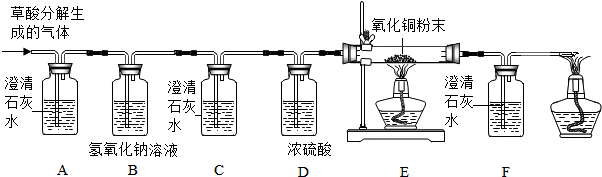
【提出问题】如何通过实验确定碳的氧化物的成分.
| 猜想1 | 猜想2 | 猜想3 |
| 只有CO | 只有CO2 | CO和CO2都有 |
【设计实验】基于猜想3,兴趣小组同学设计了如图实验装置:
【实验探究】
(1)实验过程中观察到A装置(填字母)中的澄清石灰水变浑浊,证明有CO2气体.
(2)实验过程中还观察到以下实验现象:①C装置中澄清石灰水不变浑浊;②E装置中黑色粉末变成红色;③F中澄清石灰水变浑浊,证明有CO气体.E装置中反应的化学方程式为CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2.
【实验结论】通过实验探究证明:猜想3成立.草酸分解的化学方程式是H2C2O4$\frac{\underline{\;浓硫酸\;}}{△}$CO2↑+CO↑+H2O.
【问题讨论】
(1)B装置的作用是检验二氧化碳是否被完全吸收,D装置的作用是吸收水分.
(2)装置末端酒精灯的作用是处理尾气CO,防止污染空气.
分析 【猜想】根据猜想1和3分析;
【实验探究】(1)A装置中的澄清石灰水变浑浊,能够证明有CO2气体;
(2)氧化铜有黑色变红色,最后有二氧化碳生成,说明有CO存在,根据反应物、反应条件、生成物然后写出化学反应式即可;
【实验结论】根据猜想3成立可知,反应物、反应条件、生成物然后写出化学反应式即可;
【问题讨论】(1)二氧化碳可以检验二氧化碳气体的存在;浓硫酸可以吸收水分;
(2)装置末端酒精灯可以处理尾气CO
解答 解:【猜想】根据猜想1和3可知,猜想2是只有CO2;
故答案为:CO2.
【实验探究】(1)二氧化碳遇澄清石灰水,可使石灰水变浑浊,所以A装置中的澄清石灰水变浑浊,能够证明有CO2气体;
故答案为:A.
(2)C装置中澄清石灰水不变浑浊,说明原有的二氧化碳已经被完全吸收;E装置中黑色粉末变成红色,说明氧化铜被还原;F中澄清石灰水变浑浊,说明有二氧化碳生成,说明还原气是CO.氧化碳与氧化铜混合加热生成铜和二氧化碳,反应的化学方程式为:CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2.
故答案为:黑色粉末变成红色;F中澄清石灰水变浑浊.CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2.
【实验结论】根据猜想3成立可知,生成物中有一氧化碳、二氧化碳、水,所以化学反应式是:H2C2O4$\frac{\underline{\;浓硫酸\;}}{△}$CO2↑+CO↑+H2O.
故答案为:H2C2O4$\frac{\underline{\;浓硫酸\;}}{△}$CO2↑+CO↑+H2O.
【问题讨论】(1)澄清石灰水可以检验二氧化碳气体的存在,所以C装置的作用是检验二氧化碳是否被完全吸收;浓硫酸可以吸收水分,所以D装置的作用是吸收水分;
故答案为:检验二氧化碳是否被完全吸收;吸收水分.
(2)为防止一氧化碳污染空气,装置末端酒精灯可以点燃尾气CO,防止污染空气.
故答案为:处理尾气CO,防止污染空气.
点评 此题是检验一氧化碳和二氧化碳的存在,就要我们熟悉一氧化碳和二氧化碳的性质特点.

 新编小学单元自测题系列答案
新编小学单元自测题系列答案| A. |  倾倒液体 | B. |  量取液体 | C. |  点燃酒精灯 | D. |  滴加液体 |
| A. | 糖类 | B. | 油脂 | C. | 蛋白质 | D. | 无机盐 |
 甲、乙两种固体的溶解度曲线如图所示.下列说法中,正确的是( )
甲、乙两种固体的溶解度曲线如图所示.下列说法中,正确的是( )| A. | 20℃时,甲溶液中溶质的质量分数一定大于乙溶液 | |
| B. | 40℃时,分别在100 g水中加入50 g 甲、乙,所得溶液溶质的质量分数相等 | |
| C. | 40℃时,分别在100 g水中加入30 g 甲、乙,同时降温至20℃,甲、乙溶液均为饱和溶液 | |
| D. | 20℃时,分别在100 g水中加入40 g 甲、乙,加热到40℃时,甲溶液为饱和溶液 |
| A. | H+、Ba2+、Cl-、SO42- | B. | CO32-、K+、Cl-、Ca2+ | ||
| C. | K+、NO3-、Na+、OH- | D. | K+、OH-、SO42-、Cu2+ |
| A. | Na2CO3 HCl,H2SO4 BaCl2 | B. | CuSO4 NaOH BaCl2 HCl | ||
| C. | HCl FeCl3 NaOH NaCl | D. | NaCl KOH Ca(OH)2 H2SO4 |
