题目内容
8.味精是烹制菜肴时常用的调味品,其主要成分是谷氨酸钠.谷氨酸钠有鲜味,易溶于水.小明发现某品牌味精包装上标注:“谷氨酸钠含量≥80%,NaCl含量≤20%”.他想测定此味精中NaCl的含量.【查 资 料】NaCl+AgNO3=AgCl↓+NaNO3,谷氨酸钠存在不影响NaCl性质.
【实验过程】
①称取该味精样品5.0g,并溶于蒸馏水;②加入过量的硝酸银溶液;③过滤;④用蒸馏水反复洗涤沉淀多次;⑤将沉淀烘干、称量,测得固体质量为2.87g.根据上述实验步骤回答下列有关问题:
(1)过滤操作所需要的仪器除烧杯、铁架台(带铁圈)、玻璃棒外,还需要的玻璃仪器是漏斗.
(2)此样品中NaCl的质量分数为23.4%,是否符合其包装上标注的标准?不符合.
【应用】最近专家否认了“味精致癌”的说法.实验表明,味精在100℃时加热半小时,只有0.3%的味精(谷氨酸钠)生成焦谷氨酸钠(有毒),其对人体的影响甚微.对此下列认识正确的是CD.
A.谷氨酸钠受热不发生化学变化
B.谷氨酸钠在加热下生成焦谷氨酸钠是物理变化
C.大量食用味精不利于身体健康
D.研究问题的一种有效方法是通过实验.
分析 (1)进行过滤操作最重要的一步就是过滤,需要的仪器较多烧杯(两只)、铁架台(带铁圈)、玻璃棒、漏斗、胶头滴管、洗瓶(塑料)等;
(2)根据生成的氯化银的质量计算出氯化钠的质量,进而求出质量分数,然后进行判断;
【应用】根据所给的信息进行判断作出正确的判断.
解答 解:(1)要使液体与固体分离,用过滤的方法进行,缺少的仪器是漏斗
(2)设调料味精中混有的氯化钠的质量为x
NaCl+AgNO3=AgCl↓+NaNO3
58.5 143.5
x 2.87g
$\frac{58.5}{x}$=$\frac{143.5}{2.87g}$
解得:x=1.17g
味精中氯化钠的质量分数为:$\frac{1.17g}{5g}$×100%=23.4%
23.4%>20%与包装的标准不符,所以不符合标准.
【应用】根据题意可以知道,谷氨酸钠受热已分解,能够产生有害物质,属于化学变化,所产生的物质对人体的身体健康不利,在解决问题时可以通过实验来解决
故答案为:
(1)漏斗;
(2)23.4%,不符合,CD.
点评 进行解题是我们必须培养的能力,熟练的利用化学方程式根据已知的物质的质量计算求出其它物质的质量.

练习册系列答案
相关题目
18.下列各组物质的溶液混合后,最终不一定有沉淀生成的是( )
| A. | Ba(OH)2 H2SO4 HCl | B. | CuCl2 NaOH HCl | ||
| C. | BaCl2 Na2CO3 HNO3 | D. | AgNO3 H2SO4 HCl |
19.2011年6月份,无锡被纳入全国26个环境空气质量评价方式试点城市.之后便开展了PM2.5、一氧化碳和臭氧等10项指标的试点监测. 下列说法正确的是( )
| A. | 直接焚烧植物秸秆不会造成大气污染 | |
| B. | 吸入细颗粒物对人体健康没有危害 | |
| C. | 化学在环境监测和保护中起重要作用 | |
| D. | 臭氧(03)是一种氧化物 |
16.下列说法正确的是( )
| A. | 手持量筒量取一定体积的液体 | |
| B. | 铁、氮气、氯化钠分别是由分子、原子、离子构成的 | |
| C. | 用托盘天平称量5.65g食盐 | |
| D. | 生铁和钢的物理性质不同主要是因为含碳量不同 |
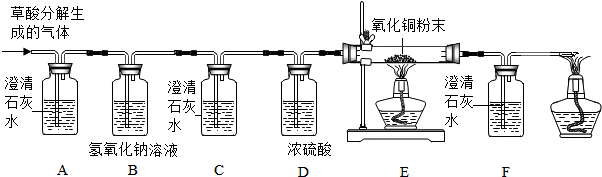
20.在浓硫酸的催化作用下,固体草酸(H2C2O4)受热分解生成碳的氧化物和水.某化学课外兴趣小组对碳的氧化物的成分进行了实验探究.
【提出问题】如何通过实验确定碳的氧化物的成分.
【猜 想】
【设计实验】基于猜想3,兴趣小组同学设计了如图实验装置:
【实验探究】
(1)实验过程中观察到A装置(填字母)中的澄清石灰水变浑浊,证明有CO2气体.
(2)实验过程中还观察到以下实验现象:①C装置中澄清石灰水不变浑浊;②E装置中黑色粉末变成红色;③F中澄清石灰水变浑浊,证明有CO气体.E装置中反应的化学方程式为CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2.
【实验结论】通过实验探究证明:猜想3成立.草酸分解的化学方程式是H2C2O4$\frac{\underline{\;浓硫酸\;}}{△}$CO2↑+CO↑+H2O.
【问题讨论】
(1)B装置的作用是检验二氧化碳是否被完全吸收,D装置的作用是吸收水分.
(2)装置末端酒精灯的作用是处理尾气CO,防止污染空气.

【提出问题】如何通过实验确定碳的氧化物的成分.
| 猜想1 | 猜想2 | 猜想3 |
| 只有CO | 只有CO2 | CO和CO2都有 |
【设计实验】基于猜想3,兴趣小组同学设计了如图实验装置:
【实验探究】
(1)实验过程中观察到A装置(填字母)中的澄清石灰水变浑浊,证明有CO2气体.
(2)实验过程中还观察到以下实验现象:①C装置中澄清石灰水不变浑浊;②E装置中黑色粉末变成红色;③F中澄清石灰水变浑浊,证明有CO气体.E装置中反应的化学方程式为CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2.
【实验结论】通过实验探究证明:猜想3成立.草酸分解的化学方程式是H2C2O4$\frac{\underline{\;浓硫酸\;}}{△}$CO2↑+CO↑+H2O.
【问题讨论】
(1)B装置的作用是检验二氧化碳是否被完全吸收,D装置的作用是吸收水分.
(2)装置末端酒精灯的作用是处理尾气CO,防止污染空气.
17.在配制10%NaCl溶液的过程中,导致溶液中NaCl质量分数小于10%的可能原因是:①用量筒量取水时仰视读数 ②配制溶液时烧杯先用少量水润湿 ③在天平的左盘称量氯化钠时,游码不在零位置就调节天平平衡,然后将游码移动到读数 ④盛装溶液的试剂瓶用蒸馏水润洗( )
| A. | ①②③④ | B. | ①②④ | C. | ①②③ | D. | ②③④ |
18.下列实验现象对应的结论正确的( )
| 选项 | A | B | C | D |
| 实验 | 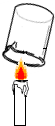 | 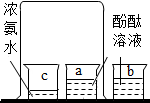 | 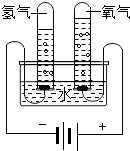 | 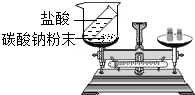 |
| 实验现象 | 烧杯内壁附着的澄清石灰水变浑浊 | a烧杯中溶液由无色变成红色 | 试管两极处有气体产生,且左右两极气体体积比为2:1 | 反应后天平指针向右偏移 |
| 实验结论 | 说明蜡烛燃烧产生二氧化碳和水 | 既说明分子在不断的运动,又说明浓氨水能使酚酞变红 | 既说明水由氢元素、氧元素组成,又说明水分子中含有氢分子和氧分子 | 盐酸与碳酸钠的反应不遵守质量守恒定律 |
| A. | A | B. | B | C. | C | D. | D |