题目内容
10.下列各组溶液,不用其他试剂,就不能将组内物质鉴别出来的是( )| A. | Na2CO3 HCl,H2SO4 BaCl2 | B. | CuSO4 NaOH BaCl2 HCl | ||
| C. | HCl FeCl3 NaOH NaCl | D. | NaCl KOH Ca(OH)2 H2SO4 |
分析 不用其他试剂,就能将组内物质鉴别出来,首先需考虑物质的颜色,然后将鉴别出来的物质与其他物质混合,根据现象的不同加以鉴别,若物质都是没有颜色,则让溶液之间两两混合,根据不同的实验现象加以鉴别.
解答 解:A、四种物质两两混合,既能产生沉淀,又能产生气泡的是碳酸钠,能够和碳酸钠反应产生沉淀的是氯化钡,能够和氯化钡产生沉淀的还有稀硫酸,剩下的是稀盐酸,可以鉴别;故不符合题意;
B、硫酸铜溶液为蓝色,首先鉴别出硫酸铜;然后向硫酸铜溶液中滴加其它三种溶液,能够产生蓝色沉淀的是氢氧化钠,能够产生白色沉淀的是氯化钡,无明显现象的是盐酸,可以鉴别,故不符合题意;
C、氯化铁溶液为黄色,首先鉴别出氯化铁;然后向氯化铁中滴加其他三种物质,有红棕色沉淀生成的为NaOH;向红棕色沉淀中滴加其他两种溶液,沉淀溶解的为稀HCl,无现象的为NaCl,所以该组溶液不用其他试剂就能鉴别出来;故不合题意;
D、四种物质两两混合,硫酸能够和氢氧化钾、氢氧化钙反应,但都没有现象,因此无法鉴别四种物质;故符合题意;
故选项为:D.
点评 本题考查了常见物质的鉴别,不用其他试剂,应该采用供检物质两两混合的方式,根据物质的溶液颜色以及物质间反应实验现象进行,要求同学们掌握基础知识,以便灵活应用.

练习册系列答案
相关题目
20.在浓硫酸的催化作用下,固体草酸(H2C2O4)受热分解生成碳的氧化物和水.某化学课外兴趣小组对碳的氧化物的成分进行了实验探究.
【提出问题】如何通过实验确定碳的氧化物的成分.
【猜 想】
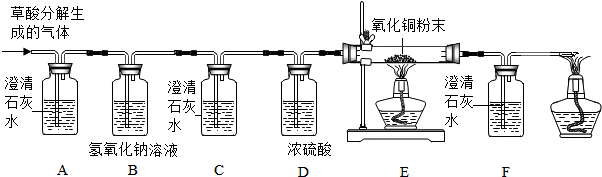
【设计实验】基于猜想3,兴趣小组同学设计了如图实验装置:
【实验探究】
(1)实验过程中观察到A装置(填字母)中的澄清石灰水变浑浊,证明有CO2气体.
(2)实验过程中还观察到以下实验现象:①C装置中澄清石灰水不变浑浊;②E装置中黑色粉末变成红色;③F中澄清石灰水变浑浊,证明有CO气体.E装置中反应的化学方程式为CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2.
【实验结论】通过实验探究证明:猜想3成立.草酸分解的化学方程式是H2C2O4$\frac{\underline{\;浓硫酸\;}}{△}$CO2↑+CO↑+H2O.
【问题讨论】
(1)B装置的作用是检验二氧化碳是否被完全吸收,D装置的作用是吸收水分.
(2)装置末端酒精灯的作用是处理尾气CO,防止污染空气.

【提出问题】如何通过实验确定碳的氧化物的成分.
| 猜想1 | 猜想2 | 猜想3 |
| 只有CO | 只有CO2 | CO和CO2都有 |
【设计实验】基于猜想3,兴趣小组同学设计了如图实验装置:
【实验探究】
(1)实验过程中观察到A装置(填字母)中的澄清石灰水变浑浊,证明有CO2气体.
(2)实验过程中还观察到以下实验现象:①C装置中澄清石灰水不变浑浊;②E装置中黑色粉末变成红色;③F中澄清石灰水变浑浊,证明有CO气体.E装置中反应的化学方程式为CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2.
【实验结论】通过实验探究证明:猜想3成立.草酸分解的化学方程式是H2C2O4$\frac{\underline{\;浓硫酸\;}}{△}$CO2↑+CO↑+H2O.
【问题讨论】
(1)B装置的作用是检验二氧化碳是否被完全吸收,D装置的作用是吸收水分.
(2)装置末端酒精灯的作用是处理尾气CO,防止污染空气.
1.如图是X、Y、Z三种固体物质的溶解度曲线图.下列说法正确的是( )


| A. | 在t1温度时三者的溶解度从大到小的顺序依次是:X、Y、Z | |
| B. | t2 时,X、Y两种物质的饱和溶液的溶质质量分数相等 | |
| C. | 将t2温度三者的饱和溶液降温至t1温度时,三者溶液都有晶体析出 | |
| D. | 若将t2℃时X物质的不饱和溶液转变成饱和溶液,可采用的一种方法是升高温度 |
18.下列实验现象对应的结论正确的( )
| 选项 | A | B | C | D |
| 实验 | 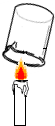 | 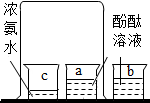 | 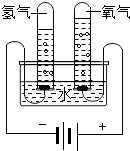 | 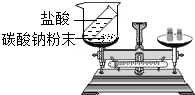 |
| 实验现象 | 烧杯内壁附着的澄清石灰水变浑浊 | a烧杯中溶液由无色变成红色 | 试管两极处有气体产生,且左右两极气体体积比为2:1 | 反应后天平指针向右偏移 |
| 实验结论 | 说明蜡烛燃烧产生二氧化碳和水 | 既说明分子在不断的运动,又说明浓氨水能使酚酞变红 | 既说明水由氢元素、氧元素组成,又说明水分子中含有氢分子和氧分子 | 盐酸与碳酸钠的反应不遵守质量守恒定律 |
| A. | A | B. | B | C. | C | D. | D |
5.某校兴趣小组对氢氧化钠溶液与稀盐酸混合后的有关问题,进行了如下探究,请同学们一起参与此次探究之旅.
(1)探究一:判断氢氧化钠溶液与稀盐酸混合后是否恰好完全中和?
【方案设计】小亮、小丽、小林三位同学设计了如下方案进行探究:
【方案评价】请判断以上设计的三个方案中,小丽同学的方案是正确的.
【方案反思】请分析另外两个方案错误的原因:反应后的溶液如果呈酸性,酚酞也不变色;因为中和反应的产物NaCl和硝酸银溶液反应也会产生白色沉淀.
(2)探究二:氢氧化钠溶液与稀盐酸混合后,所得溶液中溶质的成分是什么?
【作出猜想】小亮猜想:溶质有NaCl、HCl、NaOH
小丽猜想:溶质只有NaCl
小林猜想:溶质有NaCl、HCl
你的猜想:溶质有NaCl、NaOH(填化学式)
小丽认为小亮的猜想是错误的,她的理由是由于氢氧化钠可以和稀盐酸反应,所以盐酸和氢氧化钠不能共存.
【实验设计及验证】请你将下列实验报告填写完整:
(1)探究一:判断氢氧化钠溶液与稀盐酸混合后是否恰好完全中和?
【方案设计】小亮、小丽、小林三位同学设计了如下方案进行探究:
| 方案设计者 | 方案步骤 | 方案预估现象 | 方案预估结论 |
| 小亮 | 取少量反应后的溶液于一支试管中,并向试管中滴加几滴无色酚酞试液,振荡 | 酚酞试液 不变色 | 恰好完全中和 |
| 小丽 | 用一根洁净的玻璃棒蘸取反应后的溶液沾在pH试纸上,把试纸呈现的颜色与标准比色卡对照 | pH=7 | 恰好完全中和 |
| 小林 | 取少量反应后的溶液于一支试管中,并向试管中滴加稀硝酸和硝酸银溶液 | 有白色沉淀生产 | 盐酸过量,没 有完全中和 |
【方案反思】请分析另外两个方案错误的原因:反应后的溶液如果呈酸性,酚酞也不变色;因为中和反应的产物NaCl和硝酸银溶液反应也会产生白色沉淀.
(2)探究二:氢氧化钠溶液与稀盐酸混合后,所得溶液中溶质的成分是什么?
【作出猜想】小亮猜想:溶质有NaCl、HCl、NaOH
小丽猜想:溶质只有NaCl
小林猜想:溶质有NaCl、HCl
你的猜想:溶质有NaCl、NaOH(填化学式)
小丽认为小亮的猜想是错误的,她的理由是由于氢氧化钠可以和稀盐酸反应,所以盐酸和氢氧化钠不能共存.
【实验设计及验证】请你将下列实验报告填写完整:
| 实验操作 | 实验现象 | 实验结论 |
| 取反应后的溶液于试管中,加入碳酸钠溶液 | ③ | 小林猜想正确 |
| ④ | 有蓝色沉淀生成 | 你的猜想正确 |
6.要解决“温室效应”问题,在生活中我们可以采取的措施正确的是( )
①禁止使用化石燃料
②大力植树种草,严禁乱砍滥伐
③逐步普及太阳能等清洁能源
④大力推广乙醇汽油.
①禁止使用化石燃料
②大力植树种草,严禁乱砍滥伐
③逐步普及太阳能等清洁能源
④大力推广乙醇汽油.
| A. | ①③ | B. | ②③ | C. | ②③④ | D. | ①②③④ |
4.下列说法正确的是( )
| A. | 能使燃着的木条熄灭的气体一定是二氧化碳 | |
| B. | 一氧化碳、二氧化碳均为无色无毒气体 | |
| C. | 一氧化碳与二氧化碳的分子构成不同 | |
| D. | 一氧化碳通入紫色石蕊试液,试液会变红 |