题目内容
14.绿茶中含有的单宁酸(其化学式为C76H52O46)具有抑制血压上升、清热解毒等功效,下列关于单宁酸的说法中正确的是( )| A. | 属于氧化物 | |
| B. | 由碳原子、氢分子和氧分子构成 | |
| C. | 碳、氧两种元素的相对质量比为76:46 | |
| D. | 氢元素的质量分数最小 |
分析 单宁酸由碳、氢、氧三种元素组成;每个单宁酸分子由76个碳原子、52个氢原子、46个氧原子构成;一个单宁酸分子中各种原子的个数比为:38:26:23;而各种元素的质量比为(12×76):(1×52):(16×46),进行分析解答.
解答 解:A、氧化物只有两种元素组成,单宁酸是由碳、氢、氧三种元素组成的,故选项说法错误.
B、单宁酸是由单宁酸分子构成的,不含有碳原子、氢分子和氧分子,故选项说法错误.
C、单宁酸中碳、氧元素的质量比为(12×76):(16×46);题中76:46是原子个数比,所以说法错误;
D、单宁酸中碳、氢、氧元素的质量比为(12×76):(1×52):(16×46)=228:13:184;故氢元素的质量分数最小,故选项说法正确.
故选:D
点评 本题难度不大,考查同学们结合新信息灵活运用化学式的含义、有关计算进行分析问题、解决问题的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
2.乙酸乙酯( C4H8O2)常用作食品、饮料的调香剂.下列有关乙酸乙酯的叙述正确的是( )
| A. | 由14个原子构成 | |
| B. | 其中碳元素的质量分数为41.4% | |
| C. | 一个乙酸乙酯分子中,碳、氢、氧原子的个数比为2:4:1 | |
| D. | 其中碳、氢、氧元素的质量比为12:1:16 |
5.下列物质的用途中,主要利用其化学性质的是( )
| A. | 铜丝做导线 | B. | 石墨制铅笔芯 | C. | 液氨做制冷剂 | D. | 焦炭用于炼铁 |
6. 溶解度是解决溶液相关问题的重要依据.
溶解度是解决溶液相关问题的重要依据.
I.根据图1解决下列问题:(M,N均不含结晶水)
(1)溶解度随温度的升高而减小的是N,温度为t2℃时,M,N两种物质的溶解度相等;
(2)t1℃时,将20gM加入50g水中,充分溶解,形成溶液的质量为65g.保持温度不变,向该溶液中再加入10g水充分搅拌,溶液的溶质质量分数将不变(填“变大”、“变小”或“不变”);
Ⅱ.根据表格解决实际问题:
某KNO3样品中含有少量K2CO3,其提纯过程如图2:
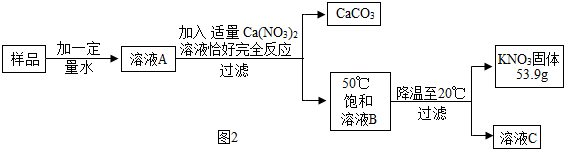
(1)操作2的名称是过滤.若图2中溶液B是饱和溶液,则C是饱和(填“饱和”或“不饱和”)溶液;
(2)写出向溶液A中加入Cu(NO3)2发生反应的化学方程式K2CO3+Ca(NO3)2=CaCO3↓+2KNO3 .
 溶解度是解决溶液相关问题的重要依据.
溶解度是解决溶液相关问题的重要依据.I.根据图1解决下列问题:(M,N均不含结晶水)
(1)溶解度随温度的升高而减小的是N,温度为t2℃时,M,N两种物质的溶解度相等;
(2)t1℃时,将20gM加入50g水中,充分溶解,形成溶液的质量为65g.保持温度不变,向该溶液中再加入10g水充分搅拌,溶液的溶质质量分数将不变(填“变大”、“变小”或“不变”);
Ⅱ.根据表格解决实际问题:
| 温度/℃ | 20 | 30 | 50 | 60 | 80 | |
| 溶解度/g | KNO3 | 31.6 | 45.8 | 85.5 | 100 | 169 |
| K2CO3 | 110 | 114 | 121 | 126 | 139 | |

(1)操作2的名称是过滤.若图2中溶液B是饱和溶液,则C是饱和(填“饱和”或“不饱和”)溶液;
(2)写出向溶液A中加入Cu(NO3)2发生反应的化学方程式K2CO3+Ca(NO3)2=CaCO3↓+2KNO3 .
4. 小明同学在总结酸、碱、盐之间的相互反应关系时发现,选用适当物质可实现如图中所示的 所有反应.若中间的物质为硫酸钡,那么对酸、碱、甲盐、乙盐四种物质的推断中,合理的是( )
小明同学在总结酸、碱、盐之间的相互反应关系时发现,选用适当物质可实现如图中所示的 所有反应.若中间的物质为硫酸钡,那么对酸、碱、甲盐、乙盐四种物质的推断中,合理的是( )
 小明同学在总结酸、碱、盐之间的相互反应关系时发现,选用适当物质可实现如图中所示的 所有反应.若中间的物质为硫酸钡,那么对酸、碱、甲盐、乙盐四种物质的推断中,合理的是( )
小明同学在总结酸、碱、盐之间的相互反应关系时发现,选用适当物质可实现如图中所示的 所有反应.若中间的物质为硫酸钡,那么对酸、碱、甲盐、乙盐四种物质的推断中,合理的是( )| A. | HCl NaOH BaCl2 Na2SO4 | B. | H2SO4 Ba(OH)2 Na2SO4 BaCl2 | ||
| C. | HCl Ba(OH)2 Na2SO4 BaCl2 | D. | H2SO4 NaOH BaCl2 Na2SO4 |





