题目内容
9.建立宏观、微观和符号之间的联系是化学学科的特点.(1)图1表示水、二氧化碳和氧气的循环图.

①从宏观角度看,图1中三种物质的组成中都含有氧元素.
从微观角度看,图1中三种物质都是由分子构成的.
②试写出图1中c对应的化学方程式:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
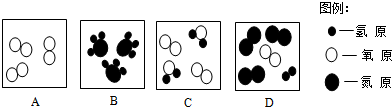
③图2为图1中b对应一种反应的微观示意图.由此图你能获得的信息有化学反应前后原子的种类和数目不变(任写一点).
(2)图3表示氯和溴元素(Br)的原子结构示意图,由图可知,溴在元素周期表中位于第四周期,氯和溴具有相似化学性质是因为原子的最外层电子数相同,氯气常用于自来水消毒,是因为氯气能与水反应生成盐酸和次氯酸(HClO),写出溴单质(Br2)与氢氧化钠溶液反应的化学方程式:Br2+2NaOH═NaBr+NaBrO+H2O.
分析 (1)①根据物质的组成和构成分析回答;
②根据水通电生成了氧气分析回答;
③根据微粒的变化分析分子、原子的变化等;
(2)在原子中,电子层数等于周期数,最外层电子数决定了元素性质,根据氯气能与水的反应,写出溴单质(Br2)与氢氧化钠溶液反应的化学方程式.
解答 解:(1)①从宏观角度看,图1中三种物质的组成中都含有氧元素.从微观角度看,图1中三种物质都是由分子 构成的.
②图1中c对应的反应可以是水通电生成了氧气和氢气,反应的化学方程式是:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
③图2为图1中b对应一种反应的微观示意图.由微粒的变化可知,化学反应前后原子的种类和数目不变等.
(2)图3表示氯和溴元素(Br)的原子结构示意图,由图可知,溴原子的核外有四个电子层,该元素周期表中位于第四周期,氯和溴具有相似化学性质是因为原子的最外层电子数相同,氯气常用于自来水消毒,是因为氯气能与水反应生成盐酸和次氯酸(HClO),则溴单质(Br2)与氢氧化钠溶液反应的化学方程式为:Br2+2NaOH═NaBr+NaBrO+H2O.
故答为:(1)①氧元素,分子 ②2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑ ③化学反应前后原子的种类和数目不变;(2)原子的最外层电子数相同 Br2+2NaOH═NaBr+NaBrO+H2O
点评 本题的难度不大,能够从宏观和微粒两个方面正确认识物质是解答本题的基础知识.

练习册系列答案
相关题目
17.在冶炼金属钛时会发生如下反应:TiO2+2Cl2+2C═TiCl4+2X,其中X的化学式是( )
| A. | CO | B. | TiO | C. | CO2 | D. | ClO2 |
14.绿茶中含有的单宁酸(其化学式为C76H52O46)具有抑制血压上升、清热解毒等功效,下列关于单宁酸的说法中正确的是( )
| A. | 属于氧化物 | |
| B. | 由碳原子、氢分子和氧分子构成 | |
| C. | 碳、氧两种元素的相对质量比为76:46 | |
| D. | 氢元素的质量分数最小 |
18.为配制溶质质量分数为1.15%的磷酸二氢铵溶液用于无土栽培,已称取2.3kg的磷酸二氢铵固体,还需要水( )
| A. | 200kg | B. | 197.7kg | C. | 230kg | D. | 59.6kg |
19.下列各组溶液,不用其他试剂就不能鉴别出来的是( )
| A. | NaCl、AgNO3、CuCl2、稀HNO3 | B. | NaOH、稀HCl、FeCl3、KNO3 | ||
| C. | 酚酞、Ca(OH)2、Na2CO3、NaNO3 | D. | Na2CO3、稀HCl、Ba(NO3)2、稀H2SO4 |
 现有一瓶久置的过氧化氢溶液(标签如图所示),已知过氧化氢溶液在存放过程中会缓慢分解,取该溶液34g于烧杯中,加入一定量的二氧化锰,完全反应后,称得烧杯内剩余物质的总质量是33.8g,将杯内剩余物质过滤、洗涤、干燥后得滤渣3g.
现有一瓶久置的过氧化氢溶液(标签如图所示),已知过氧化氢溶液在存放过程中会缓慢分解,取该溶液34g于烧杯中,加入一定量的二氧化锰,完全反应后,称得烧杯内剩余物质的总质量是33.8g,将杯内剩余物质过滤、洗涤、干燥后得滤渣3g. 甲、乙、丙三种固体物质的溶解度曲线如图所示,请加答下列问题.
甲、乙、丙三种固体物质的溶解度曲线如图所示,请加答下列问题.