题目内容
9.实验课上,为检验镁条能否在N2中燃烧,兴趣小组展开如下探究:【查阅资料】氮化镁(Mg3N2)是一种淡黄色固体,能和水反应,生成Mg(OH)2和NH3;
【实验步骤】
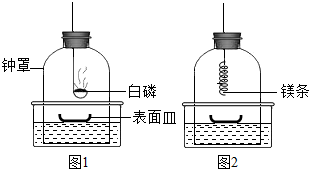
①将足量白磷在空气中点燃后,迅速伸入钟罩内,塞紧橡皮塞(图1);
②待钟罩内水面不再变化时,向水槽中加水,使水槽中液面与钟罩内液面相平;
③打开橡皮塞,将燃着的螺旋状镁条迅速伸入钟罩内,塞紧橡皮塞(图2);
④待钟罩内水面不再变化时,观察钟罩内壁及表面皿中固体颜色,取少量固体加入水中.
【分析】
(1)步骤①中足量白磷在钟罩内燃烧的目的是除去钟罩内空气中的氧气,以便镁条在氮气中燃烧;
(2)步骤②中如果不加水至水槽中液面与钟罩内液面相平,会造成什么后果?使钟罩内外气压一致,防止空气进入钟罩,影响后续(步骤③)实验,造成偏差;
(3)步骤③中镁条绕成螺旋状的目的是增大接触面积、积聚热量;镁条剧烈燃烧,反应的化学方程式
为3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2,反应的现象是镁带剧烈燃烧,发出耀眼的白光,放出大量的热,产生白色固体
(4)步骤④中钟罩内壁及表面皿中出现淡黄色固体.加入水中,产生白色浑浊及能使湿润红色石蕊试纸变蓝色的气体,反应的化学方程式为Mg3N2+6H2O═3Mg(OH)2+2NH3↑;
【结论】
镁能在N2中燃烧,并生成Mg3N2.
(5)请你判断:2.40g镁条在某密闭容器中完全燃烧,所得固体质量可能为CD;
A.3.33g B.4.00g C.3.93g D.3.96g.
分析 (1)根据实验目的探究镁条能否与氮气反应分析白磷燃烧的目的
(2)根据减小实验误差分析
(3)根据绕成螺旋状与不绕成螺旋状受热面积不同分析
(4)根据题中信息写出化学方程式
(5)极端假设全部生成氧化镁或氮化镁,分别求出其质量.
解答 解:(1)要验证镁条在氮气中能否燃烧,需将空气中的氧气除去,因此步骤①中足量白磷在钟罩内燃烧的目的是 除去钟罩内空气中的氧气,以便镁条在氮气中燃烧;
(2)步骤①结束后钟罩内水面上升,此时钟罩内气压小于外界气压,向钟罩内加水是为了使钟罩内外气压一致,防止空气进入钟罩,影响后续(步骤③)实验,造成偏;
(3)步骤③中镁条绕城螺旋状的目的是 增大受热面积;镁条剧烈燃烧生成氮化镁,反应的化学方程式为 3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$ Mg3N2;反应的现象是 镁带剧烈燃烧,发出耀眼的白光,放出大量的热,产生白色固体.
(4)步骤④中钟罩内壁及表面皿中出现淡黄色固体.此固体为氮化镁(Mg3N2),能和水反应,生成Mg(OH)2和NH3,因此加入水中,产生白色沉淀氢氧化镁及能使湿润红色石蕊试纸变 蓝色的气体氨气,反应的化学方程式为 Mg3N2+6H2O═3Mg(OH)2+2NH3↑;
(5)设2.4g镁全部与氧气反应,则生成氧化镁的质量为$\frac{24g}{\frac{24}{40}}$=4g 设2.4g镁全部与氮气反应生成氮化镁,则生成的氮化镁的质量为$\frac{24g}{\frac{24×3}{24×3+14×2}}$=3.33g
因此2.4g镁燃烧生成的固体质量应大于3.33g小于4g,故选CD
故答案为:(1)除去钟罩内空气中的氧气,以便镁条在氮气中燃烧
(2)使钟罩内外气压一致,防止空气进入钟罩,影响后续(步骤③)实验,造成偏差
(3)增大接触面积、积聚热量 3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2 镁带剧烈燃烧,发出耀眼的白光,放出大量的热,产生白色固体.
(4)蓝 Mg3N2+6H2O═3Mg(OH)2+2NH3↑
(5)CD
点评 本题主要考查学生获取信息并运用信息的能力,解答本题的关键是要充分理解镁的性质,只有这样才能对问题做出正确的判断.

(1)草木灰是一种农家肥料,有效成分是碳酸钾(K2CO3),草木灰属于钾(填“磷”或“钾”)肥.
(2)测得某地土壤酸碱度的pH为4.5,下列作物适合在该地区种植的是茶树;若要种植玉米,需要施用熟石灰降低土壤酸性.
| 作物 | 小麦 | 玉米 | 茶树 | 西瓜 | 萝卜 |
| 适宜生长的pH | 5.5-6.5 | 6.5-7.0 | 4.0-6.5 | 5.0-7.0 | 7.0-7.5 |
(4)当身体某些部位发生磕碰或出现伤口时,可以先用冷敷袋进行处理,冷敷袋中有一层很薄的膜将水与一种固体分开,使用时挤压包装袋即可将两种物质混合,下列物质适合做冷敷袋中固体物质的是B(填字母序号).
A、NaHCO3 B、NH4NO3 C、NaOH
(5)在汽车电路中,经常用铜作导线,这是利用了铜的延展性和导电性.
(6)铝抗腐蚀性能好,是因为铝与氧气反应,在其表面生成一层致密的氧化铝薄膜,氧化铝的化学式为Al2O3.
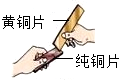
(7)黄铜是铜锌合金,将纯铜片和黄铜片相互刻画(如图所示),纯铜片上留下明显的划痕,说明黄铜的硬度比纯铜的大.
(8)自然界中的水需净化后饮用,活性炭常用于净化水,其主要作用是吸附.
(9)啤酒酿造需要大量的软水,生活中常用肥皂水区别软水和硬水.
(10)水常用于灭火,其灭火原理是隔绝氧气并降温至着火点以下.
| A. | 酒精挥发 | B. | 轮胎在烈日下爆裂 | ||
| C. | 菜刀生锈 | D. | 瓷碗破碎 |
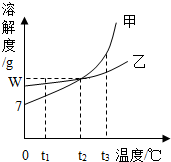 甲、乙两物质的溶解度曲线如图所示,下列叙述错误的是( )
甲、乙两物质的溶解度曲线如图所示,下列叙述错误的是( )| A. | t1℃时,甲的溶解度小于乙的溶解度 | |
| B. | t1℃时,加入甲物质,可使不饱和的甲溶液变成饱和溶液 | |
| C. | 将甲、乙饱和溶液的温度从t3℃降到t1℃时,乙析出晶体比甲多 | |
| D. | t2℃时,甲或乙两种物质的饱和溶液中溶质与溶剂的质量比是W:100 |
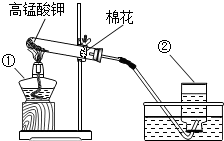 老师在课堂上用高锰酸钾利用下图所示的装置制取氧气.回答下列问题:
老师在课堂上用高锰酸钾利用下图所示的装置制取氧气.回答下列问题: