题目内容
1.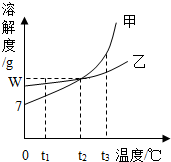 甲、乙两物质的溶解度曲线如图所示,下列叙述错误的是( )
甲、乙两物质的溶解度曲线如图所示,下列叙述错误的是( )| A. | t1℃时,甲的溶解度小于乙的溶解度 | |
| B. | t1℃时,加入甲物质,可使不饱和的甲溶液变成饱和溶液 | |
| C. | 将甲、乙饱和溶液的温度从t3℃降到t1℃时,乙析出晶体比甲多 | |
| D. | t2℃时,甲或乙两种物质的饱和溶液中溶质与溶剂的质量比是W:100 |
分析 A、据溶解度曲线可比较同一温度下不同物质的溶解度大小;
B、不饱和溶液变为饱和溶液可采取加入溶质的方法;
C、不知溶液的质量,无法判断析出晶体质量多少;
D、据该温度下甲乙的溶解度分析解答.
解答 解:A、t1℃时,甲的溶解度小于乙的溶解度,正确;
B、t1℃时,加入甲物质,可使不饱和的甲溶液变成饱和溶液,还可采取恒温蒸发溶剂的方法,正确;
C、不知饱和溶液的质量,无法判断析出晶体质量多少,若二者饱和溶液的质量相等,则将甲、乙饱和溶液的温度从t3℃降到t1℃时,乙析出晶体比甲多,故错误;
D、t2℃时,甲乙的溶解度相等,均是wg,即100g水中最多溶解wg的溶质,故两种物质的饱和溶液中溶质与溶剂的质量比是W:100,正确;
故选:C.
点评 了解溶解度曲线的意义、溶解度的概念,并能灵活运用,等质量的饱和溶液降低相同的温度,溶解度变化大的析出溶质多.

练习册系列答案
 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
11.某同学针对石蜡燃烧开展如下延伸探究,请你帮助解决探究过程的相关问题:
【提出问题】石蜡中除含碳、氢元素外,是否还含有氧元素?
【实验设计】根据质量守恒定律,该同学用精制石蜡、棉线烛芯做成蜡烛,设计了如下实验(其中浓硫酸、无水硫酸铜均易吸收水分,药品用量保证充足,部分固定装置省略).

【操作原理】
(1)请写出A装置(含导气管)气密性的检查方法:先关闭分液漏斗的活塞,将导气管一端放入水中,用手紧握烧瓶,若导管口有气泡产生,则装置气密性良好,反之,则不好.装置A中发生反应的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(2)装置B的作用是干燥氧气;装置D的作用是确保不完全燃烧的一氧化碳及碳全部转化为二氧化碳.
(3)装置F发生反应的化学方程式是2NaOH+CO2═Na2CO3+H2O.
(4)为达到实验目的,反应前、后必须称量CEF(填装置序号)装置中的药品质量.
【数据处理】
(5)该同学在老师帮助下,经过一些补充实验和误差处理后得出了如下数据,请你帮助完成数据分析及结论部分.
【讨论交流】误差分析与处理:
(6)根据该学生设计的实验,你认为造成误差的原因是装置内残留的空气含有水和二氧化碳或棉线烛芯燃烧也会产生水和二氧化碳或未完全燃烧的石蜡蒸气、碳黑残留在导管内或未进行多次重复实验等(填写一条).
(7)针对你提出的误差原因,提出减少误差的实验或改进措施:实验前先通氧气将装置内的空气赶尽或取相同规格的棉线烛芯代替蜡烛,做相同的实验,然后扣除相应的数据或进行多次重复实验取平均值等.
【提出问题】石蜡中除含碳、氢元素外,是否还含有氧元素?
【实验设计】根据质量守恒定律,该同学用精制石蜡、棉线烛芯做成蜡烛,设计了如下实验(其中浓硫酸、无水硫酸铜均易吸收水分,药品用量保证充足,部分固定装置省略).

【操作原理】
(1)请写出A装置(含导气管)气密性的检查方法:先关闭分液漏斗的活塞,将导气管一端放入水中,用手紧握烧瓶,若导管口有气泡产生,则装置气密性良好,反之,则不好.装置A中发生反应的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(2)装置B的作用是干燥氧气;装置D的作用是确保不完全燃烧的一氧化碳及碳全部转化为二氧化碳.
(3)装置F发生反应的化学方程式是2NaOH+CO2═Na2CO3+H2O.
(4)为达到实验目的,反应前、后必须称量CEF(填装置序号)装置中的药品质量.
【数据处理】
(5)该同学在老师帮助下,经过一些补充实验和误差处理后得出了如下数据,请你帮助完成数据分析及结论部分.
| 实验事实 | 数据分析及结论 |
| 2.12g石蜡完全燃烧,得到6.6g CO2和2.88g H2O | 写出计算过程: 结论:石蜡中不含氧元素. |
(6)根据该学生设计的实验,你认为造成误差的原因是装置内残留的空气含有水和二氧化碳或棉线烛芯燃烧也会产生水和二氧化碳或未完全燃烧的石蜡蒸气、碳黑残留在导管内或未进行多次重复实验等(填写一条).
(7)针对你提出的误差原因,提出减少误差的实验或改进措施:实验前先通氧气将装置内的空气赶尽或取相同规格的棉线烛芯代替蜡烛,做相同的实验,然后扣除相应的数据或进行多次重复实验取平均值等.
10.下列有关二氧化碳的说法正确的是( )
| A. | 二氧化碳过多引发酸雨 | B. | 二氧化碳气体可用于人工降雨 | ||
| C. | 二氧化碳可使紫色石蕊试液变蓝 | D. | 二氧化碳可作为气体肥料 |
7.牙膏是生活中常见的物质,其配料成分有摩擦剂、增稠剂、发泡剂等,其中摩擦剂的类型有很多,如CaCO3、Al(OH)3、SiO2或这些物质的混合物.我校化学兴趣小组同学想研究牙膏摩擦剂的成分.
【实验探究一】某品牌牙膏中是否含有CaCO3?
【查阅资料】二氧化硅不与稀盐酸反应
【实验方案】
【实验探究二】该牙膏中CaCO3的含量是多少?
【实验装置】利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数.
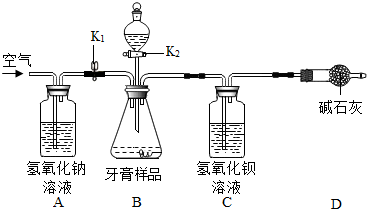
【友情提示】
(1)氢氧化钡跟氢氧化钙的性质类似,CO2+Ba(OH)2═BaCO3↓+H2O;
(2)CO2的相对分子质量为44,CaCO3的相对分子质量为100,BaCO3的相对分子质量为197;
(3)以上药品均足量,且每步反应或作用都是完全的.
【实验步骤】
(1)按上图连接好装置后,检查装置的气密性;
(2)在B装置中加入牙膏样品8.00g;
(3)先断开装置B和C,打开K1,关闭K2,通入空气一段时间,目的是赶尽装置中的空气,再接上装置B和C;关闭K1,打开K2(选填“打开”或“关闭”),向牙膏样品中滴入10%的盐酸,至不再产生气泡为止,停止滴加盐酸;然后再打开K1,关闭K2(选填“打开”或“关闭”),缓缓通入空气至C中不再产生沉淀为止,目的是将反应生成的二氧化碳气体赶到装置C中充分反应.
(4)将C装置中的固液混合物过滤、洗涤、烘干后称量其质量;
(5)重复实验.
【实验数据】重复实验,3次数据记录如下:
【实验分析及数据处理】
(1)装置A的作用是CO2+2NaOH=Na2CO3+H2O(用化学方程式表示),若没有A装置,则测定结果将偏大(选填“偏大”、“偏小”或“不变”).
(2)装置B中产生气体的化学方程式CaCO3+2HCl═CaCl2+H2O+CO2↑.
(3)装置D的作用是防止空气中的二氧化碳气体进入装置C中,产生误差.
(4)据上表数据,取D装置中沉淀质量的平均值为3.94g,目的是减小偶然误差,使实验数据更准确;由产生沉淀的质量可计算出反应生成二氧化碳的质量为0.88g,然后可求出牙膏样品中CaCO3的质量分数为25%.
【实验探究一】某品牌牙膏中是否含有CaCO3?
【查阅资料】二氧化硅不与稀盐酸反应
【实验方案】
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量样品于试管中,滴加稀盐酸 | ①产生大量气泡 | 该牙膏样品中含有CaCO3 |
| ②把生成的气体通入澄清石灰水中 | ②石灰水变浑浊 |
【实验装置】利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数.

【友情提示】
(1)氢氧化钡跟氢氧化钙的性质类似,CO2+Ba(OH)2═BaCO3↓+H2O;
(2)CO2的相对分子质量为44,CaCO3的相对分子质量为100,BaCO3的相对分子质量为197;
(3)以上药品均足量,且每步反应或作用都是完全的.
【实验步骤】
(1)按上图连接好装置后,检查装置的气密性;
(2)在B装置中加入牙膏样品8.00g;
(3)先断开装置B和C,打开K1,关闭K2,通入空气一段时间,目的是赶尽装置中的空气,再接上装置B和C;关闭K1,打开K2(选填“打开”或“关闭”),向牙膏样品中滴入10%的盐酸,至不再产生气泡为止,停止滴加盐酸;然后再打开K1,关闭K2(选填“打开”或“关闭”),缓缓通入空气至C中不再产生沉淀为止,目的是将反应生成的二氧化碳气体赶到装置C中充分反应.
(4)将C装置中的固液混合物过滤、洗涤、烘干后称量其质量;
(5)重复实验.
【实验数据】重复实验,3次数据记录如下:
| 实验次数 | 实验1 | 实验2 | 实验3 |
| D装置中沉淀质量(g) | 3.93 | 3.94 | 3.95 |
(1)装置A的作用是CO2+2NaOH=Na2CO3+H2O(用化学方程式表示),若没有A装置,则测定结果将偏大(选填“偏大”、“偏小”或“不变”).
(2)装置B中产生气体的化学方程式CaCO3+2HCl═CaCl2+H2O+CO2↑.
(3)装置D的作用是防止空气中的二氧化碳气体进入装置C中,产生误差.
(4)据上表数据,取D装置中沉淀质量的平均值为3.94g,目的是减小偶然误差,使实验数据更准确;由产生沉淀的质量可计算出反应生成二氧化碳的质量为0.88g,然后可求出牙膏样品中CaCO3的质量分数为25%.