题目内容
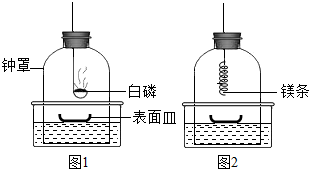
19.空气中含有氮气、氧气、二氧化碳和水蒸气等成分,试填空:(1)能说明空气中含有氧气的现象或事实是:木炭可以在空气中燃烧等;
(2)能说明空气中含有水蒸气的现象或事实是:酥脆的饼干在空气中放置一段时间后变软;
(3)能说明空气中含有二氧化碳的现象或事实是:石灰水露置在空气中一段时间后,液面会形成一层白色薄膜;
(4)化工厂用空气为原料制取氮肥.原因是空气中含有氮气.
分析 空气的成分含有氮气、氧气、二氧化碳、稀有气体等,结合各成分的性质与用途进行分析解答即可.
解答 解:(1)氧气能支持燃烧,木炭可以在空气中燃烧,能说明空气中含有氧气(合理即可).
(2)酥脆的饼干在空气中放置一段时间后变软,是因为吸收了空气的水蒸气,说明空气中含有水蒸气(合理即可).
(3)石灰水露置在空气中一段时间后,液面会形成一层白色薄膜,原因是空气中含有二氧化碳,二氧化碳与氢氧化钙反应生成碳酸钙白色沉淀和水(合理即可).
(4)化工厂用空气为原料制取氮肥,原因是空气中含有氮气.
故答案为:(1)木炭可以在空气中燃烧等;(2)酥脆的饼干在空气中放置一段时间后变软;(3)石灰水露置在空气中一段时间后,液面会形成一层白色薄膜;(4)空气中含有氮气.
点评 本题难度不大,结合生活实际考查了空气的成分,了解空气中各种成分的性质与用途是解答本题的关键.

练习册系列答案
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案
相关题目
10.下列有关二氧化碳的说法正确的是( )
| A. | 二氧化碳过多引发酸雨 | B. | 二氧化碳气体可用于人工降雨 | ||
| C. | 二氧化碳可使紫色石蕊试液变蓝 | D. | 二氧化碳可作为气体肥料 |
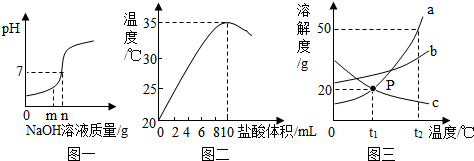
4.t℃时,向硝酸钠饱和溶液中加入一定量的水,下列有关该溶液的叙述正确的是( )
| A. | 溶质的质量分数不变 | B. | 溶质的质量变小 | ||
| C. | 溶液的质量增大 | D. | 仍为饱和溶液 |
7.牙膏是生活中常见的物质,其配料成分有摩擦剂、增稠剂、发泡剂等,其中摩擦剂的类型有很多,如CaCO3、Al(OH)3、SiO2或这些物质的混合物.我校化学兴趣小组同学想研究牙膏摩擦剂的成分.
【实验探究一】某品牌牙膏中是否含有CaCO3?
【查阅资料】二氧化硅不与稀盐酸反应
【实验方案】
【实验探究二】该牙膏中CaCO3的含量是多少?
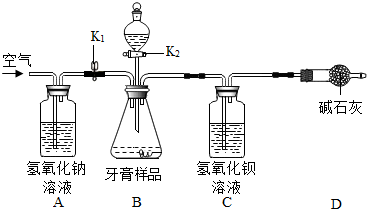
【实验装置】利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数.
【友情提示】
(1)氢氧化钡跟氢氧化钙的性质类似,CO2+Ba(OH)2═BaCO3↓+H2O;
(2)CO2的相对分子质量为44,CaCO3的相对分子质量为100,BaCO3的相对分子质量为197;
(3)以上药品均足量,且每步反应或作用都是完全的.
【实验步骤】
(1)按上图连接好装置后,检查装置的气密性;
(2)在B装置中加入牙膏样品8.00g;
(3)先断开装置B和C,打开K1,关闭K2,通入空气一段时间,目的是赶尽装置中的空气,再接上装置B和C;关闭K1,打开K2(选填“打开”或“关闭”),向牙膏样品中滴入10%的盐酸,至不再产生气泡为止,停止滴加盐酸;然后再打开K1,关闭K2(选填“打开”或“关闭”),缓缓通入空气至C中不再产生沉淀为止,目的是将反应生成的二氧化碳气体赶到装置C中充分反应.
(4)将C装置中的固液混合物过滤、洗涤、烘干后称量其质量;
(5)重复实验.
【实验数据】重复实验,3次数据记录如下:
【实验分析及数据处理】
(1)装置A的作用是CO2+2NaOH=Na2CO3+H2O(用化学方程式表示),若没有A装置,则测定结果将偏大(选填“偏大”、“偏小”或“不变”).
(2)装置B中产生气体的化学方程式CaCO3+2HCl═CaCl2+H2O+CO2↑.
(3)装置D的作用是防止空气中的二氧化碳气体进入装置C中,产生误差.
(4)据上表数据,取D装置中沉淀质量的平均值为3.94g,目的是减小偶然误差,使实验数据更准确;由产生沉淀的质量可计算出反应生成二氧化碳的质量为0.88g,然后可求出牙膏样品中CaCO3的质量分数为25%.
【实验探究一】某品牌牙膏中是否含有CaCO3?
【查阅资料】二氧化硅不与稀盐酸反应
【实验方案】
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量样品于试管中,滴加稀盐酸 | ①产生大量气泡 | 该牙膏样品中含有CaCO3 |
| ②把生成的气体通入澄清石灰水中 | ②石灰水变浑浊 |
【实验装置】利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数.

【友情提示】
(1)氢氧化钡跟氢氧化钙的性质类似,CO2+Ba(OH)2═BaCO3↓+H2O;
(2)CO2的相对分子质量为44,CaCO3的相对分子质量为100,BaCO3的相对分子质量为197;
(3)以上药品均足量,且每步反应或作用都是完全的.
【实验步骤】
(1)按上图连接好装置后,检查装置的气密性;
(2)在B装置中加入牙膏样品8.00g;
(3)先断开装置B和C,打开K1,关闭K2,通入空气一段时间,目的是赶尽装置中的空气,再接上装置B和C;关闭K1,打开K2(选填“打开”或“关闭”),向牙膏样品中滴入10%的盐酸,至不再产生气泡为止,停止滴加盐酸;然后再打开K1,关闭K2(选填“打开”或“关闭”),缓缓通入空气至C中不再产生沉淀为止,目的是将反应生成的二氧化碳气体赶到装置C中充分反应.
(4)将C装置中的固液混合物过滤、洗涤、烘干后称量其质量;
(5)重复实验.
【实验数据】重复实验,3次数据记录如下:
| 实验次数 | 实验1 | 实验2 | 实验3 |
| D装置中沉淀质量(g) | 3.93 | 3.94 | 3.95 |
(1)装置A的作用是CO2+2NaOH=Na2CO3+H2O(用化学方程式表示),若没有A装置,则测定结果将偏大(选填“偏大”、“偏小”或“不变”).
(2)装置B中产生气体的化学方程式CaCO3+2HCl═CaCl2+H2O+CO2↑.
(3)装置D的作用是防止空气中的二氧化碳气体进入装置C中,产生误差.
(4)据上表数据,取D装置中沉淀质量的平均值为3.94g,目的是减小偶然误差,使实验数据更准确;由产生沉淀的质量可计算出反应生成二氧化碳的质量为0.88g,然后可求出牙膏样品中CaCO3的质量分数为25%.
4.阿司匹林是常见解热镇痛药之一,其化学式为C7H6O3,.下列对其叙述正确的是( )
| A. | 每个阿司匹林分子中含3 个氢分子 | |
| B. | 它的相对分子质量为138 g | |
| C. | 该化合物中碳、氢、氧三种元素质量比为12:l:16 | |
| D. | 69 g 阿司匹林含碳元素质量为42 g |