题目内容
20.阅读下面科普短文.食醋中一般含有3%~5%的醋酸,醋酸的化学名称叫乙酸(CH3COOH),是无色有刺激性气味的液体,能溶于水.
食醋可以除去水壶内的水垢,水垢的主要成分是碳酸钙.除水垢时,可在水壶中加入水,倒入适量醋,浸泡一段时间,不溶于水的碳酸钙会转变成可溶于水的醋酸钙而被除掉,化学方程式为:CaCO3+2CH3COOH═(CH3COO)2Ca+H2O+CO2↑.
在熬制骨头汤时,常常在汤中加入少量食醋,因为骨头中含有不溶于水的磷酸钙,当磷酸钙与醋酸作用时生成可溶于水的磷酸二氢钙,能够增加汤内的含钙量,促进人体对钙、磷的吸收和利用.
食醋不仅在厨房中大显身手,还是一种杀菌剂,冬天在屋子里熬醋可以杀灭细菌,对抗感冒有很大作用.饮酒过量的人可以用食醋来解酒,因为乙酸能跟乙醇发生酯化反应生成乙酸乙酯(CH3COOC2H5)和水,从而达到解酒的目的.
由于醋酸能与活泼的金属发生置换反应产生氢气,所以家用铝制品不能用来盛放食醋,以免被腐蚀.
根据文章内容,回答下列问题:
(1)乙酸属于有机物(填“有机物”或“无机物”).
(2)乙酸的物理性质无色有刺激性气味液体,能溶于水.
(3)食醋能用来解酒的原因是乙酸能跟乙醇发生酯化反应生成乙酸乙酯和水,从而达到解酒的目的.
(4)用铁锅炒菜时,放一点食醋能补铁,用化学方程式解释原因2CH3COOH+Fe=(CH3COO)2Fe+H2↑.
(5)醋酸和盐酸、硫酸的化学性质,是因为它们在水溶液中均能解离出H+.
分析 (1)含有碳元素的化合物叫有机化合物,简称有机物.
(2)物理性质是不需要发生化学变化就能表现出来的性质,包括物质的颜色、状态、气味、熔点、沸点、密度、溶解性等.
(3)根据题意,饮酒过量的人可以用食醋来解酒,因为乙酸能跟乙醇发生酯化反应生成乙酸乙酯(CH3COOC2H5)和水,从而达到解酒的目的.
(4)铁的金属活动性比氢强,能与醋酸反应生成醋酸亚铁和氢气,写出反应的化学方程式即可.
(5)根据酸是电离时产生的阳离子全部是氢离子的化合物,据此进行分析解答.
解答 解:(1)乙酸是含碳元素的化合物,属于有机物.
(2)由新信息可知,醋酸是无色有刺激性气味液体,能溶于水,不需要通过化学变化就能表现出来,属于物理性质.
(3)饮酒过量的人可以用食醋来解酒,因为乙酸能跟乙醇发生酯化反应生成乙酸乙酯(CH3COOC2H5)和水,从而达到解酒的目的.
(4)铁的金属活动性比氢强,能与醋酸反应生成醋酸亚铁和氢气,反应的化学方程式为:2CH3COOH+Fe=(CH3COO)2Fe+H2↑.
(5)醋酸和盐酸、硫酸的化学性质,是因为它们在水溶液中均能解离出氢离子,其离子符号为:H+.
故答案为:
(1)有机物;
(2)无色有刺激性气味液体,能溶于水;
(3)乙酸能跟乙醇发生酯化反应生成乙酸乙酯和水,从而达到解酒的目的;
(4)2CH3COOH+Fe=(CH3COO)2Fe+H2↑;
(5)H+.
点评 本题难度不大,掌握酸的化学性质、有机物的特征、物理性质的特征、化学方程式的书写方法等是正确解答本题的关键.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
10.下列化学反应中,没有黑色物质生成的是( )
| A. | 加热碱式碳酸铜 | B. | 铁丝在氧气中燃烧 | ||
| C. | 加热碳铵 | D. | 加热高锰酸钾 |
11.以下是四位同学对生活中的化学现象进行探究后的结果表述,其中不正确的是( )
| A. | “纯碱”其实不是碱,属于盐类 | |
| B. | 可用纯碱代替洗涤灵洗涤餐具表面的油污 | |
| C. | 用加水溶解的方法检验纯碱中是否混入了食盐 | |
| D. | 用纯碱可除去面团发酵产生的酸 |
8.水资源非常重要,联合国确定2003年为国际淡水年.海水淡化是海岛地区提供淡水的重要手段,所谓海水淡化是指除去海水中的盐分以获得淡水的工艺过程(又称海水脱盐),其方法较多,如反渗透法、水合物法、电渗透法、离子交换法和压渗法等.下列方法中也可以用来进行海水淡化的是( )
| A. | 过滤法 | B. | 蒸馏法 | C. | 分液法 | D. | 萃取法 |
15.下列实验操作正确的是( )
| A. | 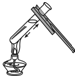 加热液体 | B. | 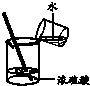 稀释浓硫酸 | C. | 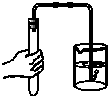 检验气密性 | D. |  熄灭酒精灯 |
5.下列反应属于化合反应的是( )
| A. | 水--氧气+氢气 | B. | 氧化汞--汞+氧气 | ||
| C. | 铝+氧气--氧化铝 | D. | 石蜡+氧气--二氧化碳+水 |
9.课外小组同学进一步研究铁与氧气的反应.
【提出问题】铁丝燃烧时为什么会有“火星四射”的现象?
【查阅资料】生铁中含有一定量的碳.铁丝燃烧时“火星四射”现象与铁丝中含碳量有关.
【进行实验】探究铁丝在氧气中燃烧时“火星四射”的现象与其含碳量的关系.
【提出问题】纯铁在氧气中燃烧溅落的“黑色固体”是什么?
【查阅资料】
①自然界中铁的氧化物主要是Fe3O4和Fe2O3两种(FeO易被氧化)
②铁的氧化物均能溶于酸溶液
③单质铁与稀盐酸反应的化学方程式为:Fe+2HCl═FeCl2+H2↑.
【进行实验】测定黑色固体的成分.
【实验反思】
同学们认为铁丝燃烧的现象还与氧气的浓度有关,所以想收集不同浓度的氧气进行相关实验.若用排水集气法收集一瓶体积分数约为60%的氧气,预先应向容积为250mL的集气瓶中加水,水的体积约为125mL.
【提出问题】铁丝燃烧时为什么会有“火星四射”的现象?
【查阅资料】生铁中含有一定量的碳.铁丝燃烧时“火星四射”现象与铁丝中含碳量有关.
【进行实验】探究铁丝在氧气中燃烧时“火星四射”的现象与其含碳量的关系.
| 实验 | 现象 | 解释与结论 |
| 实验1:取直径0.20mm、含碳0.1% 的铁丝,在氧气中燃烧 | 零星的火星四射 | ①铁燃烧的化学方程式是3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4. ②0.20mm的铁丝在氧气中燃烧,“火星四射”与其含碳量的关系为含碳量越高,火星四射的现象越明显 |
| 实验2:取直径0.20mm、含碳0.32%的铁丝,在氧气中燃烧 | 较明显的火星四射 | |
| 实验3:取直径0.20mm、含碳0.52%的铁丝,在氧气中燃烧 | 明显的火星四射 |
【查阅资料】
①自然界中铁的氧化物主要是Fe3O4和Fe2O3两种(FeO易被氧化)
②铁的氧化物均能溶于酸溶液
③单质铁与稀盐酸反应的化学方程式为:Fe+2HCl═FeCl2+H2↑.
【进行实验】测定黑色固体的成分.
| 实验 | 现象及数据 | 解释与结论 |
| 实验4:将冷却后的黑色固体碾碎,装入试管,加入稀盐酸 | 现象是有气泡产生 | 铁燃烧时溅落下来的黑色 固体中含有铁 |
| 实验5:取2.8g纯铁在氧气中燃烧,收集溅落的黑色固体,干燥并称其质量 | 黑色固体质量为3.44g | 黑色固体的组成及质量 为Fe1.12g,Fe3O42.32g |
同学们认为铁丝燃烧的现象还与氧气的浓度有关,所以想收集不同浓度的氧气进行相关实验.若用排水集气法收集一瓶体积分数约为60%的氧气,预先应向容积为250mL的集气瓶中加水,水的体积约为125mL.
10.科学家研制出高灵敏度的CO探测器,通过颜色变化可探测空气中是否含有CO.下列有关说法不正确的是( )
| A. | CO的物理性质是无色、无味、具有可燃性 | |
| B. | 该探测器可警示室内燃煤取暖是否安全 | |
| C. | CO中毒时,应将病人迅速转移到室外 | |
| D. | CO有毒,是因其易与人体中的血红蛋白结合,影响血液对氧气的输送 |