题目内容
3.框图中A的浓溶液通常用作干燥剂,B广泛用于制肥皂、炼制石油、造纸等的生产,F→G发生非常复杂的化学变化,G是一种红棕色的固体,E、F、I为无色气体.根据图示回答下列问题(部分反应物、生成物已略去).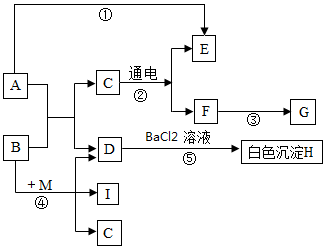
(1)写出有关物质的化学式:BNaOH、HBaSO4;
(2)日常生活中为了阻止反应③发生,通常采取的措施是刷漆(写一条);
(3)要使反应④能够发生,需要反应物B和M,其中M的化学式为(NH4)2SO4.
分析 根据题干提供的信息进行分析解答,A的浓溶液通常用作干燥剂,故A是硫酸;B广泛用于制肥皂、炼制石油、造纸等的生产,故B是氢氧化钠;F→G发生非常复杂的化学变化,G是一种红棕色的固体,故G是氧化铁,F是无色气体,故F是氧气,C通电生成氧气和E,故C是水,E是氢气;硫酸和氢氧化钠反应生成水和硫酸钠,故D是硫酸钠,硫酸钠和氯化钡反应生成的白色沉淀H是硫酸钡;氢氧化钠能与M反应生成硫酸钠、I和C,I是气体,故M可能是硫酸铵,生成的I是氨气,据此解答.
解答 解:A的浓溶液通常用作干燥剂,故A是硫酸;B广泛用于制肥皂、炼制石油、造纸等的生产,故B是氢氧化钠;F→G发生非常复杂的化学变化,G是一种红棕色的固体,故G是氧化铁,F是无色气体,故F是氧气,C通电生成氧气和E,故C是水,E是氢气;硫酸和氢氧化钠反应生成水和硫酸钠,故D是硫酸钠,硫酸钠和氯化钡反应生成的白色沉淀H是硫酸钡;氢氧化钠能与M反应生成硫酸钠、I和C,I是气体,故M可能是硫酸铵,生成的I是氨气,带入框图,推断合理;
(1)B是氢氧化钠,H是硫酸钡,故填:NaOH;BaSO4;
(2)反应③是铁的锈蚀的过程,可以采用刷漆的方法防止铁的锈蚀,故填:刷漆;
(3)M是硫酸铵,故填:(NH4)2SO4.
点评 物质推断题的推断主要是找到突破口,之后围绕突破口进行展开.本题的物质转化关系是借助常见物质的转化来实现的,所以平时学习中要通过构建物质转化关系的网络图加深对物质的整体理解和掌握.最后一问是信息给予题,要从信息中需要突破.

练习册系列答案
相关题目
14.以下实验方法中,能达到目的是
| 选项 | 目的 | 方法 |
| A | 除去氯化铁中的盐酸 | 加入适量的铁粉 |
| B | 除去NaCl溶液中的CaCl2 | 加入适量的Na2CO3溶液,过滤 |
| C | 除去HCl气体中的CO2 | 通过足量的NaOH溶液 |
| D | 除去炭粉中的铁粉 | 加入足量的CuSO4溶液后过滤 |
| A. | A | B. | B | C. | C | D. | D |
11.我市盛产石灰石,其中含有的杂质主要是二氧化硅.某学生为了测定石灰石中碳酸钙的含量,取10.0克石灰石样品,经粉碎后放入烧杯中,并加入足量的稀盐酸(石灰石中的杂质不与稀盐酸反应),烧杯及所盛物质的总质量为80.0克.反应过程中测得烧杯及所盛物质的质量与相应反应时间记录如小表:
(1)反应生成CO2的总质量为2.2克.
(2)实验室制取气体,采用图中B套装置,收集CO2气体时,应从C装置中的a导管进入.
(3)该石灰石样品中碳酸钙的质量分数是多少?
| 反应时间/分 | 0 | 2 | 4 | 6 | 8 | 10 |
| 烧杯及所盛物质质量/克 | 80.0 | 79.0 | 78.3 | 77.9 | 77.8 | 77.8 |
(2)实验室制取气体,采用图中B套装置,收集CO2气体时,应从C装置中的a导管进入.

(3)该石灰石样品中碳酸钙的质量分数是多少?
12.化学与生活有着千丝万缕的联系,下列做法错误的是( )
| A. | 用洗洁精的乳化作用洗去餐具上的油污 | |
| B. | 为了防止食品变质腐烂,我们可以用甲醛溶液来浸泡食品 | |
| C. | 食盐中加入适量的碘可预防甲状腺肿大 | |
| D. | 用灼烧法鉴别蚕丝和涤纶面料 |
13.下列有关溶液性质的说法中正确的是( )
| A. | 均一、稳定的液体一定是溶液 | |
| B. | 溶液一定是无色透明的 | |
| C. | 食盐水能导电是因为食盐水中含有较多自由移动的离子 | |
| D. | 硝酸铵溶于水后溶液温度升高 |
