题目内容
14.以下实验方法中,能达到目的是| 选项 | 目的 | 方法 |
| A | 除去氯化铁中的盐酸 | 加入适量的铁粉 |
| B | 除去NaCl溶液中的CaCl2 | 加入适量的Na2CO3溶液,过滤 |
| C | 除去HCl气体中的CO2 | 通过足量的NaOH溶液 |
| D | 除去炭粉中的铁粉 | 加入足量的CuSO4溶液后过滤 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、氯化铁和盐酸均能与铁粉反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
B、CaCl2能与适量的Na2CO3溶液反应生成碳酸钙沉淀和氯化钠,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
C、CO2和HCl气体均能与NaOH溶液反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
D、铁粉能与足量的CuSO4溶液反应生成硫酸亚铁溶液和铜,能除去杂质但引入了新的杂质铜,不符合除杂原则,故选项所采取的方法错误.
故选:B.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
13.下列实验现象描述错误的是( )
| A. | 向米饭上滴加几滴碘水后呈现蓝色 | |
| B. | 氢氧化钠固体溶于水,溶液温度升高 | |
| C. | 镁条在空气中燃烧,发出耀眼白光,生成黑色固体 | |
| D. | 将铁片放入硫酸铜溶液中,铁片上出现红色物质 |
2.下列质量增加的变化,有一种与其他三种存在本质的区别.这种变化是( )
| A. | 久置的生石灰质量增加 | |
| B. | 久置的铁钉生锈质量增加 | |
| C. | 长期放置在空气中的氢氧化钠质量增加 | |
| D. | 长期敞口放置的浓硫酸质量增加 |
9.下列变化中,属于化学变化的是( )
| A. | 金属拉丝 | B. | 酒精燃烧 | C. | 干冰升华 | D. | 冰雪融化 |
6.下列物质不属于有机物的是( )
| A. | 甲烷 | B. | 蛋白质 | C. | 二氧化碳 | D. | 脂肪 |
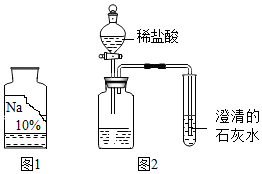
4.某化学兴趣小组在实验室发现一瓶标签残缺的溶液如图1,在老师的指导下进行如下探究:
甲同学取少量该溶液于试管中,滴加少量氯化钡溶液,发现生成了大量白色沉淀,于是他认为该溶液中的溶质是硫酸钠.
乙同学经过思考后,认为甲同学的结论不可靠,设计了如下实验:
丙同学认为,要确认是碳酸钠,还应按图2进行改进.他取该溶液于锥形瓶中,打开分液漏斗的玻璃活塞K,滴加少量稀盐酸,结果意外发现没有冒气泡,澄清石灰水也没变浑浊.
提出猜想:猜想一:盐酸放置时间过久,溶质已完全挥发
猜想二:碳酸钠变质
猜想三:当滴加的盐酸较少时,先和碳酸钠反应生成了一种新的化合物
【进行实验】(1)向该盐酸中加入少量铁粉,产生大量气泡
(2)向该溶液A中滴加氯化钙溶液,产生大量沉淀
【实验小结】猜想一和猜想二都是错误的
写出实验(1)的化学方程式Fe+2HCl═FeCl2+H2↑
【讨论与交流】
丁同学认为实验(2)不必要做,原因是甲同学滴加氯化钡溶液已经证明了猜想二是错误的.
进一步探究:在老师的指导下,同学们查到如下相关资料.
【查阅资料】溶液里的复分解反应实际上是离子间的反应,碳酸钠和酸反应的过程如下
2H++CO32-=H2O+CO2↑,每个碳酸根离子需要结合2个氢离子才能生成CO2,当H+的量不够时,则发生H++CO32-=HCO3-
【进行实验】请你设计一个实验证明猜想三是否正确
【实验反思】若没有任何试剂可通过互滴法来鉴别稀盐酸和碳酸钠溶液.
甲同学取少量该溶液于试管中,滴加少量氯化钡溶液,发现生成了大量白色沉淀,于是他认为该溶液中的溶质是硫酸钠.
乙同学经过思考后,认为甲同学的结论不可靠,设计了如下实验:
| 实验操作 | 实验现象 | 实验结论 |
| 取甲同学的生成物,过滤,向滤渣中加入稀盐酸 | 白色沉淀溶解,产生无色无味的气体 | 该溶液不是硫酸钠溶液,而是碳酸钠溶液 |

提出猜想:猜想一:盐酸放置时间过久,溶质已完全挥发
猜想二:碳酸钠变质
猜想三:当滴加的盐酸较少时,先和碳酸钠反应生成了一种新的化合物
【进行实验】(1)向该盐酸中加入少量铁粉,产生大量气泡
(2)向该溶液A中滴加氯化钙溶液,产生大量沉淀
【实验小结】猜想一和猜想二都是错误的
写出实验(1)的化学方程式Fe+2HCl═FeCl2+H2↑
【讨论与交流】
丁同学认为实验(2)不必要做,原因是甲同学滴加氯化钡溶液已经证明了猜想二是错误的.
进一步探究:在老师的指导下,同学们查到如下相关资料.
【查阅资料】溶液里的复分解反应实际上是离子间的反应,碳酸钠和酸反应的过程如下
2H++CO32-=H2O+CO2↑,每个碳酸根离子需要结合2个氢离子才能生成CO2,当H+的量不够时,则发生H++CO32-=HCO3-
【进行实验】请你设计一个实验证明猜想三是否正确
| 实验操作 | 实验现象 | 结论 |
| 向反应后的溶液中继续加入盐酸 | 立即产生大量气泡 | 猜想三正确 |
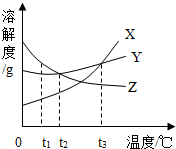 如图是X、Y、Z三种固体物质的溶解度曲线图,根据曲线图回答下列问题:
如图是X、Y、Z三种固体物质的溶解度曲线图,根据曲线图回答下列问题: