题目内容
18.向100g的稀盐酸中加入100gAgNO3溶液,恰好完全反应.过滤后得28.7g白色沉淀.求反应后所得溶液的溶质质量分数.(结果保留0.1%)分析 根据生成的白色沉淀为氯化银,根据氯化银的质量和对应的化学方程式求算硝酸的质量,进而求算对应的溶液中溶质的质量分数.
解答 解:设生成的硝酸的质量为x
HCl+AgNO3=AgCl↓+HNO3
143.5 63
28.7g x
$\frac{143.5}{63}$=$\frac{28.7g}{x}$
x=12.6g
反应后溶液中溶质的质量分数为$\frac{12.6g}{100g+100g-28.7g}$×100%≈7.4%
答:反应后所得溶液的溶质质量分数约为7.4%
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
8.下列知识归纳中,完全正确的是( )
| A.化学常识 | B.化学与生活 |
| ①活性炭除异味是利用它的吸附性 ②铵态氮肥不能与碱性物质混合使用 ③充入氮气食品防腐 | ①用pH试纸测定洗发水的酸碱度 ②用氢氧化钠改良酸性土壤 ③碳酸氢钠是焙制糕点发酵粉成分之一 |
| C.化学与健康 | D.化学与安全 |
| ①人体缺维生素C易患坏血病 ②海鲜防腐可以用甲醛溶液浸泡 ③霉变的大米可高温加热后食用 | ①图书、档案着火,用CO2灭火器灭火 ②在室内放一盆水,可防止煤气中毒 ③为防止矿井中瓦斯爆炸,严禁吸烟 |
| A. | A | B. | B | C. | C | D. | D |
9.下列变化中,属于化学变化的是( )
| A. | 金属拉丝 | B. | 酒精燃烧 | C. | 干冰升华 | D. | 冰雪融化 |
6.下列物质不属于有机物的是( )
| A. | 甲烷 | B. | 蛋白质 | C. | 二氧化碳 | D. | 脂肪 |
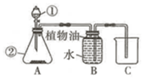 如图是小华同学设计的气体制取和收集装置,请你和他一起回答下列问题:
如图是小华同学设计的气体制取和收集装置,请你和他一起回答下列问题: