题目内容
17.空气是一种宝贵资源,如利用空气中分离出的氮气合成氨气,合成氨对社会发展和人类进步做出了巨大贡献,下列是合成氨的工艺流程图:
(1)空气中氮气的体积分数约为78%;
(2)将沸点不同的气体分离开来,常采用液化分离法.如控制温度在-183℃时,可将空气中N2与O2分离.根据下表中物质的沸点判断,要将产物NH3与N2、H2分离开来,温度应该控制在-33.35℃.
| 物质 | H2 | N2 | O2 | NH3 |
| 沸点 | -252℃ | -195.8℃ | -183℃ | -33.35℃ |
(4)写出N2、H2反应生成NH3的化学方程式N2+3H2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$2NH3;
(5)用“
 ”分别表示N2、H2、NH3.观察图,写出符合在催化剂表面合成氨反应的顺序⑤④①②③(将下面五张图按反应过程顺序用数字序号排列);
”分别表示N2、H2、NH3.观察图,写出符合在催化剂表面合成氨反应的顺序⑤④①②③(将下面五张图按反应过程顺序用数字序号排列);
(6)氨气是大气污染物,不能任意排放到空气中.下列物质排放到空气中,不会造成大气污染的是D(填字母序号).
A.一氧化碳 B.二氧化碳 C.二氧化氮 D.氮气.
分析 (1)空气中氮气的体积分数约为78%;
(2)根据提供的信息可以判断分离物质时需要控制的温度;
(3)没有生成新物质的变化属于物理变化,生成新物质的变化属于化学变化;
(4)根据反应物、生成物、反应条件及其质量守恒定律可以书写反应的化学方程式;
(5)根据图中提供的信息可以判断反应过程;
(6)一氧化碳和二氧化氮有毒,二氧化碳是一种重要的温室气体.
解答 解:(1)空气中氮气的体积分数约为78%.
故填:78%.
(2)控制温度在-183℃时,可将空气中N2与O2分离,因此要将产物NH3与N2、H2分离开来,温度应该控制在-33.35℃.
故填:-33.35.
(3)从空气中分离出氮气的过程中,没有生成新物质,属于物理变化,从含有氮气、氢气的混合物中分离出氨气的过程中,没有生成新物质,属于物理变化,从氨气中分离出氮气和氢气的过程中,没有生成新物质,属于物理变化;
由工艺流程可知,流程中能循环使用的物质是氮气、氢气.
故填:①④⑤;氮气、氢气.
(4)由N2、H2反应生成NH3的化学方程式为:N2+3H2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$2NH3.
故填:N2+3H2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$2NH3.
(5)符合在催化剂表面合成氨反应的顺序是:氮气和氢气混合,附着在催化剂表面,在催化剂作用下氮分子分解成氮原子,氢分子分解成氢原子,氮原子和氢原子结合生成氨分子,最后脱离催化剂,即顺序是⑤④①②③.
故填:⑤④①②③.
(6)一氧化碳和二氧化氮有毒,二氧化碳是一种重要的温室气体,因此下列物质排放到空气中,不会造成大气污染的是氮气.
故选:D.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

 如图是收集、吸收某气体的装置(A装置收集气体,B装置吸收多余气体).由实验装置推测该体的有关性质可能正确的是( )
如图是收集、吸收某气体的装置(A装置收集气体,B装置吸收多余气体).由实验装置推测该体的有关性质可能正确的是( )| A | B | C | D | |
| 密度比空气 | 小 | 小 | 大 | 大 |
| 溶于水中所得溶液的pH | >7 | <7 | >7 | <7 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 丙烷燃烧:C3H8+5O2$\frac{\underline{\;点燃\;}}{\;}$3CO2+4H2O | |
| B. | 铝的冶炼:2Al2O3$\frac{\underline{\;电解\;}}{\;}$4Al+3O2↑ | |
| C. | 湿法炼铜:Fe+CuSO4═Cu+FeSO4 | |
| D. | Cl-的检验:AgNO3+NaCl═NaNO3+AgCl↓ |
| A. | 一定含有碳、氢、氧三种元素 | |
| B. | 该物质的化学式为CH4. | |
| C. | 该物质的化学式量为46 | |
| D. | 该物质只含碳氢元素,且质量比为6:1 |
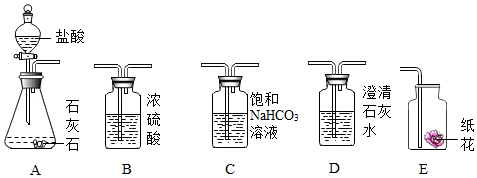
请根据实验装置和实验内容,回答下面问题:
①探究二氧化碳与碱反应时,将装置A生成的二氧化碳气体通入装置D未出现浑浊,原因是二氧化碳气体中混有氯化氢气体;可将二氧化碳先通过装置C,再通入装置D,理由是HCl+NaHCO3=NaCl+H2O+CO2↑(用化学方程式表示);
②探究二氧化碳与水反应时,实验分两步进行:首先将二氧化碳通过石蕊溶液浸泡的干燥纸花,再将二氧化碳通过石蕊溶液浸泡的湿润纸花,这样做的目的是通过对比实验,证明二氧化碳和水反应生成碳酸,碳酸能使紫色变红色;结合上面实验,装置正确的连接顺序是ACBE(填序号)
(2)家庭生活中食品制作(如面条、馒头等)经常用到食用碱,食用碱的主要成分是碳酸钠,可能含有少量氯化钠.小莉将家中食用碱带到实验室进行探究,请设计实验验证小莉提供的食用碱样品是否含有氯化钠.
| 实验步骤 | 实验现象 | 结论与解释 |
| 1.取一定量的食用碱样品放入试管,加入蒸馏水、振荡 | 样品溶解 | 食用碱溶于水 |
| 2.向食用碱溶液的试管中,滴加几滴硝酸银溶液,振荡 | 有白色沉淀生成 | 还需要证明白色沉淀不溶于稀硝酸 |
| 3.向白色沉淀中滴加稀硝酸 | 沉淀不溶解 | 证明食用碱样品中含有氯化钠 |
| A. | 浓硫酸 | B. | 大理石 | C. | 硝酸钾 | D. | 氧化铜 |