题目内容
6.下列实验装置常用于制取和收集气体.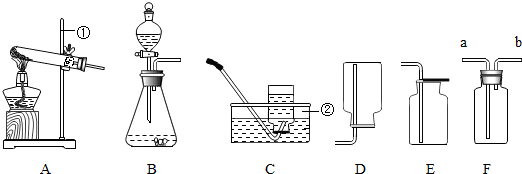
请回答下列问题:
(1)写出标号仪器的名称:①铁架台,②水槽;
(2)实验室加热高锰酸钾固体制取氧气的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,可选用的气体发生装置和收集装置分别是A和C(或E、F)(填字母序号);
(3)实验室制取二氧化碳气体常选用的两种药品是CaCO3、HCl(填化学式),可选用的气体发生装置是B(填字母序号),用装置F收集二氧化碳气体时应由a(填“a”或“b”)管口通入气体;
(4)将实验室制取的二氧化碳气体直接通入盛有蒸馏水的洗气瓶,一段时间后测得洗气瓶中溶液的pH<7,原因可能是二氧化碳与水反应生成酸(任答一点即可).
分析 (1)据常用仪器回答;
(2)据高锰酸钾分解的反应原理书写方程式,该反应需要加热,属于固体加热型,故选发生装置A,并结合氧气的密度和溶解性选择收集装置;
(3)实验室制取二氧化碳用 大理石和稀盐酸常温反应,属于固液常温型,故选发生装置B,二氧化碳密度比空气大,故应从长管进气;
(4)根据二氧化碳与水反应生成碳酸,碳酸的溶液显酸性分析解答.
解答 解:(1)编号仪器分别是固定仪器的铁架台和水槽;
(2)加热高锰酸钾生成锰酸钾、二氧化锰和氧气,反应方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;该反应需要加热,属于固体加热型,故选发生装置A,氧气密度比空气大,所以可用向上排空气法收集,不易溶于水,可用排水法收集;
(3)实验室制取二氧化碳用 大理石和稀盐酸常温反应,大理石的主要成分是碳酸钙,稀盐酸中参与反应的是盐酸,化学式分别是:CaCO3、HCl;属于固液常温型,故选发生装置B,二氧化碳密度比空气大,故应从长管进气,将空气挤压到集气瓶上部排出;
(4)二氧化碳与水反应生成碳酸,碳酸的溶液显酸性,所以将纯净的二氧化碳气体通入盛有蒸馏水的洗气瓶一段时间后,测得该装置中溶液的pH将小于7,;
故答案为:(1)铁架台;水槽;
(2)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;A;C(或E、F);
(3)CaCO3、HCl;B;a;
(4)二氧化碳与水反应生成酸.
点评 掌握实验室制取氧气的反应原理、装置选取方法,及二氧化碳的性质等知识,并能根据所学知识灵活分析和解答问题.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
16.在实际生活中,下列物质用途与其化学性质无关的是( )
| A. | 用稀盐酸除铁锈 | B. | 用钨做白炽灯泡的灯丝 | ||
| C. | 用熟石灰改良酸性土壤 | D. | 用纯碱发面蒸馒头 |
17.正确的实验操作是科学探究成功的基础.下列实验操作正确的是( )
| A. |  读出液体体积 | B. |  铁丝在氧气中燃烧 | ||
| C. |  除去CO中的CO2 | D. |  滴管的使用 |
14.关于化学式“SO2”的叙述不正确的是( )
| A. | 表示二氧化硫这种物质 | |
| B. | 表示二氧化硫由1个硫元素和2个氧元素组成 | |
| C. | 表示一个二氧化硫分子 | |
| D. | 表示一个二氧化硫分子由2个氧原子和1个硫原子构成 |
1.下列不利于人体健康的是( )
| A. | 食用地沟油炼制的“食用油” | B. | 食用新鲜的蔬菜水果 | ||
| C. | 食用加铁酱油 | D. | 食用清淡低盐的菜肴 |