题目内容
15.我省是产煤大省,煤炭资源丰富.(1)如果煤的含硫较高,大量使用原煤作燃料会产生一种能严重污染大气的有毒气体是SO2(填化学式)
(2)与煤相比,天然气是一种比较清洁的化石燃料,其主要成分是甲烷,它燃烧的化学方程式为:CH4+2O2 $\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O
(3)化石燃料是国家的重要资源,它通常指煤石油和天然气.为提高化石燃料的利用率,可采取的方法是①足量的氧气,②可燃物与氧气接触.
分析 (1)煤中主要含有碳元素,还含有少量的硫元素,不完全燃烧时会产生大量的一氧化碳、二氧化硫和烟尘等物质;
(2)甲烷燃烧能生成二氧化碳和水解答;
(3)根据已有的知识进行分析,煤、石油、天然气属于化石燃料,根据化石燃料的性质可以判断化石燃料的组成等方面的情况解答.
解答 解:
(1)硫和氧气反应能生成二氧化硫,碳不完全燃烧时能生成一氧化碳,二氧化硫和一氧化碳都是污染环境的物质.
(2)天然气的成分是甲烷,燃烧生成二氧化碳和水,故填:CH4+2O2 $\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;
(3)煤、石油、天然气属于化石燃料.为提高化石燃料的利用率,可采取的方法是足量的氧气,可燃物与氧气接触.
答案:
(1)SO2;
(2)CH4+2O2 $\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;
(3)石油;①足量的氧气;②可燃物与氧气接触.
点评 解答本题要充分理解含硫煤在氧气不足的情况下燃烧时的生成物的性质,只有这样才能对相关方面的问题做出正确的判断.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
10.下列物质中属于纯净物的是( )
| A. | 冰红茶 | B. | 洁净的空气 | C. | 白酒 | D. | 蒸馏水 |
20.发现元素周期律并编制出元素周期表的是( )
| A. | 道尔顿和阿伏伽德罗 | B. | 拉瓦锡 | ||
| C. | 门捷列夫 | D. | 牛顿 |
7.某兴趣小组设计实验探究碳酸钠、碳酸氢钠与盐酸反应过程中的放、吸热情况.操作步骤为:①向试剂1中加入试剂2,搅拌、测温;②静置、测温;③再加入试剂3,搅拌、测温、记录.得到了如下数据:
则下列说法中,错误的是( )
| 试剂1 | 试剂2 温度/℃ | 溶解后 温度/℃ | 静置后 温度/℃ | 试剂3 温度/℃ | 混合后 温度/℃ |
| 0.5g Na2CO3 | 10mL H2O 20.0 | 23.3 | 20.0 | 10mL HCl(20%) 20.0 | 23.7 |
| 0.5g NaHCO3 | 10mL H2O 20.0 | 18.5 | 20.0 | 10mL HCl(20%) 20.0 | 20.8 |
| A. | Na2CO3在溶于水的过程中以放热为主 | |
| B. | NaHCO3在溶于水的过程中以放热为主 | |
| C. | 其它条件相同时,碳酸氢钠溶液与盐酸混合过程中放出的热量更多 | |
| D. | 其它条件相同时,碳酸钠溶液与盐酸混合过程中放出的热量更多 |
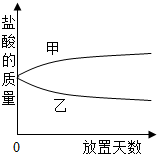 将一定质量的浓盐酸盛于烧杯中,敞口放置在实验室安全之处.
将一定质量的浓盐酸盛于烧杯中,敞口放置在实验室安全之处.