题目内容
20. 地质博物馆中有许多矿石标本,其中的3种矿石如图所示:
地质博物馆中有许多矿石标本,其中的3种矿石如图所示:(1)白钨矿的主要成分中钨元素的化合价为+6.
(2)黄铜矿的主要成分中,属于非金属元素的是S.
(3)上述三种矿石中的黄铜矿和辉铜矿可用作冶炼金属铜的原料,其原因是都含有铜元素.
分析 (1)根据在化合物中正负化合价代数和为零进行解答;
(2)黄铜矿的主要成分中,属于非金属元素的是硫元素;
(3)上述三种矿石中的黄铜矿和辉铜矿可用作冶炼金属铜的原料,其原因是都含有铜元素.
解答 解:(1)已知钙元素的化合价为+2价,氧元素的化合价为-2价,设CaWO4中钨元素(W)的化合价为x,根据化合价的原则(在化合物中正、负化合价的代数和为零),则(+2)+x+(-2)×4=0,解得x=+6,故CaWO4中钨元素(W)的化合价是+6价;
故填:+6;
(2)黄铜矿的主要成分中,属于非金属元素的是硫元素;
故填:S;
(3)上述三种矿石中的黄铜矿和辉铜矿可用作冶炼金属铜的原料,其原因是都含有铜元素;
故填:都含有铜元素.
点评 本题考查的内容较多,主要化合价的计算、质量守恒定律,难度不大.

练习册系列答案
相关题目
10. 阅读下面科普短文(原文作者:许谦,有删改)
阅读下面科普短文(原文作者:许谦,有删改)
酸奶口感酸甜,营养丰富,是深受人们喜爱的一种乳制品.与普通牛奶比较,酸奶中的蛋白质和钙更易被人体消化吸收,是乳糖不耐症患者的良好食品.
通常的酸奶是将牛奶发酵而制成的.牛奶中主要含有蛋白质、乳糖和脂肪.在发酵过程中,乳酸菌把乳糖(C12H22O11)转化成乳酸(C3H6O3),使得牛奶的酸度升高.随着酸度增加,蛋白质分子互相连接,形成了一个巨大的“网络”,这个“蛋白质网络”把乳糖、水、脂肪颗粒都“网”在其中.所以,奶变“粘”、变“酸”了.
酸奶中含有大量活力较强的乳酸菌.乳酸菌可抑制某些腐败菌和病原菌的繁殖,从而维持人体内,尤其是肠道内正常的微生态平衡,促进食物的消化吸收.酸奶在储藏和配送过程中,乳酸菌的数量会因乳酸的过量积聚而明显减少,而酸奶的乳酸积聚又会影响到酸奶的酸度.有研究者选取某种市面常见的酸奶进行实验,数据如下表所示.
表 某品牌酸奶酸度的变化
1999年颁布的国标GB2746-1999中,对成品酸奶的酸度规定为“酸度不小于70°T”.按照一般人的接受程度,酸奶酸度不能超过100°T.
依据文章内容回答下列问题.
(1)乳酸是由乳糖转化生成的,请比较二者的化学式,分析它们的相同点和不同点.
相同点:组成元素的种类相同(或原子种类相同).
不同点:各元素的质量比不同(或原子个数比不同).
(2)实验中所用酸奶若在37℃条件下储存,D天后,酸度一定会超出一般人的接受程度.(填字母序号,下同)
A.2 B.4 C.5 D.8
(3)由表中实验数据可知,影响酸奶酸度的因素有温度、时间.
(4)下列关于酸奶的说法正确的是AD.
A.酸奶适用于乳糖不耐症患者食用
B.酸奶放置时间越长,乳酸菌含量越高
C.酸奶中的乳酸菌对人类身体有害无益
D.酸奶变“粘”与蛋白质分子相互连接形成巨大“网络”有关.
 阅读下面科普短文(原文作者:许谦,有删改)
阅读下面科普短文(原文作者:许谦,有删改)酸奶口感酸甜,营养丰富,是深受人们喜爱的一种乳制品.与普通牛奶比较,酸奶中的蛋白质和钙更易被人体消化吸收,是乳糖不耐症患者的良好食品.
通常的酸奶是将牛奶发酵而制成的.牛奶中主要含有蛋白质、乳糖和脂肪.在发酵过程中,乳酸菌把乳糖(C12H22O11)转化成乳酸(C3H6O3),使得牛奶的酸度升高.随着酸度增加,蛋白质分子互相连接,形成了一个巨大的“网络”,这个“蛋白质网络”把乳糖、水、脂肪颗粒都“网”在其中.所以,奶变“粘”、变“酸”了.
酸奶中含有大量活力较强的乳酸菌.乳酸菌可抑制某些腐败菌和病原菌的繁殖,从而维持人体内,尤其是肠道内正常的微生态平衡,促进食物的消化吸收.酸奶在储藏和配送过程中,乳酸菌的数量会因乳酸的过量积聚而明显减少,而酸奶的乳酸积聚又会影响到酸奶的酸度.有研究者选取某种市面常见的酸奶进行实验,数据如下表所示.
表 某品牌酸奶酸度的变化
| 温度/℃ 时间/天 酸度/°T | 4 | 28 | 37 |
| 0 | 67.7 | 67.7 | 67.7 |
| 2 | 73.9 | 77.1 | 79.2 |
| 4 | 76.4 | 82.7 | 86.3 |
| 6 | 85.5 | 92.2 | 98.9 |
| 8 | 90.2 | 98.7 | 113.2 |
依据文章内容回答下列问题.
(1)乳酸是由乳糖转化生成的,请比较二者的化学式,分析它们的相同点和不同点.
相同点:组成元素的种类相同(或原子种类相同).
不同点:各元素的质量比不同(或原子个数比不同).
(2)实验中所用酸奶若在37℃条件下储存,D天后,酸度一定会超出一般人的接受程度.(填字母序号,下同)
A.2 B.4 C.5 D.8
(3)由表中实验数据可知,影响酸奶酸度的因素有温度、时间.
(4)下列关于酸奶的说法正确的是AD.
A.酸奶适用于乳糖不耐症患者食用
B.酸奶放置时间越长,乳酸菌含量越高
C.酸奶中的乳酸菌对人类身体有害无益
D.酸奶变“粘”与蛋白质分子相互连接形成巨大“网络”有关.
11.鱼类食物富含铁,此处“铁”指的是( )
| A. | 元素 | B. | 原子 | C. | 分子 | D. | 单质 |
8.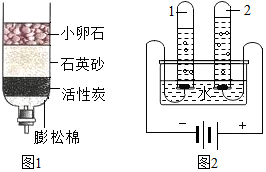 水是地球上一种最普通、最常见的物质.
水是地球上一种最普通、最常见的物质.
①图1所示的是简易净水器,其中活性炭的作用是过滤和吸附.
②水厂处理水时,有时会向水中加生石灰,此过程中发生的化学方程式为CaO+H2O═Ca(OH)2.
③图2是电解水的简易装置,试管1中生成的气体是氢气,反应的化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
④将少量下面的调味品加入水中,不能形成溶液的是D.
A.食盐B.蔗糖C.味精D.芝麻油
⑤碘酒中的溶剂为酒精(质名称)
⑥在一定温度下,向质量均为50g的4份水中分别加入一定量的KNO3固体,搅拌至充分溶解,(如有不溶的KNO3固体用过滤的方法除去),得到溶液.加入KNO3固体的质量与所得溶液的质量如下表:
①实验a、b、c、d中,有未被溶解的KNO3固体析出的实验是d(填写实验编号).
②该温度下KNO3的溶解度是110g.
③实验a、b、c、d所得溶液中质量分数大小关系为:a<b<c=d.
④取实验b所得溶液,若使其质量分数变为20%,在不改变温度的情况下,可以采取的操作是加入150g水.
 水是地球上一种最普通、最常见的物质.
水是地球上一种最普通、最常见的物质.①图1所示的是简易净水器,其中活性炭的作用是过滤和吸附.
②水厂处理水时,有时会向水中加生石灰,此过程中发生的化学方程式为CaO+H2O═Ca(OH)2.
③图2是电解水的简易装置,试管1中生成的气体是氢气,反应的化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
④将少量下面的调味品加入水中,不能形成溶液的是D.
A.食盐B.蔗糖C.味精D.芝麻油
⑤碘酒中的溶剂为酒精(质名称)
⑥在一定温度下,向质量均为50g的4份水中分别加入一定量的KNO3固体,搅拌至充分溶解,(如有不溶的KNO3固体用过滤的方法除去),得到溶液.加入KNO3固体的质量与所得溶液的质量如下表:
| 实验编号 | a | b | c | d |
| 加入KNO3固体的质量 | 45 | 50 | 55 | 60 |
| 所得溶液的质量 | 95 | 100 | 105 | 105 |
②该温度下KNO3的溶解度是110g.
③实验a、b、c、d所得溶液中质量分数大小关系为:a<b<c=d.
④取实验b所得溶液,若使其质量分数变为20%,在不改变温度的情况下,可以采取的操作是加入150g水.
15.图示的四个图象分别对应四个变化过程的一种趋势,下列分析正确的是( )
| A. | 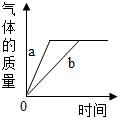 可能是双氧水溶液制氧气,a未使用催化剂,b使用了催化剂 | |
| B. | 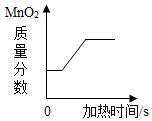 可能是加热一定质量的氯酸钾和二氧化锰固体混合物制取氧气过程 | |
| C. | 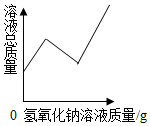 可能是硫酸铜溶液中滴加氢氧化钠溶液 | |
| D. | 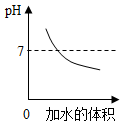 可能是向一定量的氢氧化钠溶液中加水稀释,溶液的pH变化 |
9. 合理运用燃烧与灭火的化学原理对保障生命财产安全非常重要.
合理运用燃烧与灭火的化学原理对保障生命财产安全非常重要.
(1)高层建筑物通常设计了灭火用的洒水系统.从灭火原理分析,洒水的作用主要是降低温度到可燃物着火点以下.
(2)分析下表中的数据,回答问题:
①有人认为“物质的熔、沸点越高,着火点越高”,该结论不合理(填“合理”或“不合理”).
②已知酒精灯火焰的温度约为500℃.利用如图装置,验证达到可燃物着火点是燃 烧的条件之一,上表中可用于完成该实验的两种可燃物是M和L或M和P(填代号).
 合理运用燃烧与灭火的化学原理对保障生命财产安全非常重要.
合理运用燃烧与灭火的化学原理对保障生命财产安全非常重要.(1)高层建筑物通常设计了灭火用的洒水系统.从灭火原理分析,洒水的作用主要是降低温度到可燃物着火点以下.
(2)分析下表中的数据,回答问题:
| 物质代号 | L | M | N | P |
| 熔点/℃ | -117 | 3550 | 44 | -259 |
| 沸点/℃ | 78 | 4827 | 257 | -253 |
| 着火点/℃ | 510 | 370 | 40 | 580 |
②已知酒精灯火焰的温度约为500℃.利用如图装置,验证达到可燃物着火点是燃 烧的条件之一,上表中可用于完成该实验的两种可燃物是M和L或M和P(填代号).
 用如图所示装置研究白磷和氧气的反应,装置中试管内液面与试管外相平.
用如图所示装置研究白磷和氧气的反应,装置中试管内液面与试管外相平. 阅读下面科普短文(原文作者高存文、王晶禹,原文有删改).
阅读下面科普短文(原文作者高存文、王晶禹,原文有删改). 实验室制取氧气时,某同学取一定质量的高锰酸钾加热,记录产生氧气的质量与反应时间的关系如图1所示,请回答下列问题:
实验室制取氧气时,某同学取一定质量的高锰酸钾加热,记录产生氧气的质量与反应时间的关系如图1所示,请回答下列问题: