题目内容
1.黄铜是一种重要的金属,它是铜和锌的合金,可用来制造机器、电器零件及日常用品.为了测定黄铜样品的组成,取五份样品分别加稀硫酸反应,其实验数据记录如下:| 样品 | 第1份 | 第2份 | 第3份 | 第4份 | 第5份 |
| 取样品质量(g) | 40.0 | 40.0 | 40.0 | 40.0 | 40.0 |
| 取稀硫酸质量(g) | 30.0 | 60.0 | 90.0 | 120.0 | 150.0 |
| 产生气体质量(g) | 0.3 | m | 0.9 | 1.0 | n |
(1)根据实验数据分析,表中m的数值为0.6,n的数值应该为1.0;
(2)第1、2、3份,硫酸已经反应完全了.
(3)列式计算该黄铜样品中金属锌的质量分数.(要求写出计算过程)
分析 (1)根据取样品都是40g时,硫酸质量是30g时,生成氢气0.3g,硫酸是90g时,生成氢气是0.9g,所以硫酸是60g时,生成氢气是0.6g,硫酸是120g时,生成氢气1.0g,所以硫酸是150g时,生成的氢气也是1.0g进行分析;
(2)根据前3份反应中硫酸和氢气成正比,第4份加入120g硫酸生成氢气1.0g,与前3份中的数值不成正比,说明前三份中的硫酸完全反应进行分析;
(3)
解答 解:(1)取样品都是40g时,硫酸质量是30g时,生成氢气0.3g,硫酸是90g时,生成氢气是0.9g,所以硫酸是60g时,生成氢气是0.6g,硫酸是120g时,生成氢气1.0g,所以硫酸是150g时,生成的氢气也是1.0g,所以表中m的数值为0.6,n的数值应该为1.0;
(2)前3份反应中硫酸和氢气成正比,第4份加入120g硫酸生成氢气1.0g,与前3份中的数值不成正比,说明前三份中的硫酸完全反应;
(3)设40g样品中含锌的质量为x
Zn+H2SO4=ZnSO4+H2↑
65 2
x 1.0g
$\frac{65}{x}$=$\frac{2}{0.1g}$
x=32.5g
所以黄铜样品中锌的质量分数为:$\frac{32.5g}{40g}$×100%=81.25%.
答:黄铜样品中锌的质量分数为81.25%.
故答案为:(1)0.6,1.0;
(2)1,2,3;
(3)81.25%.
点评 解答本题关键是要通过图表中数据分析出最多生成氢气1.0g,再利用方程式计算出锌的质量,再进一步进行计算.

练习册系列答案
相关题目
5.重铬酸钾(K2Cr2O7)可用于测定酒驾中的酒精含量,K2Cr2O7中Cr元素化合价为( )
| A. | +7 | B. | +6 | C. | +4 | D. | -6 |
12.下列现象或事实,用分子、原子的相关知识加以解释,其中不正确的是( )
| 选项 | 现象或事实 | 解释 |
| A | 稀有气体可作保护气 | 原子核外电子达到相对稳定结构 |
| B | 物质热胀冷缩 | 分子大小随温度改变而改变 |
| C | 氧气和臭氧(O3)性质不完全相同 | 构成物质的分子不同 |
| D | 氧化汞受热分解为汞和氧气 | 在化学变化中分子可以再分 |
| A. | A | B. | B | C. | C | D. | D |
9.新的一年,同学们的学习方式有了很大变化.下面是《气体制取与收集》学习的课堂片段:
【自主学习】仿照氧气制取的学习和气体制取的一般思路,阅读课本,老师提供了几组药品,让同学们交流并选出适宜实验室制取二氧化碳的一组.
【合作交流】围绕以上问题,各小组展开了激烈的交流,下面是老师从第二小组同学交流中听到的各位学生的发言:
1号:碳酸盐用块状石灰石(主要成分碳酸钙),为什么不用纯碱(碳酸钠)呢?
3号:碳酸钠是粉未状的,反应的速度太快,不易控制,
2号:同意3号同学的说法,那我们把碳酸钠压制成块状可以吗?
各位都在思考,问题未能解决.
【展示释疑】通过各个小组的展示,大家明白了实验室制取二氧化碳应该选择石灰石和稀盐酸.
实际实验中,所用的原料或产物一般都含有杂质,在计算用料和产量时,应考虑到杂质问题.
请你帮助二组学生解决2号学生提出的问题,实验室把碳酸钠压制成块状不可以(选填“可以”或“不可以”)代替石灰石制取二氧化碳.
【能力提升】某小组想测定所用石灰石样品中碳酸钙的质量分数,取用了2g的石灰石样品,把20g稀盐酸(氯化氢的水溶液)分4次加入样品中,(样品中除碳酸钙外,其余成分既不与盐酸反应,也不溶解于水),充分反应后经过滤、干燥等操作,最后称量,得实验数据如下:
(1)从以上数据可知,这四次实验中,第四次石灰石样品中碳酸钙已完全反应.
(2)求石灰石中碳酸钙的质量分数?
(3)求检测过程中所产生二氧化碳的质量?
【自主学习】仿照氧气制取的学习和气体制取的一般思路,阅读课本,老师提供了几组药品,让同学们交流并选出适宜实验室制取二氧化碳的一组.
【合作交流】围绕以上问题,各小组展开了激烈的交流,下面是老师从第二小组同学交流中听到的各位学生的发言:
1号:碳酸盐用块状石灰石(主要成分碳酸钙),为什么不用纯碱(碳酸钠)呢?
3号:碳酸钠是粉未状的,反应的速度太快,不易控制,
2号:同意3号同学的说法,那我们把碳酸钠压制成块状可以吗?
各位都在思考,问题未能解决.
【展示释疑】通过各个小组的展示,大家明白了实验室制取二氧化碳应该选择石灰石和稀盐酸.
实际实验中,所用的原料或产物一般都含有杂质,在计算用料和产量时,应考虑到杂质问题.
请你帮助二组学生解决2号学生提出的问题,实验室把碳酸钠压制成块状不可以(选填“可以”或“不可以”)代替石灰石制取二氧化碳.
【能力提升】某小组想测定所用石灰石样品中碳酸钙的质量分数,取用了2g的石灰石样品,把20g稀盐酸(氯化氢的水溶液)分4次加入样品中,(样品中除碳酸钙外,其余成分既不与盐酸反应,也不溶解于水),充分反应后经过滤、干燥等操作,最后称量,得实验数据如下:
| 稀盐酸的用量 | 剩余固体的质量 |
| 第一次加入5g | 1.5g |
| 第二次加入5g | 1.0g |
| 第三次加入5g | 0.5g |
| 第四次加入5g | 0.3g |
(2)求石灰石中碳酸钙的质量分数?
(3)求检测过程中所产生二氧化碳的质量?
16.下列实验项目所选择的仪器错误的是( )
| A. | 较多量液体加热--烧杯 | B. | 盛放固体药品--细口瓶 | ||
| C. | 少量试剂的反应--试管 | D. | 吸取和滴加少量液体--胶头滴管 |
6.下列实验操作正确的是( )
| A. | 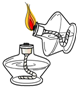 | B. | 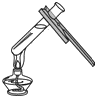 | C. | 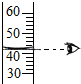 | D. | 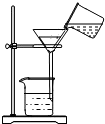 |
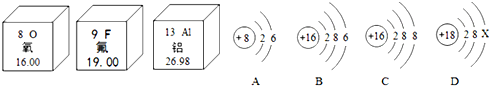
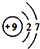 ,氟原子在化学反应中易得到(填“得到”或
,氟原子在化学反应中易得到(填“得到”或