题目内容
8.现有两种金属组成的混合物,在5.6g该混合物中加入100g一定溶质质量分数的稀盐酸,两者恰好完全反应,产生氢气的质量为m.下列说法正确的是( )①若混合物为Fe、Al,m可能是0.3g
②若混合物为Fe、Cu,m可能是0.1g
③若混合物为Fe、Zn,m可能是0.15g
④若混合物为Fe、Al,则稀盐酸中溶质质量分数一定大于7.3%
| A. | ①②③ | B. | ②③ | C. | ①②④ | D. | ①③ |
分析 铁和稀盐酸反应生成氯化亚铁和氢气,铝和稀盐酸反应生成氯化铝和氢气,锌和稀盐酸反应生成氯化锌和氢气,铜不能和稀盐酸反应.
解答 解:铁、铝、锌和稀盐酸反应的化学方程式及其质量关系为:
Fe+2HCl═FeCl2+H2↑,2Al+6HCl═2AlCl3+3H2↑,Zn+2HCl═ZnCl2+H2↑,
56 2 54 6 65 2
①若混合物为Fe、Al,则生成氢气的质量大于0.2g,m可能是0.3g;
②若混合物为Fe、Cu,则生成氢气的质量小于0.2g,m可能是0.1g;
③若混合物为Fe、Zn,如果都是铁,生成氢气的质量是0.2g,如果都是锌,生成氢气的质量是0.17g,则生成氢气的质量大于0.17g,m不可能是0.15g;
④若混合物为Fe、Al,都是铁时,消耗的氯化氢质量是7.3g,都是铝时,消耗的氯化氢质量大于7.3g,如果是铁和铝的混合物,则稀盐酸中溶质质量分数一定大于7.3%.
故选:C.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
18.某同学为了测定氯化钠和氯化镁固体混合物中氯化镁的质量分数进行如下实验:将80g固体混合物溶于水配成溶液,平均分成四份,分别加入相同质量分数的氢氧化钠溶液,获得如表实验数据:
(1)表中m的值为5.8.
(2)原固体混合物中氯化镁的质量分数是多少?
| 实验次数 | 一 | 二 | 三 | 四 |
| 固体混合物的质量(g) | 20 | 20 | 20 | 20 |
| 加入氢氧化钠溶液的质量(g) | 20 | 40 | 60 | 80 |
| 生成沉淀的质量(g) | 2.9 | m | 8.7 | 8.7 |
(2)原固体混合物中氯化镁的质量分数是多少?
19.生活在一些常见液体的pH值如下,其中酸性最强的是( )
| A. | 玉米粥6.8 | B. | 橙汁3.5 | C. | 肥皂水11 | D. | 洗发露7.6 |
3.物质在不断运动变化着,属于物理变化的是( )
| A. | 鸡蛋清中加入硫酸铜溶液“凝固” | |
| B. | 打开浓盐酸瓶口“冒白雾” | |
| C. | 全毛绒线放入氢氧化钠溶液中“溶解” | |
| D. | 氢氧化钠溶液中滴入酚酞“变化” |
13.现有一种碱性调味液,是碳酸钠和氯化钠组成的溶液,为了测定该碱性调味液中碳酸钠的质量分数,设计了如下实验:
取三份碱性调味液各100g,分别缓慢加入到20g、40g和60g某稀盐酸中,测得三组实验数据如表(气体的溶解忽略不计)
根据实验及有关数据进行分析与计算
(1)100g碱性调味液与该稀盐酸完全反应生成气体的质量为5.5g
(2)与100g碱性调味液恰好完全反应的稀盐酸的质量为50g,所用稀盐酸溶质的质量分数为多少?
(3)碱性调味液中碳酸钠的质量分数为多少?
取三份碱性调味液各100g,分别缓慢加入到20g、40g和60g某稀盐酸中,测得三组实验数据如表(气体的溶解忽略不计)
| 第Ⅰ组 | 第Ⅱ组 | 第Ⅲ组 | |
| 稀盐酸的质量/g | 20 | 40 | 60 |
| 生成气体的质量/g | 2.2 | 4.4 | 5.5 |
(1)100g碱性调味液与该稀盐酸完全反应生成气体的质量为5.5g
(2)与100g碱性调味液恰好完全反应的稀盐酸的质量为50g,所用稀盐酸溶质的质量分数为多少?
(3)碱性调味液中碳酸钠的质量分数为多少?
20.下列物质鉴别的方法错误的是( )
| A. | 区别二氧化碳、氧气和空气--分别将燃着的木条伸入瓶中,观察现象 | |
| B. | 区别过氧化氢和蒸馏水--加入MnO2,看是否有气泡 | |
| C. | 区别硬水与软水--常用肥皂水检验,泡沫减少产生浮渣的是硬水 | |
| D. | 区别二氧化锰和氧化铜--观察颜色 |
17.下列关于碳的单质和氧化物的组成、性质和用途的说法中,错误的是( )
| A. | 璀璨夺目的天然钻石和黑乎乎的碳粉外观差异很大,但它们都是由碳元素组成的 | |
| B. | 长期未用而难开启的铁锁,可在锁孔中加入少量铅笔芯粉末作润滑剂 | |
| C. | 干冰用于人工降雨和制冷剂,是利用其化学性质 | |
| D. | 可用活性炭除去糖浆里的色素,这是利用它的物理性质--吸附性 |
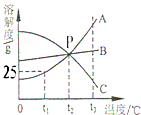 如图为A、B、C三种物质的溶解度曲线,据图回答:
如图为A、B、C三种物质的溶解度曲线,据图回答: