题目内容
13.小华测定Cu-Zn合金及Cu-Ag合金中铜的质量分数,实验室只提供一瓶稀硫酸和必要的仪器.(1)你认为能测量出铜的质量分数的是Cu-Zn合金.
(2)小华取该合金的粉末65g与100g稀硫酸溶液恰好完全反应产生氢气0.4g,该合金中铜的质量分数是多少?
(3)小华所用稀硫酸溶液中溶质的质量分数为多少?
分析 铜、银不能和稀硫酸反应,锌和稀硫酸反应生成硫酸锌和氢气,根据反应的化学方程式和提供的数据可以进行相关方面的计算和判断.
解答 解:(1)因为锌能和稀硫酸反应,因此能测量出铜的质量分数的是Cu-Zn合金.
故填:Cu-Zn.
(2)设锌的质量为x,反应的硫酸质量为y,
Zn+H2SO4═ZnSO4+H2↑,
65 98 2
x y 0.4g
$\frac{65}{x}$=$\frac{98}{y}$=$\frac{2}{0.4g}$,
x=13g,y=19.6g,
该合金中铜的质量分数是:$\frac{65g-13g}{65g}$×100%=80%,
答:该合金中铜的质量分数是80%.
(3)小华所用稀硫酸溶液中溶质的质量分数为:$\frac{19.6g}{100g}$×100%=19.6%,
答:小华所用稀硫酸溶液中溶质的质量分数为19.6%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.下列曲线图与实验事实相一致的是( )
| A. |  向一定体积HCl溶液中滴加NaOH溶液 | |
| B. | 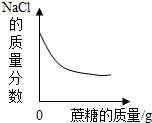 一定温度下,向一定量饱和NaCl溶液中不断加入蔗糖 | |
| C. | 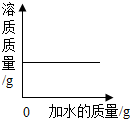 向饱和NaCl溶液中不断加水 | |
| D. |  向CuCl2和H2SO4的混合溶液中加入过量Ba(OH)2溶液 |
5. 化学调研小组的同学用氢氧化钠和稀盐酸探究中和反应,请你参与以下探究:
化学调研小组的同学用氢氧化钠和稀盐酸探究中和反应,请你参与以下探究:
(1)甲组同学取少量的氢氧化钠溶液于烧杯中,用酸度计测得该溶液的pH>(选填“<”、“>”或“=”)7,同时插入一支温度计,测量溶液的温度(如图所示).用胶头滴管吸取稀盐酸,逐滴加入盛有氢氧化钠溶液的烧杯中,边滴加边搅拌.此时可观察到的现象是:酸度计上显示的数据逐渐减少(选填“增大”、“减少”或“不变”,下同),温度计上显示的数据逐渐增大.由此可知,酸和碱的中和反应属于放热(选填“吸热”或“放热”)反应.
(2)乙组的同学改用固体氢氧化钠与稀盐酸反应来探究中和反应中能量的变化情况,你认为该方案合不合理,理由是不合理,氢氧化钠固体溶于水时也放热.
(3)丙组同学用另外一瓶氢氧化钠溶液进行实验时,当往烧杯中滴加稀盐酸时,发现有少量的气泡冒出,小组同学讨论后一致认为其原因可能是氢氧化钠溶液已经变质,为了除去氢氧化钠溶液中变质产生的碳酸钠,你认为可选用下列物质中的B(填序号).
A.稀盐酸 B.氢氧化钙溶液 C.氯化钙溶液 D.氯化钠溶液
(4)丁组同学借助酚酞试液来判断氢氧化钠溶液与稀盐酸发生中和反应时,向烧杯中的氢氧化钠溶液中滴加稀盐酸一会儿后,发现忘记了滴加酚酞试液.为了确定盐酸与氢氧化钠是否恰好完全反应,小组的同学从烧杯中取少量反应后的溶液于一支试管中,并向试管中滴加几滴酚酞试液,振荡,观察到酚酞试液不变色.于是他们得出了“两种物质已恰好完全中和”的结论.你认为他们得出的结论是否正确?理由是:否,当盐酸过量时,酚酞也不变色.
请你帮助该小组同学设计一个实验,探究上述烧杯中的溶液是否恰好完全中和,填写下表:
(5)实验室现有一瓶久置的20%的氢氧化钠溶液100g.某同学取该溶液的1/10于锥形瓶中,滴加1-2滴酚酞试液,然后滴入稀盐酸,边加边振荡.当反应恰好完全时,用去稀盐酸的体积为17.40mL.已知:常温下,所用稀盐酸的密度为1.05g/cm3.
计算所用稀盐酸的溶质质量分数.(计算结果精确到1%)
 化学调研小组的同学用氢氧化钠和稀盐酸探究中和反应,请你参与以下探究:
化学调研小组的同学用氢氧化钠和稀盐酸探究中和反应,请你参与以下探究:(1)甲组同学取少量的氢氧化钠溶液于烧杯中,用酸度计测得该溶液的pH>(选填“<”、“>”或“=”)7,同时插入一支温度计,测量溶液的温度(如图所示).用胶头滴管吸取稀盐酸,逐滴加入盛有氢氧化钠溶液的烧杯中,边滴加边搅拌.此时可观察到的现象是:酸度计上显示的数据逐渐减少(选填“增大”、“减少”或“不变”,下同),温度计上显示的数据逐渐增大.由此可知,酸和碱的中和反应属于放热(选填“吸热”或“放热”)反应.
(2)乙组的同学改用固体氢氧化钠与稀盐酸反应来探究中和反应中能量的变化情况,你认为该方案合不合理,理由是不合理,氢氧化钠固体溶于水时也放热.
(3)丙组同学用另外一瓶氢氧化钠溶液进行实验时,当往烧杯中滴加稀盐酸时,发现有少量的气泡冒出,小组同学讨论后一致认为其原因可能是氢氧化钠溶液已经变质,为了除去氢氧化钠溶液中变质产生的碳酸钠,你认为可选用下列物质中的B(填序号).
A.稀盐酸 B.氢氧化钙溶液 C.氯化钙溶液 D.氯化钠溶液
(4)丁组同学借助酚酞试液来判断氢氧化钠溶液与稀盐酸发生中和反应时,向烧杯中的氢氧化钠溶液中滴加稀盐酸一会儿后,发现忘记了滴加酚酞试液.为了确定盐酸与氢氧化钠是否恰好完全反应,小组的同学从烧杯中取少量反应后的溶液于一支试管中,并向试管中滴加几滴酚酞试液,振荡,观察到酚酞试液不变色.于是他们得出了“两种物质已恰好完全中和”的结论.你认为他们得出的结论是否正确?理由是:否,当盐酸过量时,酚酞也不变色.
请你帮助该小组同学设计一个实验,探究上述烧杯中的溶液是否恰好完全中和,填写下表:
| 实验方法 | 可能观察到的现象 | 结论 |
计算所用稀盐酸的溶质质量分数.(计算结果精确到1%)
6. 一定质量的镁条在氧气中完全燃烧后生成氧化镁.固体质量随时间的变化关系如图所示.下列说法不正确的是( )
一定质量的镁条在氧气中完全燃烧后生成氧化镁.固体质量随时间的变化关系如图所示.下列说法不正确的是( )
 一定质量的镁条在氧气中完全燃烧后生成氧化镁.固体质量随时间的变化关系如图所示.下列说法不正确的是( )
一定质量的镁条在氧气中完全燃烧后生成氧化镁.固体质量随时间的变化关系如图所示.下列说法不正确的是( )| A. | 生成MgO的质量:m2g | |
| B. | 参加反应的Mg的质量:m1 g | |
| C. | 参加反应的O2的质量:(m2-m1)g | |
| D. | 参加反应的镁和氧气的质量比:m1:(m2-m1)=3:1 |
 钙是维持人体正常功能所必需的元素.如图所示为“迪巧”钙片说明书的一部分.取5片钙片,放入 有50g稀盐酸的烧杯中,其中碳酸钙跟盐酸恰好完全反应(其它成分与盐酸不反应).烧杯内物质质量变为57.8g.试计算:
钙是维持人体正常功能所必需的元素.如图所示为“迪巧”钙片说明书的一部分.取5片钙片,放入 有50g稀盐酸的烧杯中,其中碳酸钙跟盐酸恰好完全反应(其它成分与盐酸不反应).烧杯内物质质量变为57.8g.试计算: