题目内容
2.请写出符合下列要求的物质的化学用语:(1)2个镁离子2Mg2+;
(2)人体内含量最多的金属元素Ca;
(3)造成温室效应的单质O3;
(4)实验室常用的液体燃料C2H5OH.
分析 本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式,才能熟练准确的解答此类题目.
解答 解:(1)离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字,故2个镁离子可表示为:2Mg2+;
(2)人体内含量最多的金属元素是钙元素,其符号为:Ca;
(3)造成温室效应的单质是臭氧,其化学式为:O3;
(4)实验室常用的液体燃料是酒精,其化学式为:C2H5OH;
故答案为:(1)2Mg2+ (2)Ca (3)O3 (4)C2H5OH
点评 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础,题目难度较易.

练习册系列答案
相关题目
10.Fe2O3、FeO、Fe3O4的固体混合粉末10.00g,在加热条件下用足量CO还原,得到金属铁ag,将生成的CO2气体用足量的澄清石灰水吸收后,产生15.00g白色沉淀,则a的数值为( )
| A. | 7.24 | B. | 7.60 | C. | 5.20 | D. | 7.80 |
17.下列变化中一定含有化学变化的是( )
| A. | 蒸馏净水 | B. | 海水晒盐 | C. | 高炉炼铁 | D. | 石蜡熔化 |
7. 某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.
某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.
(1)请写出镁条与氧气反应的化学方程式2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO.
(2)小明发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵守质量守恒定律.我不同意 (“同意”或“不同意”)小明的观点.
(3)小红按图装置改进实验,验证了质量守恒定律,却发现产物中还有少量黄色固体.
【提出问题】黄色固体是什么呢?
【查阅资料】①氧化镁为白色固体;
②镁能与氮气反应生成黄色的氮化镁(Mg3N2)固体;
③氮化镁可与水剧烈反应产生氨气,该气体能使无色酚酞试液变色.
【做出猜想】黄色固体为Mg3N2
【实验探究】请设计实验,验证猜想
【反思与交流】空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成的MgO却远多于Mg3N2,为什么呢?请给出合理的解释氧气的化学性质比氮气更活泼,镁条更容易与氧气发生反应.
 某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.
某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.(1)请写出镁条与氧气反应的化学方程式2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO.
(2)小明发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵守质量守恒定律.我不同意 (“同意”或“不同意”)小明的观点.
(3)小红按图装置改进实验,验证了质量守恒定律,却发现产物中还有少量黄色固体.
【提出问题】黄色固体是什么呢?
【查阅资料】①氧化镁为白色固体;
②镁能与氮气反应生成黄色的氮化镁(Mg3N2)固体;
③氮化镁可与水剧烈反应产生氨气,该气体能使无色酚酞试液变色.
【做出猜想】黄色固体为Mg3N2
【实验探究】请设计实验,验证猜想
| 实验操作 | 实验现象 | 结论 |
| ①取样于试管中,加入少量的水 | 试管中产生气泡 | 黄色固体为Mg3N2 |
| ②将生成的气体通入到酚酞溶液中 | 溶液呈红色 |
14.下列物质加入水中,所得溶液pH可能为10的是( )
| A. | 生石灰 | B. | 醋酸 | C. | 石灰石 | D. | 食盐 |
11.下列关于化学史方面的叙述中,不正确的是( )
| A. | 发明侯氏制碱法的科学家是侯德榜 | |
| B. | 最早用湿法冶金原理炼铜的国家是中国 | |
| C. | 最早通过实验得出空气由氮气和氧气组成的科学家是道尔顿 | |
| D. | 最早发现元素之间存在联系并排列出元素周期表的科学家是门捷列夫 |
15.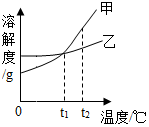 如表是NaCl、NH4Cl在不同温度时的溶解度.
如表是NaCl、NH4Cl在不同温度时的溶解度.
(1)如图表示氯化铵溶解度曲线的是甲(填甲或者乙).
(2)t1的范围为0~20
(3)将t2℃等质量的两种物质的饱和溶液降温至t1℃,对所得溶液的叙述正确的③④⑤(填序号).
①溶质质量分数:甲>乙 ②溶液质量:甲>乙
③所含溶剂质量:甲<乙 ④甲、乙都是饱和溶液 ⑤溶质质量:甲<乙
(4)t2℃等质量的两种物质配置成饱和溶液所得溶液的质量甲<乙(填><或=)
 如表是NaCl、NH4Cl在不同温度时的溶解度.
如表是NaCl、NH4Cl在不同温度时的溶解度.| 温度/℃ | 0 | 20 | 40 | 60 | 80 | |
| 溶解度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
| NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 | 65.6 | |
(2)t1的范围为0~20
(3)将t2℃等质量的两种物质的饱和溶液降温至t1℃,对所得溶液的叙述正确的③④⑤(填序号).
①溶质质量分数:甲>乙 ②溶液质量:甲>乙
③所含溶剂质量:甲<乙 ④甲、乙都是饱和溶液 ⑤溶质质量:甲<乙
(4)t2℃等质量的两种物质配置成饱和溶液所得溶液的质量甲<乙(填><或=)
