题目内容
10.将生锈的铁钉放入过量的稀硫酸中,首先看到铁锈逐渐消失,溶液呈黄色,反应的化学方程式为Fe2O3+3H2SO4=Fe2(SO4)3+3H2O,过一会儿,又看见有气泡产生,这是因为Fe+H2SO4=FeSO4+H2↑(用化学方程式表示).分析 铁锈的主要成分是氧化铁,能与稀硫酸反应生成硫酸铁和水,写出反应的现象、化学方程式即可;铁锈完全消失后,铁与稀硫酸反应生成硫酸亚铁和氢气,故会看到铁钉表面有气泡产生,据此写出反应的化学方程式.
解答 解:铁锈的主要成分是氧化铁,能与稀硫酸反应生成硫酸铁和水,反应现象为:铁锈逐渐消失,无色溶液变成黄色,反应的化学方程式为:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;
铁锈完全消失后,铁与稀硫酸反应生成硫酸亚铁和氢气,反应的化学方程式为:Fe+H2SO4=FeSO4+H2↑.
故答案为:铁锈逐渐消失,黄;Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;Fe+H2SO4=FeSO4+H2↑.
点评 本题难度不大,掌握酸的化学性质、化学方程式的书写等是正确解答本题的关键.

练习册系列答案
相关题目
20.用化学方法制得高纯度硅的反应原理是:SiCl4+2H2═Si+4HCl,该反应属于( )
| A. | 化合反应 | B. | 复分解反应 | C. | 置换反应 | D. | 分解反应 |
15.下列各物质(或其主要成分)的名称或俗称与其后的化学式不一致的是( )
| A. | 金刚石 石墨 C | B. | 冰 干冰 H2O | ||
| C. | 氧气 液氧 O2 | D. | 石灰石 大理石 CaCO3 |
2.下列选项不属于化学这门学科研究范畴的是( )
| A. | 物质的组成与结构 | B. | 物质的性质与变化 | ||
| C. | 物质的运动状态 | D. | 物质的用途与制取 |
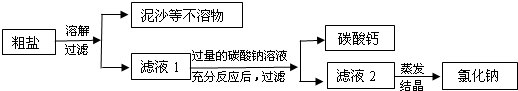
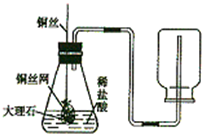 我们学习了实验室制取O2和CO2的方法,相信你能够回答下列间题.
我们学习了实验室制取O2和CO2的方法,相信你能够回答下列间题.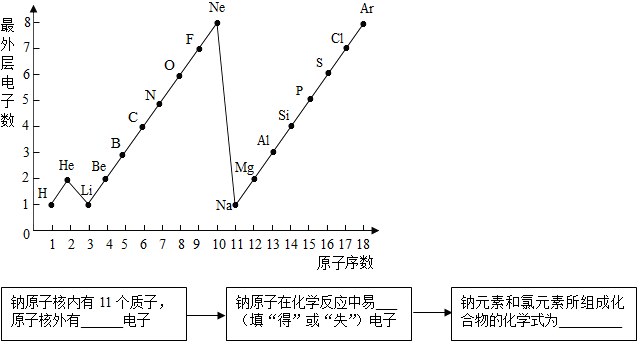
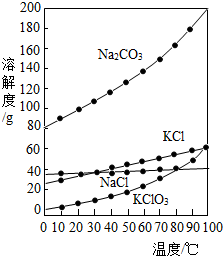 氯酸钾多用来制造火柴和烟花等.电解法是工业制造氯酸钾的主要方法:先电解热的氯化钠水溶液,电解的生成物烧碱和Cl2相互反应制得氯酸钠、氯化钠和水;再以氯酸钠和氯化钾为原料制备氯酸钾.
氯酸钾多用来制造火柴和烟花等.电解法是工业制造氯酸钾的主要方法:先电解热的氯化钠水溶液,电解的生成物烧碱和Cl2相互反应制得氯酸钠、氯化钠和水;再以氯酸钠和氯化钾为原料制备氯酸钾.