题目内容
18. 我们学习了实验室制取O2和CO2的方法,相信你能够回答下列间题.
我们学习了实验室制取O2和CO2的方法,相信你能够回答下列间题.(1)实验室制取O2可以选择多种药品,当选择高锰酸钾时,发生反应的化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
如果要收集纯度比较高的O2,最好用排水法收集.比较用过氧化氢溶液和用氯酸钾制取O2的方法,二者的共同点是BC.
A.发生装置相同 B.都可用MnO2作催化剂
C.反应的基本类型相同 D.完全反应后剩余固体成分相同
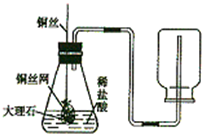
(2)李丽同学设计了实验室制取CO2装置(如图所示),装置中出现了一个错误,你的纠正方法是
用向上排空气法收集CO2.锥形瓶中发生反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑.铜丝上下抽动起到的作用是使反应随时停止和发生.
如果将铜丝网改成铁丝网,收集到的CO2中还会含有H2.
分析 (1)可比较两种制取氧气的反应原理进行对比,根据氧气的水溶性结合实验目的选择收集方法.根据排水法收集的气体较为纯净、运用双氧水制取氧气的反应原理、装置及运用氯酸钾制取氧气的反应原理、装置分析;
(2)根据二氧化碳是密度来判断收集方法的正误;根据反应的操作性分析铜丝的作用;根据铁的化学性质及反应液进行分析铁丝的反应.
解答 解:(1)实验室用高锰酸钾制取氧气的反应方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
用双氧水制取氧气的反应方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,因为氧气不溶于水,密度比空气大,可用排水法和向下排空气法收集,根据实验目的要求收集比较纯净的氧气,所以用排水法;对比两种方法可知因为条件不同所以反应装置不同,二氧化锰第一个和第二个都是催化剂,反应类型都是分解反应,生成物不相同,所以选BC.
故答案为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;排水;BC;
(2)大理石和稀盐酸反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑,因为二氧化碳密度大于空气,所以应该用向上排空气法收集;操作时当铜丝向上提升时,大理石和盐酸分离,反应停止,落下时接触反应开始,所以铜丝的作用是使反应随时停止和发生;当把铜丝换成铁丝时,铁丝可用和盐酸反应生成氢气.
故答案为:用向上排空气法收集CO2; CaCO3+2HCl=CaCl2+H2O+CO2↑;使反应随时停止和发生;H2
点评 熟练掌握实验室中制取气体的发生装置和收集装置的选择依据,并能作出正确的选择.

 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案| A. | 合金是金属的混合物 | B. | 合金是有金属特性的化合物 | ||
| C. | 生铁和钢都是铁的合金 | D. | 钢是铁合金,生铁不是铁合金 |
| A. | Cu(Zn ) 加入过量的稀硫酸 | B. | CO2(CO) 通入氧气点燃 | ||
| C. | Fe(Fe2O3) 加入适量的盐酸 | D. | CaO(CaCO3) 加入适量稀盐酸 |
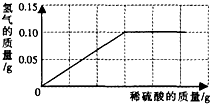 为了测定黄铜(铜、锌合金)的组成,某研究性学习小组称取该样品10g,向其中逐滴加入9.8%的稀硫酸至刚好不再产生气体为止.反应过程中生成的气体与所用硫酸溶液的质量关系如图所示.试计算:
为了测定黄铜(铜、锌合金)的组成,某研究性学习小组称取该样品10g,向其中逐滴加入9.8%的稀硫酸至刚好不再产生气体为止.反应过程中生成的气体与所用硫酸溶液的质量关系如图所示.试计算: