题目内容
10.用化学方程式解释下列现象.(1)“湿法冶铜”的反应原理:Fe+CuS04=Cu+FeSO4.
(2)氢化镁(MgH2)固体可作为氢动力汽车的能源提供剂.提供能源时MgH2与水反应生成一种碱和氢气:MgH2+2H2O═Mg(OH)2+2H2↑.
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写即可.
解答 解:(1)“湿法冶铜”是铁和硫酸铜溶液反应生成硫酸亚铁和铜,反应的化学方程式为Fe+CuS04=Cu+FeSO4.
(2)氢化镁(MgH2)固体与水反应生成生成一种碱(由质量守恒定律,反应前后元素种类不变,该碱是氢氧化镁)和氢气,反应的化学方程式为:MgH2+2H2O═Mg(OH)2+2H2↑.
故答案为:(1)Fe+CuS04=Cu+FeSO4;(2)MgH2+2H2O═Mg(OH)2+2H2↑.
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
相关题目
15.下列实验操作、现象、结论或解释,其中错误的一组是( )
| 组别 | 操作 | 现象 | 结论或解释 |
| A | 切开土豆,在剖面上滴两滴碘水 | 变蓝 | 土豆含有淀粉 |
| B | 在1mL无色溶液中滴加石蕊试液 | 溶液变红 | 原溶液呈碱性 |
| C | 取3mLH2O2溶液微热,再向该溶液中加入 少量MnO2 | 先产生少量气泡,加MnO2后产生大量气泡 | MnO2对H2O2分解有催化作用 |
| D | 取2mL鸡蛋清,加入几滴硫酸铜溶液 | 鸡蛋清凝结 | 硫酸铜能使蛋白质变性 |
| A. | A | B. | B | C. | C | D. | D |
20.下列各组离子在水中能大量共存的是( )
| A. | Na+、Ba2+、CO32-、NO3- | B. | Na+、H+、OH-、K+ | ||
| C. | K+、NO3-、Cl-、NH4+ | D. | H+、HCO3-、Cl-、SO42- |
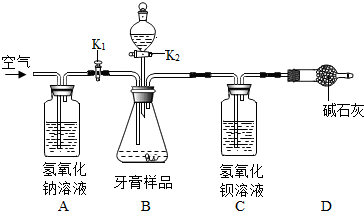 牙膏摩擦剂的类型很多,如CaCO3、SiO2或它们的混合物.某兴趣小组对某品牌牙膏摩擦剂的成分进行了如下探究.
牙膏摩擦剂的类型很多,如CaCO3、SiO2或它们的混合物.某兴趣小组对某品牌牙膏摩擦剂的成分进行了如下探究.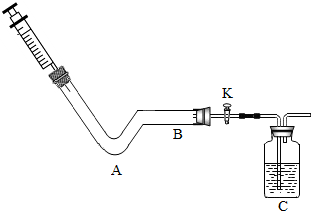 实验装置创新:
实验装置创新: