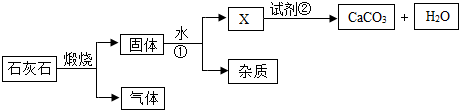
题目内容
17.下列除去杂质的方法均正确的是( )| 物质 | 所含杂质 | 所加药品 | 用量 | 操作 | |
| A | NaCl溶液 | NaOH和Na2CO3 | 稀盐酸 | 适量 | 加稀盐酸至恰好不再产生气泡 |
| B | CuO粉末 | C | 稀盐酸 | 足量 | 加入稀盐酸充分反应后过滤 |
| C | Cu | CuCl2固体 | 水 | 适量 | 加水搅拌后,过滤 |
| D | K2SO4 | CuSO4 | 氢氧化钾溶液 | 适量 | 加入适量氢氧化钾溶液,蒸发 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、NaOH和Na2CO3能与适量稀盐酸反应分别生成氯化钠和水,氯化钠、水和二氧化碳,至恰好不再产生气泡,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
B、CuO粉末能与稀盐酸反应生成氯化铜和水,铜不与稀硫酸反应,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
C、CuCl2固体易溶于水,Cu难溶于水,可采取加水溶解、过滤的方法进行分离除杂,故选项所采取的方法正确.
D、CuSO4能与氢氧化钾溶液溶液反应生成氢氧化铜沉淀和硫酸钾,应过滤后再进行蒸发,故选项所采取的方法错误.
故选:C.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
相关题目
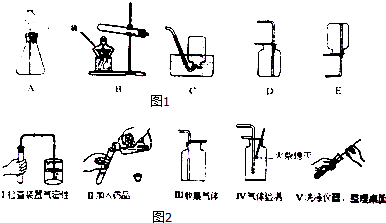
7.①实验室制取氧气,结合下列实验装置图回答有关问题:

Ⅰ.仪器i名称是酒精灯,装置D名称是启普发生器.
Ⅱ.实验室用氯酸钾和二氧化锰的混合物制O2,发生反应的化学方程式为2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
Ⅲ.实验室用双氧水和二氧化锰的混合物制O2,为了控制氧气产生的速率,应选用的发生装置是C(填字母).经实验验证,以下四种物质:红砖粉、细砂、金属铜网、水泥块,都可用作双氧水分解的催化剂,其中适合在D装置中使用的是b(填序号).
a.红砖粉 b.金属铜网、水泥块
c.细砂、金属铜网、水泥块 d.都可以
②同学们在进行氧气性质实验时,发现很多因素都会对实验结果产生影响.

Ⅰ.仪器i名称是酒精灯,装置D名称是启普发生器.
Ⅱ.实验室用氯酸钾和二氧化锰的混合物制O2,发生反应的化学方程式为2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
Ⅲ.实验室用双氧水和二氧化锰的混合物制O2,为了控制氧气产生的速率,应选用的发生装置是C(填字母).经实验验证,以下四种物质:红砖粉、细砂、金属铜网、水泥块,都可用作双氧水分解的催化剂,其中适合在D装置中使用的是b(填序号).
a.红砖粉 b.金属铜网、水泥块
c.细砂、金属铜网、水泥块 d.都可以
②同学们在进行氧气性质实验时,发现很多因素都会对实验结果产生影响.
| 实验 | 分析与结论 |
| Ⅰ.硫在空气中燃烧发出微弱的淡蓝色火焰,硫在氧气中燃烧发出明亮的蓝紫色火焰. | 说明反应物的浓度不同,反应现象不同. |
| Ⅱ.细铁丝在氧气中易燃烧,发生的化学方程式3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.粗铁丝在氧气中不燃烧. | 说明反应物的形状不同,反应的速率不同. |
| Ⅲ.碳在氧气不足的条件下燃烧生成一氧化碳,碳在氧气充足的条件下燃烧生成二氧化碳. | 说明反应物的用量不同,生成物不同. |
8.下列关于物质的用途不正确的是( )
| A. | 公路上的积雪可用氯化钠来消除 | B. | 熟石灰可以改良碱性土壤 | ||
| C. | 盐酸可用于制造氯化锌等药物 | D. | 碳酸氢钠能治疗胃酸过多的症状 |
5. 某校化学兴趣小组为了解碳酸氢钠粉末(NaHCO3)的化学性质,进行了如下探究.该小组成员将少量碳酸氢钠粉末置于如图装置的试管中,充分加热至反应完全,发现试管口出现无色液体,澄清石灰水变浑浊,且试管底部有白色固体残余.两位同学提出以下猜想:
某校化学兴趣小组为了解碳酸氢钠粉末(NaHCO3)的化学性质,进行了如下探究.该小组成员将少量碳酸氢钠粉末置于如图装置的试管中,充分加热至反应完全,发现试管口出现无色液体,澄清石灰水变浑浊,且试管底部有白色固体残余.两位同学提出以下猜想:
(1)提出问题:残余白色固体的成分是什么?
(2)猜想与假设:根据化学反应前后元素种类不变,两位同学提出以下猜想:
【猜想一】甲同学:“白色固体是氢氧化钠(NaOH)”;
【猜想二】乙同学:“白色固体是碳酸钠(Na2CO3)”.
(3)实验与结论:①澄清石灰水变浑浊的反应方程式:CO2+Ca(OH)2═CaCO3↓+H2O;
②为了验证自己的猜想,甲同学设计了以下方案并实验验证:
根据甲同学的猜想与验证,乙同学认为甲的结论不准确,因为NaOH与Na2CO3的水溶液均显碱性,都能使无色酚酞试液变红.
③以下是乙同学设计的实验:
④根据以上实验探究内容,写出碳酸氢钠受热分解的化学方程式:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
(4)讨论交流:你还能设计不同的实验方案来验证乙同学的猜想吗?
 某校化学兴趣小组为了解碳酸氢钠粉末(NaHCO3)的化学性质,进行了如下探究.该小组成员将少量碳酸氢钠粉末置于如图装置的试管中,充分加热至反应完全,发现试管口出现无色液体,澄清石灰水变浑浊,且试管底部有白色固体残余.两位同学提出以下猜想:
某校化学兴趣小组为了解碳酸氢钠粉末(NaHCO3)的化学性质,进行了如下探究.该小组成员将少量碳酸氢钠粉末置于如图装置的试管中,充分加热至反应完全,发现试管口出现无色液体,澄清石灰水变浑浊,且试管底部有白色固体残余.两位同学提出以下猜想:(1)提出问题:残余白色固体的成分是什么?
(2)猜想与假设:根据化学反应前后元素种类不变,两位同学提出以下猜想:
【猜想一】甲同学:“白色固体是氢氧化钠(NaOH)”;
【猜想二】乙同学:“白色固体是碳酸钠(Na2CO3)”.
(3)实验与结论:①澄清石灰水变浑浊的反应方程式:CO2+Ca(OH)2═CaCO3↓+H2O;
②为了验证自己的猜想,甲同学设计了以下方案并实验验证:
| 实验步骤 | 现象 | 实验结论 |
| 取少量残余固体于试管中,加入适量的水使之溶解,往试管中滴加2滴无色酚酞溶液,观察现象 | 溶液变红 | 白色固体是氢氧化钠 |
③以下是乙同学设计的实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量残余固体于试管中, 加入适量稀盐酸,观察现象 | 试管中产生大量气泡 | 白色固体是碳酸钠 |
(4)讨论交流:你还能设计不同的实验方案来验证乙同学的猜想吗?
| 实验步骤 | 现象 | 实验结论 |
| 白色固体是碳酸钠 |
12.近日,中外科学家开发出一种新型光催化剂-碳纳米点一氮化碳纳米复合物,它可以利用太阳能高效并完全地分解水,整个过程分为两个阶段:第一步,氮化碳分解水生成过氧化氢和氢气;第二步,碳纳米点将过氧化氢分解成水和氧气.下列有关该过程的说法正确的是( )
| A. | 碳纳米点一氮化碳纳米复合物是一种新型化合物 | |
| B. | 氮化碳(C3N4)中碳、氧质量比为3:4 | |
| C. | 该新型光催化剂的质量在反应前后发生了变化 | |
| D. | 以上两个反应前后原子总数都不变 |
2.小军和小明两位同学想用野外的“石头”代替大理石制取二氧化碳.他们找到一块石头(白色),为了确定其能否作代用品,请你参与他们探究白色固体成分的活动.
[查阅资料]碳酸钙在高温下分解得到氧化钙和二氧化碳.
(1)小军的探究过程是:
[作出猜想]白色固体中可能含有CaCO3.
[实验验证](写出实验步骤和现象)取试样于试管中,加入足量稀盐酸,有气泡产生.
[实验结论]猜想成立.
(2)小明的探究过程是:
[作出猜想]白色固体可能含有氧化钙.
[设计方案]
[反思与评价]小明的探究过程能证明他的猜想吗?请说明理由.不能,固体部分溶解说明还有未分解的碳酸钙
(3)根据探究,推测此石头样品的成分中含有碳酸钙和氧化钙.
[查阅资料]碳酸钙在高温下分解得到氧化钙和二氧化碳.
(1)小军的探究过程是:
[作出猜想]白色固体中可能含有CaCO3.
[实验验证](写出实验步骤和现象)取试样于试管中,加入足量稀盐酸,有气泡产生.
[实验结论]猜想成立.
(2)小明的探究过程是:
[作出猜想]白色固体可能含有氧化钙.
[设计方案]
| 操 作 | 现 象 | 结 论 |
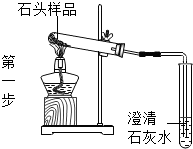 | 石头样品变疏松 | 石头样品可能发生了化学变化 |
| 澄清石灰水变浑浊 | 化学方程式为 CO2+Ca(OH)2═H20+CaCO3↓ | |
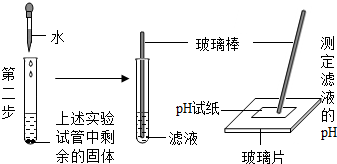 | 固体部分溶解,测得pH约为12 | 该滤液呈碱性.白色固体中含有氧化钙 |
(3)根据探究,推测此石头样品的成分中含有碳酸钙和氧化钙.