题目内容
5.下列方案设计中能够达到实验目的是( )| A. | 用点燃的方法除去CO2中的CO | |
| B. | 用生石灰除去二氧化碳中的水蒸气 | |
| C. | 用水鉴别NH4NO3和NaOH固体 | |
| D. | 用硝酸银溶液鉴别氯化钠溶液和稀盐酸 |
分析 除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
根据三种物质与同种试剂反应产生的不同现象来鉴别它们,若两种物质与同种物质反应的现象相同,则无法鉴别它们.
解答 解:A、除去二氧化碳中的一氧化碳不能够点燃,这是因为当二氧化碳(不能燃烧、不能支持燃烧)大量存在时,少量的一氧化碳是不会燃烧的;故选项方案设计不能够达到实验目的.
B、生石灰与水反应生成氢氧化钙,生成的氢氧化钙与二氧化碳反应生成碳酸钙和水,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项方案设计不能够达到实验目的.
C、NH4NO3和NaOH固体分别溶于水吸热、放热,使溶温度分别降低、升高,可以鉴别,故选项方案设计能够达到实验目的.
D、氯化钠溶液和稀盐酸均能与硝酸银溶液反应生成氯化银白色沉淀,不能比较,故选项方案设计不能够达到实验目的.
故选:C.
点评 本题难度不是很大,化学实验方案的设计是考查学生能力的主要类型,同时也是实验教与学难点,在具体设计时要对其原理透彻理解,可根据物质的物理性质和化学性质结合实验目的进行分析判断.

练习册系列答案
相关题目
14.在密闭容器中,盛放A、B、C三种物质各30g,经电火花引燃,充分反应后,各物质质量变化如表:关于此反应,下列认识不正确的是( )
| 物质 | A | B | C | 新物质D |
| 反应前质量/g | 30 | 30 | 30 | 0 |
| 反应后质量/g | 待测 | 33 | 0 | 22 |
| A. | 变化后待测的A质量为5g | |
| B. | 物质C中所含有的元素种类是A、B、D三种物质中所有元素种类之和 | |
| C. | 该变化的基本反应类型是分解反应 | |
| D. | A物质可能是单质,C一定是化合物 |

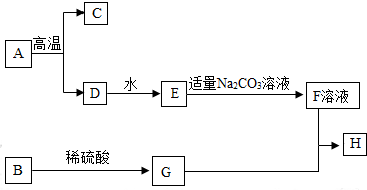
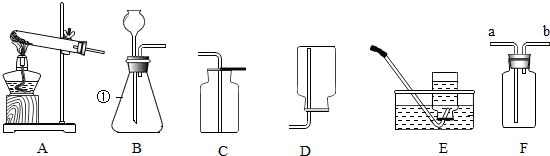
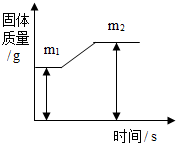 质量守恒定律是一条重要规律,请利用该规律的相关知识回答下列问题.
质量守恒定律是一条重要规律,请利用该规律的相关知识回答下列问题. 甲和乙两种固体物质的溶解度曲线如图所示,回答下列问题:
甲和乙两种固体物质的溶解度曲线如图所示,回答下列问题: