题目内容
6.下列实验操作中,正确的是( )| A. | 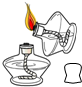 点燃酒精灯 | B. |  取锌粒 | C. | 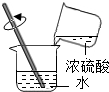 稀释浓硫酸 稀释浓硫酸 | D. |  蒸发 |
分析 A、根据酒精灯要用火柴点燃分析;
B、根据直接将锌粒倒入试管中,会砸破试管分析;
C、根据稀释浓硫酸要注意事项分析判断;
D、根据蒸发操作的注意事项:用玻璃棒不断搅拌进行分析判断.
解答 解:A、用燃着的酒精灯去点燃另一只酒精灯时,容易引起火灾.错误;
B、直接将锌粒倒入试管中,会砸破试管,应该将试管横放,将锌粒送入试管底部,然后慢慢竖起试管,故错误;
C、稀释浓硫酸时,将浓硫酸倒入水,并不断搅拌,这样可以防止液滴飞溅,正确;
D、蒸发时,应用玻璃棒不断搅拌,以防液体受热不均匀,造成液体飞溅,错误.
故选C.
点评 本题主要考查实验操作方面的知识,解答时要理解各种操作的规范性,如果操作不当,容易引发安全事故.

练习册系列答案
相关题目
17.学完了酸碱的知识,老师安排同学们做稀盐酸和氢氧化钠溶液的中和反应实验.
【实验步骤】先取10滴氢氧化钠溶液,再滴加2滴无色酚酞,待溶液变红之后逐滴加入稀盐酸溶液,至恰好无色为止,请写出该中和反应的化学方程式NaOH+HCl=NaCl+H2O.
【发现问题】小明同学用pH计测试自己中和后的溶液pH=5.6,则此时溶液显酸性(填“酸性”或“中性”或“碱性”),于是同学们建议使用紫色石蕊溶液做指示剂,但是得到的实验结果仍然不能令人满意.
【查阅资料】同学们上网查找到如下资料:
酚酞:pH>0 红色:pH<8.2 无色 8.2≤pH≤10 浅红色:
石蕊:pH<5.0 红色:pH>8.0 蓝色 5.0≤pH≤8.0 紫色:
【解决问题】
(1)通过以上资料分析,酚酞溶液和石蕊溶液能否准确指示中和反应的终点?不能
(2)为了更科学的测试,小明又重新做了一次实验,用pH计测试逐滴加入后的pH,实验数据记录如下:
(3)你判断此次实验操作是A.
A.稀盐酸溶液滴加到氢氧化钠溶液中 B.氢氧化钠溶液滴加到稀盐酸溶液中
(4)你认为稀盐酸和氢氧化钠溶液恰好完全中和发生在第7~8滴之间.
【反思】小明同学在用放置了一段时间的药品进行实验的过程中,发现了有一部分气体生成.解释生成的气体的原因:氢氧化钠发生变质生成碳酸钠,碳酸钠与盐酸反应生成二氧化碳气体.
【实验步骤】先取10滴氢氧化钠溶液,再滴加2滴无色酚酞,待溶液变红之后逐滴加入稀盐酸溶液,至恰好无色为止,请写出该中和反应的化学方程式NaOH+HCl=NaCl+H2O.
【发现问题】小明同学用pH计测试自己中和后的溶液pH=5.6,则此时溶液显酸性(填“酸性”或“中性”或“碱性”),于是同学们建议使用紫色石蕊溶液做指示剂,但是得到的实验结果仍然不能令人满意.
【查阅资料】同学们上网查找到如下资料:
酚酞:pH>0 红色:pH<8.2 无色 8.2≤pH≤10 浅红色:
石蕊:pH<5.0 红色:pH>8.0 蓝色 5.0≤pH≤8.0 紫色:
【解决问题】
(1)通过以上资料分析,酚酞溶液和石蕊溶液能否准确指示中和反应的终点?不能
(2)为了更科学的测试,小明又重新做了一次实验,用pH计测试逐滴加入后的pH,实验数据记录如下:
| 滴数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 |
| PH | 13.4 | 13.3 | 13.2 | 13.0 | 12.8 | 12.96 | 12.4 | 4.5 | 1.6 | 1.4 | 1.3 |
A.稀盐酸溶液滴加到氢氧化钠溶液中 B.氢氧化钠溶液滴加到稀盐酸溶液中
(4)你认为稀盐酸和氢氧化钠溶液恰好完全中和发生在第7~8滴之间.
【反思】小明同学在用放置了一段时间的药品进行实验的过程中,发现了有一部分气体生成.解释生成的气体的原因:氢氧化钠发生变质生成碳酸钠,碳酸钠与盐酸反应生成二氧化碳气体.
14.下列事实的结论、解释或方法中不正确的是( )
| A. | 稀盐酸用于除铁锈--酸能与金属氧化物反应 | |
| B. | 洗涤剂去除油污--溶解作用 | |
| C. | 区分硬水与软水--加肥皂水搅拌 | |
| D. | 区分羊毛纤维与合成纤维--灼烧后闻气味 |
11.以科学原理和事实为依据进行推理是学习化学的一种重要方法,下列推理合理的是( )
| A. | 铵盐能与碱反应产生氨气,所以碳酸氢铵能与氢氧化钠反应产生氨气 | |
| B. | 盐是由金属离子和酸根离子组成的,所以盐中一定含有金属离子 | |
| C. | 有机物中一定含有碳元素,所以含有碳元素的化合物一定是有机物 | |
| D. | 碱溶液能使无色酚酞试液变红,所以使无色酚酞试液变红的溶液一定是碱溶液 |
18.某化学兴趣小组在探究稀盐酸的化学性质时,做了如图一所示的三个实验.
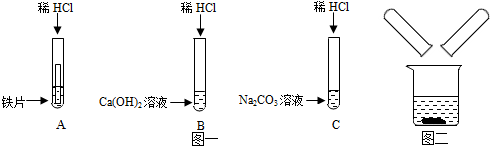
(1)写出A试管中的反应现象铁片表面有气泡产生,溶液由无色逐渐变为浅绿色.
(2)写出B试管中反应的化学方程式Ca(OH)2+2HCl═CaCl2+2H2O.
(3)实验结束后,小组同学将B、C两支试管中的废液同时倒入一个洁净的烧杯中(如图二所示),观察到先有气泡产生,后有白色沉淀生成.同学们将烧杯内的物质进行过滤,对所得滤液的溶质成分进行探究.
【提出猜想】
甲同学猜想:NaCl;
乙同学猜想:NaCl、CaCl2;
丙同学猜想:NaCl、CaCl2、HCl;
你的猜想:NaCl、Na2CO3.
【交流讨论】
你认为丙同学的猜想一定不正确,理由是Na2CO3先和HCl反应,当HCl过量时,Na2CO3被完全反应,不可能再与CaCl2反应生成白色沉淀.
【设计实验】请设计实验证明你的猜想正确.

(1)写出A试管中的反应现象铁片表面有气泡产生,溶液由无色逐渐变为浅绿色.
(2)写出B试管中反应的化学方程式Ca(OH)2+2HCl═CaCl2+2H2O.
(3)实验结束后,小组同学将B、C两支试管中的废液同时倒入一个洁净的烧杯中(如图二所示),观察到先有气泡产生,后有白色沉淀生成.同学们将烧杯内的物质进行过滤,对所得滤液的溶质成分进行探究.
【提出猜想】
甲同学猜想:NaCl;
乙同学猜想:NaCl、CaCl2;
丙同学猜想:NaCl、CaCl2、HCl;
你的猜想:NaCl、Na2CO3.
【交流讨论】
你认为丙同学的猜想一定不正确,理由是Na2CO3先和HCl反应,当HCl过量时,Na2CO3被完全反应,不可能再与CaCl2反应生成白色沉淀.
【设计实验】请设计实验证明你的猜想正确.
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量滤液于试管中,向其中滴加无色酚酞试液 | 无色酚酞试液变红 | 猜想成立 |

 与
与 的不同之处是(写两点):①质子数不同;②电子数层不同(或电子数不同等).
的不同之处是(写两点):①质子数不同;②电子数层不同(或电子数不同等).