题目内容
18.某化学兴趣小组在探究稀盐酸的化学性质时,做了如图一所示的三个实验.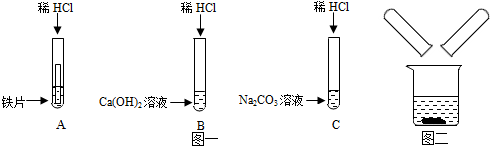
(1)写出A试管中的反应现象铁片表面有气泡产生,溶液由无色逐渐变为浅绿色.
(2)写出B试管中反应的化学方程式Ca(OH)2+2HCl═CaCl2+2H2O.
(3)实验结束后,小组同学将B、C两支试管中的废液同时倒入一个洁净的烧杯中(如图二所示),观察到先有气泡产生,后有白色沉淀生成.同学们将烧杯内的物质进行过滤,对所得滤液的溶质成分进行探究.
【提出猜想】
甲同学猜想:NaCl;
乙同学猜想:NaCl、CaCl2;
丙同学猜想:NaCl、CaCl2、HCl;
你的猜想:NaCl、Na2CO3.
【交流讨论】
你认为丙同学的猜想一定不正确,理由是Na2CO3先和HCl反应,当HCl过量时,Na2CO3被完全反应,不可能再与CaCl2反应生成白色沉淀.
【设计实验】请设计实验证明你的猜想正确.
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量滤液于试管中,向其中滴加无色酚酞试液 | 无色酚酞试液变红 | 猜想成立 |
分析 (1)根据铁与稀盐酸的反应分析A试管中的反应现象;
(2)根据氢氧化钙与稀盐酸的反应写出反应的化学方程式;
(3)根据反应的现象分析可能混合的试管.
【提出猜想】根据反应的量分析滤液的溶质成分;
【交流讨论】根据根据碳酸钠、氯化钙和盐酸的性质分析反应分析错误的猜想;
【设计实验】根据碳酸钠显碱性能使酚酞试液变红色设计实验.
解答 解:(1)由于铁与稀盐酸的反应生成了氯化亚铁和氢气,所以A试管中的反应现象铁片表面有气泡产生,溶液由无色逐渐变为浅绿色.
(2)在B试管中氢氧化钙与盐酸反应生成了氯化钙和水,反应的化学方程式是:Ca(OH)2+2HCl═CaCl2+2H2O.
(3)由实验的现象可知,混合后的溶液先产生气泡,说明在C中有剩余的碳酸钠,另一支试管中有剩余的盐酸,后有白色沉淀生成,沉淀应为碳酸钙,说明溶液含有氯化钙,由此可知,应是B、C试管的混合.
【提出猜想】由上述分析可知,当碳酸钠与盐酸、氯化钙恰好反应时,滤液中只含有氯化钠;当氯化钙有剩余时,滤液中含有氯化钠和氯化钙,当碳酸钠剩余时,滤液中含有氯化钠和碳酸钠.所以我的猜想是:NaCl、Na2CO3.
【交流讨论】由于Na2CO3先和HCl反应,当HCl过量时,Na2CO3被完全反应,不可能再与CaCl2反应生成白色沉淀,所以丙同学猜想不成立.
【设计实验】由于碳酸钠显碱性能使酚酞试液变红色,所以,设计实验如下:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量滤液于试管中,向其中滴加 无色酚酞试液 | 无色酚酞试液变红 | 猜想成立 |
(3)B、C;
【提出猜想】NaCl、Na2CO3;
【交流讨论】①丙,Na2CO3先和HCl反应,当HCl过量时,Na2CO3被完全反应,不可能再与CaCl2反应生成白色沉淀.
【设计实验】:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量滤液于试管中,向其中滴加 无色酚酞试液 | 无色酚酞试液变红 | 猜想成立 |
点评 本题通过实验探究了稀盐酸的性质,难度不大,掌握盐酸与金属、碱、盐反应的性质、现象等知识是解答本题的关键.

练习册系列答案
相关题目
8.如图是某个化学反应的微观示意图,下列判断正确的是( )
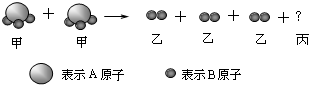

| A. | 反应物是混合物 | |
| B. | 乙是化合物 | |
| C. | 根据质量守恒定律可推知,1个丙分子中含有2个A原子 | |
| D. | 该化学反应中分子的种类没有发生改变 |
6.下列实验操作中,正确的是( )
| A. | 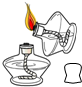 点燃酒精灯 | B. |  取锌粒 | C. | 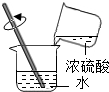 稀释浓硫酸 稀释浓硫酸 | D. |  蒸发 |
3.某学习小组用相同的洁净无锈的铁钉对铁制品锈蚀的条件进行探究,设计的实验如图所示,一周后观察,下列说法错误的是( )
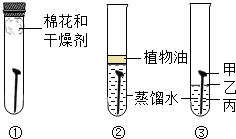

| A. | ①和②中的铁钉无明显变化,③中的铁钉明显生锈 | |
| B. | ②中加入的蒸馏水要事先煮沸,目的是除去水中溶解的氧气 | |
| C. | ③中铁钉的甲、乙、丙三处,甲处锈蚀最严重 | |
| D. | 探究发现铁生锈的主要条件是铁与空气和水(火或水蒸气)直接接触 |
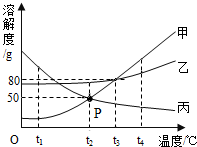 如图为甲、乙、丙三种物质的溶解度曲线.回答下列问题:
如图为甲、乙、丙三种物质的溶解度曲线.回答下列问题: