题目内容
14.KNO3和NaCl的溶解度如下表所示,回答下列问题.| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | |
| 溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
| KCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 | |
(2)60℃KNO3的饱和溶液中含有少量的NaCl,将其降温到20℃时,一定析出的物质是硝酸钾;
(3)在溶质质量分数不变的情况下,将60℃KNO3的不饱和溶液变为饱和溶液可采用的方法是降温.
分析 (1)根据20℃时氯化钠溶解度分析溶解情况判断溶液的状态;
(2)根据硝酸钾和氯化钠的溶解度随温度变化的情况分析;
(3)根据不饱和溶液转化为饱和溶液的方法及溶质质量分数的变化分析.
解答 解:(1)20℃时氯化钠溶解度为36g,因此100g水中需要溶解36g的氯化钠才能达到饱和,因此将33g NaCl放入100g水中形成的是不饱和溶液;故填:不饱和;
(2)硝酸钾的溶解度受温度影响变化大,而氯化钠的溶解度随温度变化不大,因此降低温度硝酸钾能够大量析出;故填:硝酸钾;
(3)硝酸钾的不饱和溶液转化为饱和溶液可以通过加溶质、蒸发溶剂或降低温度的方法,但加溶质和蒸发溶剂都会使溶液的溶质质量分数变大,而降温时溶质质量分数不变;故填:降温.
点评 本题考查了溶解度的有关知识,完成此题,可以依据题干提供的信息结合溶解度的概念进行.

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
4.氢氧化钴[CO(OH)2]受热易分解,能与酸性溶液反应,可作涂料和油漆的干燥剂,制备方法为:①CO+2HCl═CoCl2+H2↑,②COCl2+2NaOH═CO(OH)2↓+2NaCl.下列判断正确的是( )
| A. | 钴的金属活动性比铜弱 | B. | 钴在化合物中一般显+2价 | ||
| C. | 氢氧化钴的化学性质稳定 | D. | 氢氧化钴可以干燥氯化氢气体 |
2.下列现象中,一定发生化学变化的是( )
| A. | 木材燃烧 | B. | 汽油挥发 | C. | 干冰升华 | D. | 石蜡熔化 |
9.下列实验方案设计,合理的是( )
| A. | 用稀盐酸除去铁粉中的氧化铁粉末 | |
| B. | 用二氧化碳鉴别氧化钙溶液和氯化钠溶液 | |
| C. | 用电解水的方法获取氢气作燃料 | |
| D. | 用CuSO4溶液能证明NaOH溶液和盐酸发生反应 |
6.下列说法中,正确的是( )
| A. | CH4和CO都能在空气中燃烧,所以都可以用作燃料 | |
| B. | 铜在金属活动性顺序表中排在氢后,所以氧化铜不能与稀盐酸发生反应 | |
| C. | 有机物都含有碳元素,所以含碳元素的化合物都属于有机物 | |
| D. | 向某无色溶液中加入酚酞溶液后酚酞变红色,说明该无色溶液一定是碱溶液 |
3.水是重要的资源.下列关于水的说法中,正确的是( )
| A. | 水是一种单质 | |
| B. | 过滤可除去污水中的不溶物,使污水变为纯水 | |
| C. | 净化水时,可用活性炭作杀菌剂 | |
| D. | 用肥皂水可区分硬水和软水 |
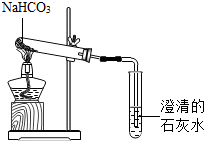 用如图所示装置加热NaHCO3,试管中留下的白色固体只有Na2CO3,并观察到试管内壁有水珠生成,澄清石灰水变浑浊.根据实验回答问题.
用如图所示装置加热NaHCO3,试管中留下的白色固体只有Na2CO3,并观察到试管内壁有水珠生成,澄清石灰水变浑浊.根据实验回答问题.