题目内容
3.图为四种粒子的结构示意图,完成以下填空: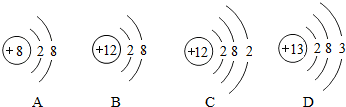
(1)属于阳离子结构的粒子是B;
(2)B粒子的符号是Mg2+
(3)某元素R形成的氧化物为R2O3,则R的原子结构示意图可能是D.
分析 (1)当质子数=核外电子数,为原子;当质子数>核外电子数,为阳离子;当质子数<核外电子数,为阴离子.
(2)B粒子质子数=12,核外电子数=10,质子数>核外电子数,为带2个单位正电荷的镁离子,写出其离子符号即可.
(3)根据元素的正化合价数等于其原子的最外层电子数、氧化物化学式为R2O3 进行分析解答.
解答 解:(1)A、质子数=8,核外电子数=10,质子数<核外电子数,为阴离子,故选项错误.
B、质子数=12,核外电子数=10,质子数>核外电子数,为阳离子,故选项正确.
C、质子数=核外电子数=12,为原子,故选项错误.
D、质子数=核外电子数=13,为原子,故选项错误.
(2)B粒子质子数=12,核外电子数=10,质子数>核外电子数,为带2个单位正电荷的镁离子,其离子符号为:Mg2+.
(3)根据某元素R形成的氧化物为R2O3,氧元素显-2价,则R元素的化合价为+3价;因为元素的正化合价数等于其原子的最外层电子数,由此可知:R的原子最外层电子数为3,原子结构示意图可能是D.
故答案为:(1)B;(2)Mg2+;(3)D.
点评 本题难度不大,考查学生对粒子结构示意图及其意义的理解,明确粒子中核内质子数和核外电子数之间的关系等是解题的关键.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
2. 某校化学活动小组为探究X、Y、Z三种金属与酸的反应情况,进行了如下实验:取等质量的X、Y、Z分别与足量的溶质质量分数相等的稀硫酸反应,都生成+2价金属的硫酸盐,反应情况如图所示.下列对该图象理解的叙述中,正确的是( )
某校化学活动小组为探究X、Y、Z三种金属与酸的反应情况,进行了如下实验:取等质量的X、Y、Z分别与足量的溶质质量分数相等的稀硫酸反应,都生成+2价金属的硫酸盐,反应情况如图所示.下列对该图象理解的叙述中,正确的是( )
 某校化学活动小组为探究X、Y、Z三种金属与酸的反应情况,进行了如下实验:取等质量的X、Y、Z分别与足量的溶质质量分数相等的稀硫酸反应,都生成+2价金属的硫酸盐,反应情况如图所示.下列对该图象理解的叙述中,正确的是( )
某校化学活动小组为探究X、Y、Z三种金属与酸的反应情况,进行了如下实验:取等质量的X、Y、Z分别与足量的溶质质量分数相等的稀硫酸反应,都生成+2价金属的硫酸盐,反应情况如图所示.下列对该图象理解的叙述中,正确的是( )| A. | 金属活动性由强到弱:X、Z、Y | B. | 金属活动性由强到弱:X、Y、Z | ||
| C. | X、Y、Z依次可能是Mg、Zn、Fe | D. | 相对原子质量的大小:Y>Z>X |
3.下列变化中,属于化学变化的是( )
| A. | 葡萄榨汁 | B. | 酒精挥发 | C. | 动物呼吸 | D. | 冰雪融化 |
20.下列变化中一定属于化学变化的是( )
| A. | 爆炸 | B. | 汽油挥发 | C. | 空气液化 | D. | 食物腐烂 |
7.下列各组物质中的杂质除去方案合理的是A
| 选项 | 杂质 | 除杂质所用试剂或方法 |
| A.H2 | HCl气体 | 先通过NaOH溶液,再通过浓硫酸 |
| B.NaOH | Ba(OH)2溶液 | 先加入CuSO4溶液、过滤 |
| C.CO | CO2气体 | 通过灼热的CuO |
| D CuCl2 | Cu(OH)2 | 加入足量稀盐酸,再进行蒸发 |
8.除去下列各组物质中的杂质,所用试剂和方法均正确的是( )
| 物质 | 杂质 | 除杂所用的试剂和方法 | |
| A | CaO | CaCO3 | 加入适量的稀盐酸,蒸发 |
| B | H2 | HCl | 依次通过NaOH溶液、浓硫酸 |
| C | NaOH溶液 | Ca(OH)2 | 先加入过量的Na2CO3溶液,再过滤 |
| D | KCl溶液 | CuCl2 | 加入氢氧化钠溶液至不再产生沉淀,过滤 |
| A. | A | B. | B | C. | C | D. | D |
13.下表是NaCl、KCl、NH4Cl、KNO3,在不同温度时的溶解度,根据表中数据间答问题
(1)30℃时,MH4Cl的溶解度为41.1g.
(2)以上四种物质中温度变化对溶解度的彩响最小的物质是NaCl;
(3)以上四种物质在农业上可用作复合肥的是KNO3;
(4)从含有少量的NaCl的KNO3溶液中得到KNO晶体的结晶较纯的方法是降温结晶;
(5)分别把1OO℃的NaCl、KCl、NH4Cl、KNO3饱和溶液降温至10℃时所得溶液的溶质质量分数最小的是硝酸钾溶液.
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 | |
| 溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 | 38.4 | 39.0 | 39.8 |
| KCl | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | 48.3 | 51.1 | 54.0 | 56.7 | |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.1 | 45.8 | 50.4 | 55.2 | 60.2 | 65.6 | 71.3 | 77.3 | |
| KNO3 | 13.3 | 20.4 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 | 202 | 246 | |
(2)以上四种物质中温度变化对溶解度的彩响最小的物质是NaCl;
(3)以上四种物质在农业上可用作复合肥的是KNO3;
(4)从含有少量的NaCl的KNO3溶液中得到KNO晶体的结晶较纯的方法是降温结晶;
(5)分别把1OO℃的NaCl、KCl、NH4Cl、KNO3饱和溶液降温至10℃时所得溶液的溶质质量分数最小的是硝酸钾溶液.
 如图所示的举重比赛中,涉及到许多物理、化学知识,如运动员在结束该次动作时,杠铃总会重重的落在地上,这是因为杠铃受到重力的作用,运动员举着杠铃在如图位置停留几秒钟,此时运动员不做功(填“做功”或“不做功”),运动员赛前所擦“镁粉”的化学名称叫“碳酸镁”,请写出其化学式为MgCO3.
如图所示的举重比赛中,涉及到许多物理、化学知识,如运动员在结束该次动作时,杠铃总会重重的落在地上,这是因为杠铃受到重力的作用,运动员举着杠铃在如图位置停留几秒钟,此时运动员不做功(填“做功”或“不做功”),运动员赛前所擦“镁粉”的化学名称叫“碳酸镁”,请写出其化学式为MgCO3.