题目内容
11.下列关于水的说法不正确的是( )| A. | 水是一种氧化物 | |
| B. | 保持水化学性质的最小微粒是水分子 | |
| C. | 电解水时在负极得到氢气 | |
| D. | NH4NO3、NaCl、NaOH三者溶于水后所得溶液温度逐渐降低 |
分析 A.根据氧化物的概念来分析;
B.根据分子的概念和水的结构来分析;
C.根据电解水的实验现象来分析;
D.根据物质溶解时的温度变化来分析.
解答 解:A.水是由氢元素与氧元素两种元素组成的化合物,属于氧化物,故正确;
B.分子是保持物质化学性质的最小粒子,水是由水分子构成的,所以水分子是保持水的化学性质的最小粒子,故正确;
C.电解水时,与电源正极相连的试管内的气体体积较小,是氧气,与电源负极相连的试管内的气体体积较大,是氢气,故正确;
D.物质在溶解时经常伴随有吸热或放热现象,氢氧化钠固体溶于水放出大量的热,温度升高;硝酸铵固体溶于水吸热,温度降低;氯化钠溶于水温度变化不大,故错误.
故选D.
点评 本题考查了氧化物的概念、分子的概念、电解水的知识以及物质溶解过程中的热量变化,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
19.PM2.5是指直径小于或等于2.5微米的颗粒物,它对人体危害很大.下列做法不利于保护环境的是( )
| A. | 尽量乘坐公交车或骑自行车出行 | B. | 露天焚烧废旧塑料解决“白色污染” | ||
| C. | 用清洁能源代替化石燃料 | D. | 植树造林增加绿化面积 |
3.进行化学实验必须注意安全,下列说法不正确的是( )
| A. | 不慎将酸或碱溶液溅到眼中,应立即用水冲洗 | |
| B. | 不慎洒出的酒精在桌上燃烧起来,应立即用湿抹布扑盖 | |
| C. | 不要尝实验室里所有药品的味道 | |
| D. | 配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌下慢慢加入浓硫酸 |
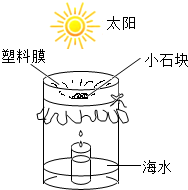 水是重要资源.
水是重要资源. 如图是a、b两种固体物质的溶解度曲线.
如图是a、b两种固体物质的溶解度曲线.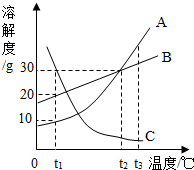 如图是A、B、C、三种物质的溶解度曲线.
如图是A、B、C、三种物质的溶解度曲线.