题目内容
4.X、M、N、Y、Z、W 6种常见物质,由氢、碳、氧、钠、氯、钙5种元素中的1~3种组成.(1)X俗称烧碱,其化学式为NaOH.
(2)碳与水蒸气在高温下发生置换反应,生成两种可燃性气体M和N,其微观示意图如下,请在方框中补全相应微粒的图示.

(3)M在高温下与某红色固体反应,生成与其元素组成相同的气体.该反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(4)在化学晚会上,小明同学选用X、Y、Z、W 4种物质为同学们做了变色小魔术,其操作及现象如下图所示(已知X、Z属于同类物质).

①Y溶液为稀盐酸.
②加入W溶液后溶液变浑浊的原因是Ca(OH)2+Na2CO3═CaCO3↓+2NaOH(用化学方程式表示,写出一定发生的化学反应方程式即可).
分析 已知X、M、N、Y、Z、W6种常见物质,由氢,碳,氧,钠,氯,钙5种元素中的1-3种组成,则:
(1)X俗称烧碱,推测为氢氧化钠.
(2)根据“碳与水蒸气在高温下发生置换反应,生成两种可燃性气体M和N”,根据微观示意图,推测碳与水蒸气在高温下反应生成一氧化碳和氧气,进行分析.
(3)根据“M在高温下与某红色固体反应,生成与其元素组成相同的气体”,推测M为一氧化碳,书写该反应的化学方程式.
(4)已知X,Z属于同类物质,根据图可推测:Y溶液为稀盐酸,Z溶液为氢氧化钙,W溶液为碳酸钠,进行分析.
解答 解:已知X、M、N、Y、Z、W6种常见物质,由氢,碳,氧,钠,氯,钙5种元素中的1-3种组成,则:
(1)X俗称烧碱,推测为氢氧化钠,故其化学式为NaOH.
(2)根据“碳与水蒸气在高温下发生置换反应,生成两种可燃性气体M和N”,根据微观示意图,推测碳与水蒸气在高温下反应生成一氧化碳和氧气,如图
(3)根据“M在高温下与某红色固体反应,生成与其元素组成相同的气体”,推测M为一氧化碳,由题意可知,在高温条件下,一氧化碳能与氧化铁反应,生成了铁和二氧化碳.反应的方程式是:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(4)已知X,Z属于同类物质,根据图可推测:Y溶液为稀盐酸,Z溶液为氢氧化钙,W溶液为碳酸钠,故氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,反应的化学方程式为:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
故答案为:
(1)NaOH;
(2)
(3)Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;(4)稀盐酸;Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
点评 本题的推断由组成物质的元素做为限定条件,因此,熟悉常见物质的组成、性质及变化规律对该题中所涉及物质的推断就至关重要了.

 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案| 物 质 | 甲 | 乙 | 丙 |
| 未溶解固体的质量/g | 7 | 0 | 3 |
| A. | 所得溶液可能都是饱和溶液 | |
| B. | 三种溶液中溶质的质量分数乙>丙>甲 | |
| C. | 升高温度,三种溶液中溶质的质量分数一定会改变 | |
| D. | 20℃时,甲的溶解度最小 |
| 清洁产品 | 除垢净 | 去污粉 | 管道通 |
| 主要成分 | 盐酸 | 碳酸钠 | 氢氧化钠、铝粉 |
(2)去污粉与除垢净不能混合使用,其原因是Na2CO3+2HCl═2NaCl+CO2↑+H2O(用化学方程式表示).
(3)管道通使用时不能接触皮肤,原因是NaOH具有强烈的腐蚀性.使用时利用Al与NaOH溶液反应放出大量的热,以加快NaOH与淤积物的作用,该反应的化学方程式为2Al+2NaOH+2H2O═2NaAlO2+3H2↑,其中铝元素的化合价变化为0~+3.
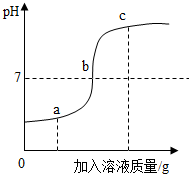 向20g溶质质量分数为3.65%的盐酸中逐滴加入NaOH溶液,得到的溶液pH变化图象如图所示.下列说法不正确的是( )
向20g溶质质量分数为3.65%的盐酸中逐滴加入NaOH溶液,得到的溶液pH变化图象如图所示.下列说法不正确的是( )| A. | a点对应的溶液中的溶质是NaCl和HCl | |
| B. | b点对应的溶液中Na+和Cl-的数目相等 | |
| C. | c点对应的溶液中Cl-的质量为0.71克 | |
| D. | 反应过程中生成NaCl的质量始终等于参加反应的HCl和NaOH的质量总和 |
| 选项 | 物质(括号内为杂质) | 杂质 | 除杂的试剂和方法 |
| A | NaOH溶液(Na2SO4) | 过量的Ba(OH)2溶液 | 过滤 |
| B | KCl(MnO2) | 水 | 溶解、过滤、洗涤干燥 |
| C | CO(CO2) | 足量氢氧化钠溶液 | 通入并干燥 |
| D | NaCl溶液(Na2CO3) | 足量稀盐酸 | 蒸发 |
| A. | A | B. | B | C. | C | D. | D |
| A. |  熄灭酒精灯 | B. |  读出液体的体积 | C. |  加热液体 | D. |  稀释浓硫酸 |


 人类利用化学变化,合成各种新材料,如合成纤维、合成塑料、合成橡胶等,新材料的应用,极大地促进了人.类社会的发展和人们生活水平的提高,请从化学视角回答下列问题:
人类利用化学变化,合成各种新材料,如合成纤维、合成塑料、合成橡胶等,新材料的应用,极大地促进了人.类社会的发展和人们生活水平的提高,请从化学视角回答下列问题: