题目内容
11.工业上用电解氧化铝的方法制取单质铝的化学反应方程式为2Al2O3$\frac{\underline{\;通电\;}}{\;}$4Al+3O2↑.对“电解10吨氧化铝最多生产多少吨铝?”一题,小丽和小明两位同学分别采用了两种不同的计算方法.| 小丽同学的解法 | 小明同学的解法 |
| 解:设最多生产铝的质量为x. 2Al2O3$\frac{\underline{\;通电\;}}{\;}$4Al+3O2↑ 204 108 10吨 x $\frac{204}{108}$=$\frac{10吨}{x}$ x=$\frac{108×10吨}{204}$≈5.3吨 答:最多生产5.3吨铝. | 解:氧化铝中铝元素的质量分数为 $\frac{Al的相对原子质量×2}{Al2O3的相对分子质量}$×100% =$\frac{27×2}{27×2+16×3}$×100% ≈53% 最多生产铝的质量为 10吨×53%=5.3吨 答:最多生产5.3吨铝. |
(1)你认为他们的解题思路和方法正确吗?正确.
(2)对“34克过氧化氢完全分解(化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑)产生氧气的质量为多少克?”一题,也能用上述两种方法解答吗?试试看,请你把能用的解法过程写出来.
分析 电解氧化铝时,氧化铝中的铝元素完全转化到铝中,因此两种方法都正确;
过氧化氢反应生成水和氧气,过氧化氢中的氧元素一部分转化到水中,一部分转化到氧气中,不能用小明同学的解法计算,因此应该用小丽同学的解法进行计算.
解答 解:(1)正确,这是因为电解氧化铝时,氧化铝中的铝元素完全转化到铝中.
故填:正确.
(2)过氧化氢反应生成水和氧气,过氧化氢中的氧元素一部分转化到水中,一部分转化到氧气中,不能用小明同学的解法计算,因此应该用小丽同学的解法进行计算;
设生成氧气质量为x,
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,
68 32
34g x
$\frac{68}{34g}$=$\frac{32}{x}$,
x=16g,
答:34克过氧化氢完全分解,产生氧气的质量为16g.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.下列化学方程式书写正确的是( )
| A. | 2Mg+O2↑$\frac{\underline{\;点燃\;}}{\;}$2MgO | B. | H2O2+MnO2═H2O+MnO2+O2 | ||
| C. | 4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 | D. | 4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5 |
16.区分氧气、空气和二氧化碳的最佳方法是( )
| A. | 观察气体颜色 | B. | 闻气味 | ||
| C. | 将燃着的木条放入各气体中 | D. | 分别通入紫色石蕊试液中 |
20.下列关于物质的量的叙述中,错误的是( )
| A. | 1mol任何物质都含有约6.02×1023个原子 | |
| B. | 2mol碳中含有约2×6.02×1023个碳原子 | |
| C. | 1mol水中含有2mol H原子和1mol O原子 | |
| D. | 1mol Ne 含有约6.02×1023个原子 |
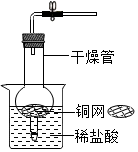 CO2是初中化学重点研究的气体之一.某化学兴趣小组设计了如下实验来探究CO2的制取和性质:
CO2是初中化学重点研究的气体之一.某化学兴趣小组设计了如下实验来探究CO2的制取和性质: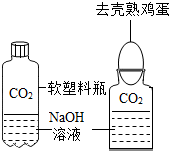 ①小明设计了甲、乙两个实验来验证CO2与NaOH发生了化学反应,如图所示.实验现象为:甲--软塑料瓶变瘪,乙--“瓶吞鸡蛋”.小虎同学认为上述实验是可行的.其共同原理是二氧化碳与氢氧化钠反应,产生的内外气压差.
①小明设计了甲、乙两个实验来验证CO2与NaOH发生了化学反应,如图所示.实验现象为:甲--软塑料瓶变瘪,乙--“瓶吞鸡蛋”.小虎同学认为上述实验是可行的.其共同原理是二氧化碳与氢氧化钠反应,产生的内外气压差.



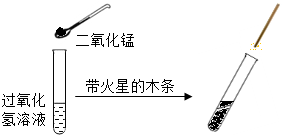 某学生学习了可用双氧水制氧气的知识后,想起自己家里也有一瓶消毒用双氧水.经查看发现已过期,但不知是否完全变质,于是他将该瓶双氧水带到学校,进行了如图所示的探究.试回答:
某学生学习了可用双氧水制氧气的知识后,想起自己家里也有一瓶消毒用双氧水.经查看发现已过期,但不知是否完全变质,于是他将该瓶双氧水带到学校,进行了如图所示的探究.试回答: