题目内容
4.水是宝贵的自然资源,在生产和生活中都有极其广泛的应用,请回答下列问题:(1)经过水质检验的自来水在运输过程中存在细菌污染,饮用该水前的处理方法是加热煮沸.
(2)硬水与软水的区别是硬水中含有大量的钙、镁离子.
(3)长期烧水的壶会有水垢,其成分为CaCO3和Mg(OH)2,实验室从该水垢中提取氯化钙晶体的主要流程如图:
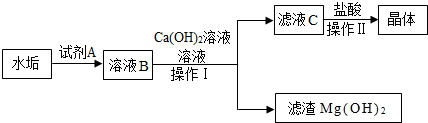
(ⅰ)试剂A是一种酸,其化学式为HCl.
(ⅱ)弦溶液B中加入Ca(OH)2溶液除去的主要离子是镁离子,写出发生的化学反应方程式Ca(OH)2+MgCl2═CaCl2+Mg(OH)2↓,操作Ⅰ的名称是过滤.
(ⅲ)向滤液C中加入盐酸的主要目的是除去氢氧化钙,操作Ⅱ的名称是蒸发结晶.
分析 (1)根据生活中杀灭自来水在传输过程中存在细菌的方法进行分析解答;
(2)根据硬水和软水的区别分析;
(3)根据反应的过程及现象进行分析;根据物质间的反应及化学方程式的书写方法,实验操作名称分析;根据除杂实验设计进行分析;
解答 解:(1)自来水在传输过程中存在细菌污染,人们在家中饮用该水之前可以加热煮沸,能有效的杀灭细菌.故填:加热煮沸;
(2)软硬水的区别是硬水中含有大量的钙、镁离子,而软水中较少,故填:硬水中含有大量的钙、镁离子;
(3)盐酸与水垢反应后生成氯化钙和氯化镁,故试剂A是盐酸,其化学式为HCl;加入氢氧化钙溶液能与氯化镁反应生成氢氧化镁沉淀,通过过滤除去氢氧化镁,故除去的主要离子是镁离子,反应的化学方程式为:Ca(OH)2+MgCl2═CaCl2+Mg(OH)2↓,操作Ⅰ的名称是过滤,把氢氧化镁分离出来.滤液中含有氯化钙和氢氧化钙,加入盐酸可以除去氢氧化钙,操作Ⅱ的名称是蒸发结晶;
故填:(ⅰ)HCl;(ⅱ)镁离子;Ca(OH)2+MgCl2═CaCl2+Mg(OH)2↓;过滤;(ⅲ)除去氢氧化钙;蒸发结晶.
点评 本题考查了有关水的性质实验,完成此题,可以依据已有的知识进行.

练习册系列答案
 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目
14.草木灰是农家肥料,其有效成分是K2CO3,它属于( )
| A. | 磷肥 | B. | 钾肥 | C. | 氮肥 | D. | 复合肥 |
15.某校兴趣小组,在实验室中做制取氧气的实验,他们取氯酸钾和二氧化锰的混合物3.0g,放入大试管中加热,并在不同时刻测定试管内剩余固体物质的质量如图:
分析表中数据,完成下列问题:
(1)氯酸钾中钾、氯、氧三种元素质量比为78:71:96(最简整数比).
(2)生成氧气的质量为0.96g.
(3)原混合物中氯酸钾的质量是多少?二氧化锰的质量是多少?(要有计算过程,计算结果保留到小数点后两位)
| 反应时间/min | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 | 3.5 |
| 剩余固体质量/g | 2.55 | 2.25 | 2.10 | 2.04 | 2.04 | 2.04 |
(1)氯酸钾中钾、氯、氧三种元素质量比为78:71:96(最简整数比).
(2)生成氧气的质量为0.96g.
(3)原混合物中氯酸钾的质量是多少?二氧化锰的质量是多少?(要有计算过程,计算结果保留到小数点后两位)
12.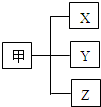 归类是我们经常用到的一种学习方法.若用如图所示的形式对所学知识进行归类,则表中的选项与图相符的是( )
归类是我们经常用到的一种学习方法.若用如图所示的形式对所学知识进行归类,则表中的选项与图相符的是( )
 归类是我们经常用到的一种学习方法.若用如图所示的形式对所学知识进行归类,则表中的选项与图相符的是( )
归类是我们经常用到的一种学习方法.若用如图所示的形式对所学知识进行归类,则表中的选项与图相符的是( ) | 选项 | 甲 | X | Y | Z |
| A | 常见的碱 | 烧碱 | 纯碱 | 熟石灰 |
| B | 常见的矿物燃料 | 煤 | 石油 | 天然气 |
| C | 常见的合金 | 钢铁 | 生铁 | 氧化铁 |
| D | 常见的行星 | 地球 | 太阳 | 月球 |
| A. | A | B. | B | C. | C | D. | D |
19.下列实验设计中不能达到实验目的是( )
| 实验设计 | 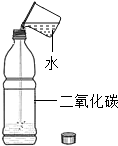 |  |  |  |
| 实验目的 | 验证二氧化碳与水反应生成碳酸 | 探究水的组成 | 证明石墨有导电性 | 验证氢气的密度比空气小 |
| 选项 | A | B | C | D |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
9.AgNO3固体见光或受热易分解,故保存在棕色瓶中,AgNO3见光分解时产生一种有刺激性气味的气体,该气体可能是( )
| A. | SO2 | B. | NH3 | C. | N2 | D. | NO2 |
16.实验桌上现有包白色粉末,可能是氢氧化钠、硫酸钠、碳酸钠和氯化铜的两种或两种以上组成.现将其放入一干净的烧杯M中,加入足量的水后,固体全部溶解得到无色溶液,再滴加几滴无色酚酞,溶液变为红色.
为进一步确定白色粉末的成分,同学们进行了如下探究.
【查阅资料】碳酸钠溶液呈碱性;氯化钡溶液和硫酸钠溶液呈中性.
【讨论猜想】进过分析,针对白色粉末的组成,大家提出如下猜想:
小红:氢氧化钠、硫酸钠; 小华:氢氧化钠、碳酸钠;
小明:碳酸钠、硫酸钠; 小亮:氢氧化钠、碳酸钠和硫酸钠.
【实验探究】四位同学共同设计并进行了如下实验:
实验完毕后,同学们将试管A、B中的物质倒在同一烧杯中,然后过滤,滤液中除酚酞外一定还含有的溶质有HCl和NaCl.
为进一步确定白色粉末的成分,同学们进行了如下探究.
【查阅资料】碳酸钠溶液呈碱性;氯化钡溶液和硫酸钠溶液呈中性.
【讨论猜想】进过分析,针对白色粉末的组成,大家提出如下猜想:
小红:氢氧化钠、硫酸钠; 小华:氢氧化钠、碳酸钠;
小明:碳酸钠、硫酸钠; 小亮:氢氧化钠、碳酸钠和硫酸钠.
【实验探究】四位同学共同设计并进行了如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 1.取烧杯M中的少量溶液于试管A中,向其中加入一定量的稀盐酸 | 溶液由红色变为无色且有气泡产生. | 小红 的猜想不正确 |
| 2.另取烧杯M中的少量溶液于另一试管B中,向其中加入过量氯化钡溶液. | 出现白色沉淀 | 小亮的猜想正确 |
| 3.继续向试管B中加入过量的稀盐酸 | 沉淀一部分消失,并生成气泡 |