题目内容
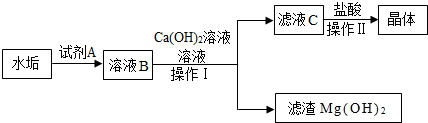
15.某校兴趣小组,在实验室中做制取氧气的实验,他们取氯酸钾和二氧化锰的混合物3.0g,放入大试管中加热,并在不同时刻测定试管内剩余固体物质的质量如图:| 反应时间/min | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 | 3.5 |
| 剩余固体质量/g | 2.55 | 2.25 | 2.10 | 2.04 | 2.04 | 2.04 |
(1)氯酸钾中钾、氯、氧三种元素质量比为78:71:96(最简整数比).
(2)生成氧气的质量为0.96g.
(3)原混合物中氯酸钾的质量是多少?二氧化锰的质量是多少?(要有计算过程,计算结果保留到小数点后两位)
分析 (1)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答;
(2)根据质量守恒定律,反应前后物质的质量总和相等,由此可计算出生成氧气的质量;
(3)根据化学方程式,求出氯酸钾的质量,进而求出混合物中二氧化锰的质量.
解答 解:
(1)在氯酸钾中,钾、氯、氧三种元素的质量比为39:35.5:(16×3)=78:71:96;故填:78:71:96;
(2)根据质量守恒定律,反应前后物质的质量总和相等,
则生成氧气的质量=反应前物质的质量-反应后剩余固体的质量=3.0g-2.04g=0.96g;故填:0.96;
(3)设原混合物中氯酸钾的质量为x
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
245 96
x 0.96g
$\frac{245}{x}=\frac{96}{0.96g}$
解得:x=2.45g
原混合物中二氧化锰的质量=3.0g-2.45g=0.55g
答案:
(1)78:71:96;
(2)0.96;
(3)原混合物中氯酸钾的质量为2.45g,二氧化锰的质量为0.55g.
点评 本题主要考查学生对物质质量守恒定律的认识以及利用化学方程式和质量分数公式进行计算的能力.

练习册系列答案
相关题目
3.“十面霾伏”,已成2013年,我国十大新词语之一,PM2.5是首要污染物,2014年5月7日,国家环保部公布,我市空气质量指数达到204,为重度污染.下列措施,不能减少雾霾的是( )
| A. | 加大城市绿化园林建设 | B. | 禁止焚烧桔杆 | ||
| C. | 大力发展火力发电 | D. | 建筑工地,定时洒水降尘 |
20.下列物质的用途,主要取决于化学性质的是( )
| A. | 用干冰作制冷剂 | B. | 用铜丝制导线 | ||
| C. | 用活性炭吸附色素 | D. | 用氮气作保护气 |

 .
.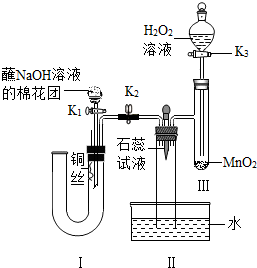 某硫酸化工厂附近居民反映:近来空气中有异味,庄稼枯黄,某学习小组对该厂附近的雨水进行检测,测得pH约为5.1,说明该区域的雨水呈酸性(填“酸性”或“碱性”或“中性”)
某硫酸化工厂附近居民反映:近来空气中有异味,庄稼枯黄,某学习小组对该厂附近的雨水进行检测,测得pH约为5.1,说明该区域的雨水呈酸性(填“酸性”或“碱性”或“中性”)