题目内容
16.请填写下列空白:(1)地壳中含量最多的金属元素是Al;
(2)气体的溶解度随温度的升高而减小,随压强的增大而增大.
(3)物质燃烧必须同时满足的三个条件是①可燃物;②与氧气接触;③温度达到着火点;
(4)碘酸钾(KIO3)中,碘元素化合价是+5.
分析 (1)根据地壳中各元素含量的排序及元素的分类判断.
(2)利用气体的溶解度随温度的升高而减小,随着压强的增大而增大,进行分析解答.
(3)根据燃烧的条件解答本题.
(4)根据在化合物中正负化合价代数和为零,进行解答.
解答 解:(1)地壳含量较多的元素按含量从高到低的排序为:氧、硅、铝、铁,在金属元素中含量最多的是铝.
(2)气体的溶解度受温度、压强的影响较大,气体的溶解度随温度的升高而减小,随着压强的增大而增大.
(3)燃烧要同时满足的三个条件:①物质具有可燃性、②与氧气接触、③温度达到可燃物的着火点.
(4)根据在化合物中正负化合价代数和为零,钾显+1价,氧显-2价,设碘酸钾(KIO3)中碘元素的化合价为x,则:(+1)+x+(-2)×3=0,解x=+5.
故答案为:(1)Al;(2)减小;增大;(3)与氧气接触;温度达到着火点;(4)+5.
点评 本题难度不大,但综合性较强,主要考查学生运用所学化学知识分析和解决实际问题的能力,增加了学生分析问题的思维跨度.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
6.我县某中学化学实验小组在探究酸的性质时,做了如下实验:
(1)分别向A试管(装有碳酸钠粉末),B试管(装有碳酸钙粉末)中注入一定量的稀盐酸,两支试管内均观察到的现象是产生气泡,A、B两支试管固体粉末全部消失,最终变成无色溶液,写出A试管中发生反应的化学方程式:Na2CO3+2HCl═2NaCl+H2O+CO2↑.
(2)实验结束后,小组同学将A、B两试管中的废液倒入同一只烧杯中,发现烧杯中的废液变浑浊.写出产生浑浊现象的化学方程式Na2CO3+CaCl2═CaCO3↓+2NaCl.
(3)实验小组的同学将烧杯中的物质进行过滤,对滤液中的溶质的成分展开探究.
【提出猜想】
猜想1:滤液中的溶质是NaCl.
猜想2:滤液中的溶质是NaCl和Na2CO3.
猜想3:滤液中的溶质是NaCl和CaCl2.
【设计实验】请你选择一种猜想进行验证.
(1)分别向A试管(装有碳酸钠粉末),B试管(装有碳酸钙粉末)中注入一定量的稀盐酸,两支试管内均观察到的现象是产生气泡,A、B两支试管固体粉末全部消失,最终变成无色溶液,写出A试管中发生反应的化学方程式:Na2CO3+2HCl═2NaCl+H2O+CO2↑.
(2)实验结束后,小组同学将A、B两试管中的废液倒入同一只烧杯中,发现烧杯中的废液变浑浊.写出产生浑浊现象的化学方程式Na2CO3+CaCl2═CaCO3↓+2NaCl.
(3)实验小组的同学将烧杯中的物质进行过滤,对滤液中的溶质的成分展开探究.
【提出猜想】
猜想1:滤液中的溶质是NaCl.
猜想2:滤液中的溶质是NaCl和Na2CO3.
猜想3:滤液中的溶质是NaCl和CaCl2.
【设计实验】请你选择一种猜想进行验证.
| 实验步骤 | 预计实验现象 | 预计结论 |
| 取少量的溶液与试管中, 滴加稀盐酸和碳酸钠溶液,滴加稀盐酸,或滴加碳酸钠溶液 | 无明显现象,或产生气泡,或产生白色沉淀 | 猜想1,或2,或3正确 |
7.下列实验现象记录正确的是( )
| A. | 铁丝在氧气中剧烈燃烧,火星四射,生成四氧化三铁 | |
| B. | 打开盛有浓盐酸的试剂瓶看到有大量白烟 | |
| C. | 长期敞口放置的石灰水表面有层白色的膜,加入稀盐酸后白膜溶解并有气体放出 | |
| D. | 紫色石蕊试液滴加到稀盐酸中,石蕊试液由紫色变为蓝色 |
11.某化学兴趣小组同学用大理石和盐酸反应制取CO2,将制得的气体通入澄清石灰水时,未变浑浊,便产生了好奇.对此展开了探究活动,请你参与探究并填写空格.
【提出问题】澄清石灰水未变浑浊的原因是什么?
【假设猜想】假设一:石灰水变质 假设二:制得气体中无CO2
【探究实验】为探究假设是否成立,小组同学取原试剂瓶中澄清石灰水进行如下实验:
【分析推理】通过上述探究,否定了两个假设,小组同学确定澄清石灰水未变浑浊是其他原因造成的.于是他们对反应物进行了分析,根据盐酸的挥发性,推测制得气体中有较多的HCl气体.
写出上述实验中AgNO3溶液中发生的化学反应方程式HCl+AgNO3═AgCl↓+HNO3.
【得出结论】澄清石灰水未变浑浊的原因是制得的CO2中有一定量HCl气体.有一定量HCI气体存在时,澄清石灰水为什么不变浑浊?请解释氯化氢先和氢氧化钙反应生成氯化钙和水.
【评价反思】小组中有一位同学认为【验证实验】中不能用紫色石蕊溶液证明HCI气体的存在,原因是二氧化碳能和水反应生成碳酸,碳酸能使石蕊试液变红色.
【提出问题】澄清石灰水未变浑浊的原因是什么?
【假设猜想】假设一:石灰水变质 假设二:制得气体中无CO2
【探究实验】为探究假设是否成立,小组同学取原试剂瓶中澄清石灰水进行如下实验:
| 实验操作 | 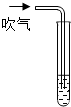 | 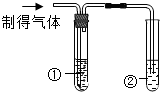 |
| 实验现象 | 澄清石灰水变浑浊 | 试管①澄清石灰水未变浑浊;试管②澄清石灰水变浑浊 |
| 实验结论 | 说明石灰水未变质 | 说明值得气体中有二氧化碳气体 |
| 实验操作 | 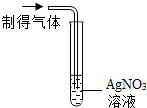 | 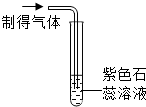 |
| 实验现象 | 出现白色沉淀 | 紫色石蕊试液变红 |
| 实验结论 | 有HCl气体 | 有HCl气体 |
【得出结论】澄清石灰水未变浑浊的原因是制得的CO2中有一定量HCl气体.有一定量HCI气体存在时,澄清石灰水为什么不变浑浊?请解释氯化氢先和氢氧化钙反应生成氯化钙和水.
【评价反思】小组中有一位同学认为【验证实验】中不能用紫色石蕊溶液证明HCI气体的存在,原因是二氧化碳能和水反应生成碳酸,碳酸能使石蕊试液变红色.
8.下列变化中,属于化学变化的是( )
| A. | 汽油挥发 | B. | 燃放鞭炮 | C. | 瓷碗破碎 | D. | 铜丝折弯 |
 人体内有很多种酶,不同的酶催化体内不同的化学反应.例如过氧化氢酶能催化H2O2分解形成H2O和O2,这种酶在马铃薯体内也存在.某同学将马铃薯块茎磨碎、过滤得到提取液进行了三次实验:
人体内有很多种酶,不同的酶催化体内不同的化学反应.例如过氧化氢酶能催化H2O2分解形成H2O和O2,这种酶在马铃薯体内也存在.某同学将马铃薯块茎磨碎、过滤得到提取液进行了三次实验: 已知,A、B、C、D四种物质之间存在如图转化关系.其中C是单质,D是相对分子质量最小的氧化物.试回答:
已知,A、B、C、D四种物质之间存在如图转化关系.其中C是单质,D是相对分子质量最小的氧化物.试回答: