题目内容
1. 已知,A、B、C、D四种物质之间存在如图转化关系.其中C是单质,D是相对分子质量最小的氧化物.试回答:
已知,A、B、C、D四种物质之间存在如图转化关系.其中C是单质,D是相对分子质量最小的氧化物.试回答:(1)写出A、C、D三种物质的化学式:AFe、CH2、DH2O.
(2)浅绿色溶液B中溶质的化学式FeSO4.
(3)写出A→C的化学方程式:Fe+H2SO4═FeSO4+H2↑.
分析 根据题意,C是单质,D是相对分子质量最小的氧化物,则D为水;A能与稀硫酸反应生成浅绿色溶液B和C,C与氧气反应生成水,则C为氢气,铁与稀硫酸反应生成硫酸亚铁溶液和氢气,硫酸亚铁溶液显浅绿色,则A为铁,B为硫酸亚铁溶液;据此进行分析解答.
解答 解:C是单质,D是相对分子质量最小的氧化物,则D为水;A能与稀硫酸反应生成浅绿色溶液B和C,C与氧气反应生成水,则C为氢气,铁与稀硫酸反应生成硫酸亚铁溶液和氢气,硫酸亚铁溶液显浅绿色,则A为铁,B为硫酸亚铁溶液.
(1)A、C、D三种物质的化学式分别是Fe、H2、H2O.
(2)浅绿色溶液B为硫酸亚铁溶液,溶质是硫酸亚铁,其化学式为:FeSO4.
(3)A→C,即铁与稀硫酸反应生成硫酸亚铁溶液和氢气,反应的化学方程式为:Fe+H2SO4═FeSO4+H2↑.
故答案为:(1)Fe;H2;H2O;(2)FeSO4;(3)Fe+H2SO4═FeSO4+H2↑.
点评 本题难度不大,解题时往往需要从题目中挖出一些明显或隐含的条件,抓住突破口(突破口往往是现象特征、反应特征等),获得结论,最后把结论代入原题中验证.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.小亮在做“盐酸中和氢氧化钠溶液”的实验时,滴加盐酸前忘了加入指示剂,导致无法判断该中和反应进行的程度.于是他对所得溶液的酸碱性进行探究.
探究目的:探究所得溶液的酸碱性
提出猜想:所得溶液可能呈碱性,也可能呈中性,还可能呈酸性.
实验验证:
[分析与思考]
(1)若溶液呈碱性,则溶液中使其呈碱性的离子是OH-(填写微粒符号).
(2)若无色酚酞试液不变色,为了进一步确定溶液的酸碱性,小亮提出了以下方案:
方案一:取样,加入碳酸钠溶液,若观察到有气泡产生,则所取溶液呈酸性;若无明显现象,则呈中性.
方案二:取样,加入金属锌,若有有气泡产生,则所取溶液呈酸性;若无明显现象,则呈中性.
探究目的:探究所得溶液的酸碱性
提出猜想:所得溶液可能呈碱性,也可能呈中性,还可能呈酸性.
实验验证:
| 实验操作 | 实验现象 | 结论 |
| 用试管取该溶液1~2ml,滴入1~2滴无色酚酞试液,振荡 | 无色酚酞试液变红 | 溶液呈碱性 |
| 无色酚酞试液不变色 | 溶液呈中性或酸性 |
(1)若溶液呈碱性,则溶液中使其呈碱性的离子是OH-(填写微粒符号).
(2)若无色酚酞试液不变色,为了进一步确定溶液的酸碱性,小亮提出了以下方案:
方案一:取样,加入碳酸钠溶液,若观察到有气泡产生,则所取溶液呈酸性;若无明显现象,则呈中性.
方案二:取样,加入金属锌,若有有气泡产生,则所取溶液呈酸性;若无明显现象,则呈中性.
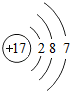
6. 某微粒的结构示意图如下所示,下列有关该微粒的说法错误的是( )
某微粒的结构示意图如下所示,下列有关该微粒的说法错误的是( )
 某微粒的结构示意图如下所示,下列有关该微粒的说法错误的是( )
某微粒的结构示意图如下所示,下列有关该微粒的说法错误的是( )| A. | 该微粒的原子核内有 11 个质子 | |
| B. | 该微粒在化学反应中易失去 1 个电子 | |
| C. | 该微粒的原子核外有 3 个电子层 | |
| D. | 该图表示的微粒是一种离子 |
10.实验室常用的下列仪器中,用合成材料制成的是( )
| A. |  塑料药匙 | B. |  不锈钢坩埚钳 | C. |  陶瓷蒸发皿 | D. |  玻璃集气瓶 |
 阅读材料,回答问题:
阅读材料,回答问题:
 碳和部分碳的化合物间转化关系如图所示.
碳和部分碳的化合物间转化关系如图所示.